
海帶中提取碘的實驗方法:①稱取3 g干海帶,用刷子把干海帶表面的附著物刷凈;②將海帶剪碎,用酒精潤濕(便于灼燒)后,放在坩堝中;③用酒精燈灼燒盛有海帶的坩堝,至海帶完全成灰,停止加熱,冷卻;④將海帶灰轉移到小燒杯中,再向燒杯中加入10 mL蒸餾水,攪拌,煮沸2~3 min,使可溶物溶解,過濾;⑤向濾液中滴入幾滴硫酸,再加入約1 mL H2O2溶液,觀察現象。下列說法正確的是
A.步驟①中也可以用水洗滌除去海帶表面的附著物
B.步驟④過濾操作需要兩種玻璃儀器
C .步驟⑤所得的溶液中加入淀粉可看到溶液變為藍色
.步驟⑤所得的溶液中加入淀粉可看到溶液變為藍色
D.通過以上①~⑤步驟即可得到純度高的I2
 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源:2016-2017學年河北省高一上第一次月考化學卷(解析版) 題型:選擇題
兩份質量相同的CH4和NH3相比較,下列結論錯誤的是
A.分子個數比為17:16 B.原子個數比為17:16
C.氫原子個數比為17:12 D.氫原子質量比為 17:12
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上第三次月考化學卷(解析版) 題型:選擇題
無色透明溶液中能大量共存的離子組是
A.Na+、Al3+、HCO3-、NO3- B.AlO2-、Cl-、Mg2+、K+
C.NH4+、Na+、CH3COO-、NO3- D.Na+、NO3-、ClO-、I-
查看答案和解析>>
科目:高中化學 來源:2017屆河北省石家莊市高三上第一次階段考試化學卷(解析版) 題型:實驗題
某氯化鐵與氯化亞鐵的混合物。現要測定其中鐵元素的質量分數,實驗按以下步驟進行:
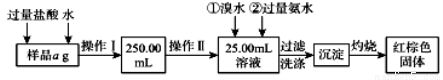
請根據上面流程,回答以下問題:
(1)操作Ⅰ所用到的玻璃儀器除燒杯、玻璃棒外,還必須有 、 。 (填儀器名稱)
(2)請寫出加入溴水發生的離子反應方程式 。
(3)將沉淀物加熱,冷卻至室溫,用天平稱量其質量為b1g。再次加熱并冷卻至室溫稱量其質量為b2g,若b1-b2=0.3g,則接下來還應進行的操作是 。若蒸發皿質量是 W1 g,蒸發皿與加熱后固體總質量是W2g,則樣品中鐵元素的質量分數是 。有同學提出,還可以采用以下方法來測定:

①溶解樣品改用了硫酸,而不用鹽酸,原因是 。
②選擇的還原劑是否能用鐵 (填“是”或“否”),原因是: 。
③若滴定用掉c mol/ L KMnO4溶液bmL,則樣品中鐵元素的質量分數是 。
查看答案和解析>>
科目:高中化學 來源:2017屆河北省石家莊市高三上第一次階段考試化學卷(解析版) 題型:選擇題
某離子反應中涉及H2O、ClO-、NH4+、H+、N2、Cl-六種微粒。其中N2的物質的量隨時間變化的曲線如圖所示。下列判斷正確的是

A.該反應的還原劑是Cl-
B.消耗1 mol還原劑,轉移6 mol電子
C.氧化劑與還原劑的物質的量之比為2:3
D.反應后溶液的酸性明顯增強
查看答案和解析>>
科目:高中化學 來源:2017屆河北省石家莊市高三上第一次階段考試化學卷(解析版) 題型:選擇題
關于Na2CO3和NaHCO3的比較中,下列說法不正確的是
A.NaHCO3固體受熱容易分解,而Na2CO3固體受熱不容易分解
B.等質量的Na2CO3和NaHCO3分別與足量的鹽酸反應,前者消耗鹽酸的物質的量比后者多
C.向等物質的量濃度的Na2CO3和NaHCO3溶液分別滴加2滴酚酞溶液,前者顏色比后者深
D.Na2CO3溶液和NaHCO3溶液分別與Ba(OH)2溶液反應的離子方程式相同
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省等四校高三上10月聯考化學試卷(解析版) 題型:簡答題
TiO2在工業生產和日常生活中有重要用途。
I、工業上用鈦鐵礦石(FeTiO3,含FeO、Al2O3、SiO2等雜質)經過下述反應制得:
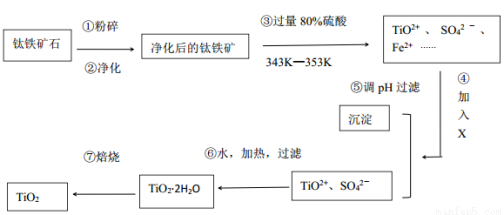
其中,步驟③發生的反應為:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)寫出鈦元素在周期表中的位置______________。
凈化鈦礦石時,是否需要除去雜質FeO?____ ________(填“需要”或“不需要”)
(2)凈化鈦礦石時,需用濃氫氧化鈉溶液來處理,寫出該過程中兩性氧化物發生反應的離子反應方程式:____________________。
(3)④中加入的X可能是( )
A.H2O2 B.KMnO4 C.KOH D.SO2
(4)④⑤兩步的目的是___________________________。
(5)寫出⑥的化學反應方程式_____________________。
II、TiO2可通過下述兩種方法制備金屬鈦:方法一是電解TiO2來獲得Ti(同時產生O2):
將處理過的TiO2作陰極,石墨為陽極,熔融CaCl2為電解液,用碳塊作電解槽池。
(6)陰極反應的電極反應式為_____________________。
(7)電解過程中需定期向電解槽池中加入碳塊的原因是__________________。
方法二是先將TiO2與Cl2、C反應得到TiCl4,再用鎂還原得到Ti。因下述反應難于發生:
TiO2 (s) +2Cl2 (g) TiCl4(1)+O2 (g) △H= +151 kJ/mol
TiCl4(1)+O2 (g) △H= +151 kJ/mol
所以不能直接由TiO2和Cl2反應(即氯化反應)來制取TiCl4。請從反應原理角度說明該反應難進行的原因__________________。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省等四校高三上10月聯考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列說法正確的是
A.44.Og14CO2與14N2O的混合物中所含中子數為22NA
B.標準狀況下,2.24L甲醛所含o鍵數目為0.3NA
C.常溫常壓下,4.5gH2O與足量Na2O2反應轉移的電子數目為0.5 NA
D.50mL 18mol/L硫酸與足量Cu共熱,轉移的電子數為0.9NA
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上學期第二次段考化學試卷(解析版) 題型:選擇題
M、Q、R、V為分別占有前3周期的元素,其原子序數依次增加,M和R、Q和V屬于同一主族,且它們的最外層電子數之和為14。下列說法中正確的是( )
A.單質的沸點:M>Q
B.Q元素的陰離子和V元素的陰離子都只有還原性[
C.M 、Q、R、V
、Q、R、V 四種元素組成的化合物的水溶液可以是
四種元素組成的化合物的水溶液可以是 堿
堿 性、中性和酸性
性、中性和酸性
D.Q與R可以組成2種離子化合物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com