
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-,Br-,CrO4-,濃度均為0.010mol/L,向該溶液中逐滴加入0.010mol/L的AgNO3溶液時,三種陰離子產生沉淀的先后順序為
A. Cl-、Br-、CrO4- B. Br-、Cl-、CrO4- C. CrO4-、Br-、Cl- D. Br-、CrO4-、Cl-
科目:高中化學 來源:2017屆河南省安陽市高三第二次模擬考試理綜化學試卷(解析版) 題型:選擇題
下列實驗對應的現象及結論均正確,且兩者具有因果關系的是
選項 | 實驗 | 現象 | 結論 |
A | 向稀硝酸與過量銅粉反應后的溶液中滴加稀硫酸 | 有氣泡生成 | 常溫下,銅與稀硫酸反應生成SO2 |
B | 在酒精燈上加熱鋁箔 | 鋁熔化,但熔化的鋁不滴落 | Al2O3的熔點比Al高 |
C | 向Fe(SCN)3溶液中滴加稀NaOH溶液 | 溶液有紅色變為紅褐色 | 減小反應物濃度、平衡向逆反應方向移動 |
D | 選用酚酞作試劑,用NaOH溶液滴定醋酸溶液 | 溶液變為粉紅色 | NaOH溶液過量 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高一下學期第一次月考化學試卷(解析版) 題型:實驗題
某化學探究小組擬用銅片制取Cu(NO3)2,并探究其化學性質。
Ⅰ、他們先把銅粉放在空氣中灼燒,再與稀硝酸反應制取硝酸銅。
(1)如果直接用銅屑與稀硝酸反應來制取硝酸銅:
①銅屑與稀硝酸反應的化學反應方程式為 ;
②可能導致的兩個不利因素是_____________、_________ _____。
(2)實驗中,欲從反應后的溶液中得到硝酸銅晶體,實驗操作步驟按順序是___ _、__ _、過濾、晾干。
Ⅱ、為了探究Cu(NO3)2在酸性條件下跟鐵單質的反應。他們取一支試管,加入Cu(NO3)2溶液,滴入適量稀硫酸酸化,再加入一定量鐵粉,實驗后沒有固體殘留物質。
(3)該探究小組對反應后溶液中鐵元素的價態進行探究,他們設計了實驗方案,并進行實驗。請按下表格式補充寫出實驗操作步驟、預期現象與結論。
實驗操作步驟 | 預期現象與結論 |
步驟1:觀察樣品 | 溶液呈藍綠色,①_____(填“能”或“不能”)確定產物中鐵元素的價態 |
步驟2:取少量溶液,滴加酸性KMnO4溶液 |
|
步驟3:③另取少量溶液,滴加KSCN溶 |
|
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列說法正確的是( )
A. 含1molFeCl3的飽和溶液滴入沸水中得到膠體數目為NA
B. 在標準狀況下,22.4LCl2和HCl的混合氣體中含有的分子總數為2×6.02×1023
C. 常溫常壓下,7.8gNa2S固體和7.8gNa2O2固體中含有的陰離子數目均為0.1NA
D. 標準狀況下,Na2O2與足量的CO2反應生成2.24LO2,轉移電子數為0.4NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:簡答題
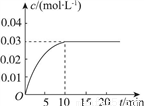
向一容積為5L的恒容密閉容器內,充入0.2molCO和0.4molH2O,在一定條件下發生反應:CO(g)+H2O(g)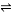 CO2(g)+H2(g) ΔH>0。反應中CO2的濃度(c)隨時間(t)的變化關系如圖所示。
CO2(g)+H2(g) ΔH>0。反應中CO2的濃度(c)隨時間(t)的變化關系如圖所示。
回答下列問題:
(1)下列敘述能判斷該反應達到平衡狀態的是________(填序號)。
①H2O的質量不再變化
②混合氣體的總壓強不再變化
③CO、H2O、CO2、H2的濃度都相等
④單位時間內生成amolCO,同時生成amolH2
(2)0~10min時段,反應速率v(H2)=________;反應達到平衡時,c(H2O)=________,CO的轉化率為________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:選擇題
下列說法正確的是
A. 用直接加熱并蒸干FeCl3溶液的方法可制得純凈的無水FeCl3
B. 等物質的量濃度的Na2CO3溶液和CH3COONa溶液的pH,前者大于后者
C. 中和等體積、等物質的量濃度的鹽酸和醋酸溶液,消耗NaOH的物質的量不相等
D. 對于有氣體參加的反應,增大氣體反應物濃度,活化分子百分數增大,反應速率加快
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:選擇題
下列事實不能用勒夏特列原理解釋的是
A. 對平衡體系H2(g)+I2(g) 2HI(g)加壓后,混合氣體的顏色加深
2HI(g)加壓后,混合氣體的顏色加深
B. 用稀鹽酸洗滌AgCl沉淀比用等體積的蒸餾水洗滌損失的AgCl少
C. 實驗室可用排飽和食鹽水的方法收集氯氣
D. 工業合成三氧化硫的過程中使用過量的氧氣,以提高二氧化硫的轉化率
查看答案和解析>>
科目:高中化學 來源:2017屆河南省濮陽市高三第一次模擬考試理綜化學試卷(解析版) 題型:推斷題
前四周期元素A、B、C、D、E的原子序數依次增大,基態A原子核外電子占鋸3個軌道,基態B原子核外電子占據3個能級且每個能級上電子數相等,C的雙原子單質分子中σ鍵和π鍵數目之比為1:2,D的最高正化合價和最低負化合價之和等于4;基態E原子核外有6個未成對電子。
(1)基態E原子的核外電子排布式為______;基態D原子核外電子占據的能量最高的能級符號為_____________。
(2)A元素的各級電離能如下:
能級(I) | I1 | I2 | I3 | I4 | I5 |
電離能/kJ·mol-1 | 800.6 | 2427 | 3660 | 25026 | 32827 |
分析上表數據知,相鄰兩個電子的電離能中,I3和I4之間差異最大,其主要原因是______________。
(3)A、B、C元素的最高價氧化物對應的水化物酸性依次增強,其原因是________。
(4)氯元素與A、B、C元素組成的共價分子ACl3、BCl4、CCl3中,中心原子采用sp3雜化、立體構型為三角錐形的是_______(填分子式)。
(5)(DC)4為熱色性固體,且有色溫效應。低于-30℃時為淡黃色,室溫下為橙黃色,高于100℃時為深紅色。在淡黃色→橙黃色→深紅色的轉化中,破壞的作用力是____;在常壓下,(DC)4高于130℃分解為相應的單質,這一變化中破壞的作用力是_______。在B、C、D的簡單氣態氫化物中,屬于非極性分子的是______(填分子式,下同),常與Cu2+、Zn2+、Ag+等形成配離子的是_______________。
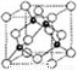
(6)A、C形成立方晶體,晶體結構類似金剛石,如圖所示。已知:該晶體密度為ρg·㎝-3,NA代表阿伏伽德羅常數的值。
①該晶體的化學式為__________。
②在該晶體中,A與C形成共價鍵的鍵長(d)為_____pm。
查看答案和解析>>
科目:高中化學 來源:2017屆海南省瓊海市高三下學期第一次月考化學試卷(解析版) 題型:填空題
(1)已知咖啡酸的結構如圖所示。關于咖啡酸的描述正確的是:(______)
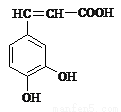
A.分子式為C9H5O4
B.1 mol 咖啡酸最多可與5 mol 氫氣發生加成反應
C.與溴水既能發生取代反應,又能發生加成反應
D.1 mol 咖啡酸最多可與3 mol Na2CO3發生反應
(2)A、B、C、D1、D2、E、F、G、H均為有機化合物,請根據下列圖示回答問題。
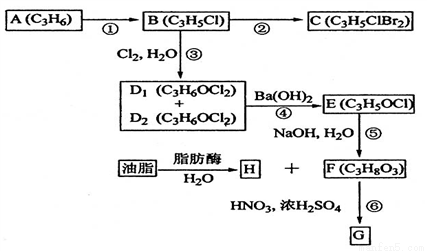
(1)直鏈有機化合物A的結構簡式是__________________;
(2)B中官能團的名稱為___________,H中含氧官能團的結構簡式為____________;
(3)①的反應試劑和反應條件是___________________,③的反應類型是_____________;
(4)B生成C的化學方程式是___________________;
D1或D2生成E的化學方程式是___________________;
(5)G可應用于醫療、爆破等,由F生成G的化學方程式是________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com