
【題目】化學與我們的生活密切相關,請回答:
(1)在生活中要注意飲食平衡,蛋白質屬于_______(填序號,下同)食物,番茄屬于______食物;①酸性 ②堿性
(2)有四種常見藥物①阿司匹林、②青霉素、③胃舒平、④麻黃堿. 某同學胃酸過多,應該服用______(填序號,下同);從用藥安全角度考慮,使用前要進行皮膚敏感性測試的是_____;由于具有興奮作用,國際奧委會嚴禁運動員服用的是_________;
(3)蘋果汁是人們喜愛的飲品,由于其中含有Fe2+,現(xiàn)榨的蘋果汁在空氣中會由淺綠色變?yōu)樽攸S色,若榨汁時加入維生素C,可有效防止這種現(xiàn)象發(fā)生.這說明維生素C具有________(填序號);①氧化性 ②還原性 ③堿性 ④酸性
(4)食用植物油進入人體后,在酶的作用下水解為高級脂肪酸和_________(寫名稱),進而被氧化成二氧化碳和水并提供能量,或作為合成人體所需其他物質的原料;
(5)硫酸亞鐵可用于治療缺鐵性貧血,某貧血患者每天須補充1.4g鐵元素,則服用的藥物中含硫酸亞鐵的質量至少為_________g;
(6)氨基酸是組成蛋白質的基本結構單元,其分子中一定含有的官能團是氨基(﹣NH2)和____(寫結構簡式或名稱).人體中共有二十多種氨基酸,其中人體自身________(填“能”或“不能”)合成的氨基酸稱為人體必需氨基酸;
(7)淀粉在淀粉酶的作用下最終水解為葡萄糖(C6H12O6),部分葡萄糖在體內被氧化生成二氧化碳和水.寫出葡萄糖在體內被氧化的化學方程式:________。
【答案】① ② ③ ② ④ ② 甘油 3.8 ﹣COOH 不能 C6H12O6+6O2![]() 6CO2+6H2O
6CO2+6H2O
【解析】
(1)食品的酸堿性與其本身的pH值無關(味道是酸的食品不一定是酸性食品),主要是食品經過消化、吸收、代謝后,最后在人體內變成酸性或堿性的物質來界定;
(2)根據(jù)藥物的成分及與酸的反應來分析;青霉素屬于消炎常用藥物,使用前需要做皮膚敏感性測試;麻黃堿的成分含有能使人興奮的作用來分析;
(3)根據(jù)蘋果汁在空氣中會由淡綠色變?yōu)樽攸S色,可知鐵元素的化合價升高被氧化,而加入維生素C,能使鐵元素的化合價降低,并利用氧化還原反應來分析;
(4)食物油是高級脂肪酸甘油酯;
(5)先計算硫酸亞鐵的含鐵質量分數(shù),然后利用鐵的質量除以鐵的質量分數(shù)即可求出硫酸亞鐵的質量;
(6)氨基酸一定含有的官能團是氨基(-NH2)和羧基(-COOH);必需氨基酸指的是人體自身不能合成或合成速度不能滿足人體需要,必須從食物中攝取的氨基酸;
(7)根據(jù)反應物和生成物及其質量守恒定律可以正確的書寫化學方程式。
(1)含鉀、鈉、鈣、鎂等礦物質較多的食物,在體內的最終的代謝產物常呈堿性,產生堿性物質的稱為堿性食品,蔬菜、水果、乳類、大豆和菌類食物等;
含氮、碳、硫、氯、等元素較多的食物,經過消化形成酸根留在體內,產生酸性物質的稱為酸性食品,如淀粉類;動物性食物;甜食;油炸食物或奶油類;豆類(如花生等),故答案為:①;②;
(2)因胃酸的成分為鹽酸,治療胃酸過多則選擇胃舒平,因氫氧化鋁與酸反應可減少鹽酸;青霉素是應用廣泛的抗菌藥物,它本身毒性很小,而較常見的卻是藥物的過敏,引起不良的反應以致死亡,則使用前要進行皮膚敏感性測試;因麻黃堿是一種生物堿,能對人的中樞神經系統(tǒng)起興奮作用,則國際奧委會嚴禁運動員服用,故答案為:③;②;④;
(3)在空氣中,氧氣能夠把+2價鐵氧化成+3價;而加入維生素C則能防止這種氧化,說明維生素C具有還原性,與三價鐵發(fā)生氧化還原反應,故答案為:②;
(4)食物油是高級脂肪酸甘油酯,在酸性條件下水解生成高級脂肪酸和甘油,故答案為:甘油;
(5)硫酸亞鐵中鐵的質量分數(shù)是:![]() =
=![]() ,需硫酸亞鐵的質量是
,需硫酸亞鐵的質量是![]() =3.8g
=3.8g
故答案為:3.8;
(6)氨基酸一定含有的官能團是氨基(-NH2)和羧基(-COOH);必需氨基酸指的是人體自身不能合成或合成速度不能滿足人體需要,必須從食物中攝取的氨基酸,
故答案為:-COOH;不能;
(7)葡萄糖在體內發(fā)生緩慢氧化生成二氧化碳和水,反應的化學方程式為:C6H12O6+6O2![]() 6CO2+6H2O。
6CO2+6H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】工業(yè)廢催化劑中含有多種金屬元素,某廢催化劑主要含有SiO2、ZnO、ZnS和CuS,為充分利用資源,變廢為寶,在實驗室中探究回收廢催化劑中的鋅和銅,具體流程如圖所示,回答下列問題:
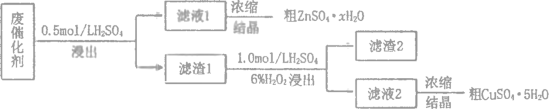
已知:ZnS與稀硫酸反應且化合價不變;CuS既不溶于稀硫酸也不與稀硫酸反應。
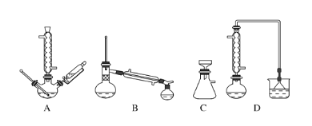
(1)下列玻璃儀器或裝置中,第一次浸出時尾氣凈化需要使用的裝置為___________(填標號),“濃縮結晶”需要使用的儀器是_______________(填名稱)。
(2)濾渣1的主要成分是 ___________。
(3)第二次浸出時,向盛有濾渣1的反應器中先加入稀硫酸,后滴入過氧化氫溶液。反應器中有淡黃色沉淀生成,寫出反應的離子方程式___________;若順序相反,會造成___________。
(4)第二次浸出時需要加熱且控溫,采用的合適加熱方式是___________。
(5)某同學在實驗完成之后,得到23.3g提純的硫酸鋅晶體(ZnSO4·xH2O)。為確定晶體化學式,取5.0g晶體,用蒸餾水完全溶解.再加入足量的氯化鋇溶液,充分反應后過濾、___________、___________、稱重得固體4.1g,則硫酸鋅晶體的化學式為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是( )
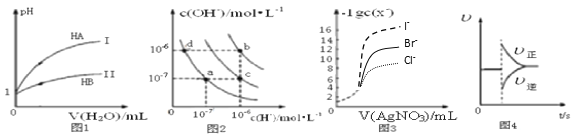
A. 圖1表示常溫下,稀釋HA、HB兩種酸的稀溶液時,溶液pH隨加水量的變化,則等物質的量濃度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B. 圖2中在b點對應溫度下,將pH=2的H2SO4溶液與pH=12的NaOH溶液等體積混合后,溶液顯中性
C. 用0.0100 mol/L硝酸銀標準溶液,滴定濃度均為0.1000 mol/L Cl-、Br-及I-的混合溶液,由圖3曲線,可確定首先沉淀的是Cl-
D. 圖4表示在N2(g)+3H2(g) ![]() 2NH3(g)達到平衡后,減小NH3濃度時速率的變化
2NH3(g)達到平衡后,減小NH3濃度時速率的變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】無色的混合氣體甲中可能含有NO、CO2、NO2、NH3、N2中的幾種,將100mL氣體甲經過如圖所示實驗處理,結果得到酸性溶液,而幾乎無氣體剩余,則氣體甲的組成可能為( )
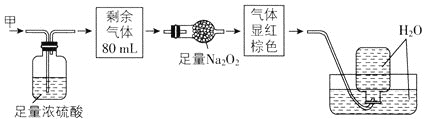
A.NO2、NH3、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】藥物阿比朵爾具有很好的抗病毒活性,其合成路線如下:
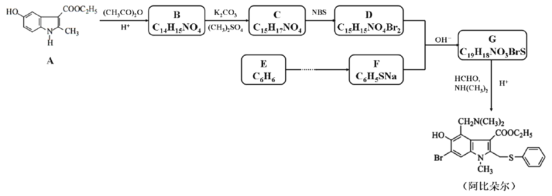
已知:①![]() +HCHO+
+HCHO+
![]()

②RX![]() RLiX
RLiX![]() RSH
RSH
請回答:
(1)下列說法正確的是___________。
A.化合物A能發(fā)生加成、取代和氧化反應,不發(fā)生還原反應
B.化合物B具有弱堿性
C.化合物D與FeCl3溶液發(fā)生顯色反應
D.阿比朵爾的分子式是C22H25N2O3BrS
(2)寫出化合物D的結構簡式___________。
(3)寫出G→阿比朵爾的化學方程式___________。
(4)設計從E→F的合成路線(用流程圖表示,無機試劑任選)___________。
(5)寫出化合物A同時符合下列條件的同分異構體的結構簡式___________。
①1H-NMR譜和IR譜檢測表明:分子中共有4種氫原子,含氮氧單鍵和碳氧雙鍵;
②含有苯環(huán)和含氮五元雜環(huán),且兩環(huán)共棱連接。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是熱量高、無污染的燃料,天然氣儲量豐富是理想的制氫原料,研究甲烷制氫具有重要的理論和現(xiàn)實意義。
(1)甲烷水蒸氣重整制氫:CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H1=+216kJmol-1,溫度1200k,壓強0.2Mpa,水碳起始物質的量之比3:1,達到平衡時氫氣的物質的量分數(shù)為0.3,甲烷轉化率為____,Kp=____(Mpa)2 。理論上近似水碳比為____,氫氣的物質的量分數(shù)將達到最大。
CO(g)+3H2(g)△H1=+216kJmol-1,溫度1200k,壓強0.2Mpa,水碳起始物質的量之比3:1,達到平衡時氫氣的物質的量分數(shù)為0.3,甲烷轉化率為____,Kp=____(Mpa)2 。理論上近似水碳比為____,氫氣的物質的量分數(shù)將達到最大。
(2)①將甲烷水蒸氣重整和甲烷氧化重整兩種方法結合,理論上按照空氣、甲烷、水蒸氣約15:7:1體積比進料(空氣中氧氣體積分數(shù)約為0.2),可以實現(xiàn)反應器中能量自給(不需要補充熱量)。
甲烷氧化重整制氫:2CH4(g)+O2(g)=2CO(g)+4H2(g) △H2=____kJmol-1
②實際生產中,空氣、甲烷、水蒸氣按照約1:1:2體積比進料,增加水蒸氣的作用是____,還能發(fā)生____(用化學方程式表示)反應,從而獲得更多的氫氣。
(3)甲烷水蒸氣重整過程中,溫度1000K,原料氣以57.6Kgh-1通入容積為1L鎳基催化反應器中,2-5s甲烷質量分數(shù)由7.32%變?yōu)?/span>5.32%,用甲烷表示2-5s的反應速率為____molmin-1 ,隨著反應的進行反應速率會急速下降,可能的原因是甲烷等高溫不穩(wěn)定,造成____。有人提出將甲烷水蒸氣重整和甲烷氧化重整兩種方法結合則能解決這個問題,原因是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:CH3—CH=CH2+HBr→CH3—CHBr—CH3(主要產物),1 mol某烴A充分燃燒后可以得到8 mol CO2和4 mol H2O。該烴A在不同條件下能發(fā)生如下面所示的一系列變化。
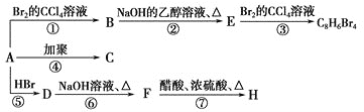
(1)A的化學式:________,A的結構簡式________。
(2)上述反應中,①是________反應,⑦是________反應。(填反應類型)
(3)寫出C,D,E,H物質的結構簡式:
C_________,D_________,E_______,H________。
(4)寫出DF反應的化學方程式_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉬酸鈉晶體(Na2MoO42H2O)是白色菱形結晶體,毒性較低,對環(huán)境污染污染程度低,可作新型水處理劑和金屬腐蝕抑制劑。工業(yè)上利用鉬精礦(主要成分是不溶于水的 MoS2)制備鉬酸鈉的兩種途徑如圖所示。
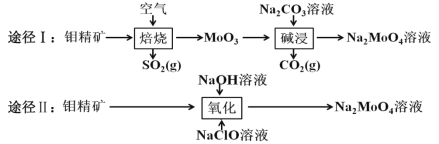
(1)途徑Ⅰ焙燒過程中,為了提高焙燒效率,除增大空氣量外還可以采用的措施有___; 在該過程的主要反應中,氧化劑與還原劑物質的量之比為________。
(2)途徑Ⅱ氧化時還有 Na2SO4 生成,則反應的離子方程式為 ____________。
(3)已知途徑Ⅰ的鉬酸鈉溶液中 c(MoO42-)=0.40 molL-1,c(CO32-)=0.10 molL-1。由鉬酸鈉溶液制備鉬酸鈉晶體時,需加入 Ba(OH)2 固體以除去 CO32-。在不損失 MoO42-的情況下,CO32-的最大去除率是 ____________ [已知 Ksp(BaCO3)=1×10-9、Ksp(BaMoO4)=4.0×10-8,忽略溶液的體積變化]。
(4)途徑Ⅱ中 Na2MoO4 溶液通過結晶的方法可得到 Na2MoO4 晶體。母液可以循環(huán)利用,但循環(huán)一定次數(shù)后必須對母液進行處理,試解釋原因 _________。
(5)途徑Ⅱ比途徑Ⅰ的優(yōu)點有 ________________(答出兩條)。
(6)鉬酸鈉和月桂酰肌氨酸的混合液常作為碳素鋼的緩蝕劑。常溫下,碳素鋼在三種不同介質中的腐蝕速率實驗結果如圖。
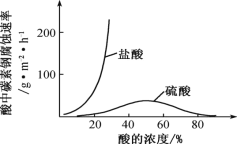
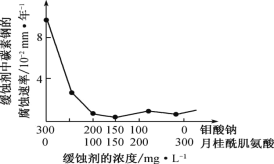
①當硫酸的濃度大于 90%時,碳素鋼腐蝕速率幾乎為零,原因是________________。
②若緩釋劑鉬酸鈉-月桂酸肌氨酸總濃度為 300 mgL-1,則緩蝕效果最好時鉬酸鈉(M=206 gmol-1)的物質的量濃度為 ________(計算結果保留 3 位有效數(shù)字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某種二次鋰離子電池工作時反應為:LixCn + Li(1-x)CoO2 == LiCoO2 + nC。電池如圖所示。下列說法不正確的是
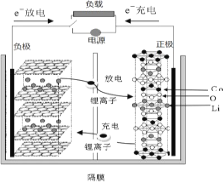
A.放電時,碳材料極失去電子,發(fā)生氧化反應,電子經外電路,Li+經內電路同時移向正極
B.放電時正極反應為: Li(1-x)CoO2 + xLi+ + xe- = LiCoO2
C.充電時, Li+從負極脫出,又嵌入正極
D.鋰離子二次電池正負極之間充放電時發(fā)生傳輸 Li+的反應,少有副反應
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com