
【題目】化合物J是一種常用的抗組胺藥物,一種合成路線如下:

已知:①C為最簡單的芳香烴,且A、C互為同系物。
②2ROH+NH3![]() HNR2+2H2O(R代表烴基)。
HNR2+2H2O(R代表烴基)。
請回答下列問題:
(1)A的化學名稱是______________,H中的官能團名稱是________________________。
(2)由D生成E的反應類型是__________,G的結構簡式為________________________。
(3)B+C→D的化學方程式為______________。
(4)L是F的同分異構體,含有聯苯結構,遇FeCl3溶液顯紫色,則L有__________________(不考慮立體異構)種。其中核磁共振氫譜為六組峰,峰面積之比為3∶2∶2∶2∶2∶1的結構簡式為______。
(5)寫出用氯乙烷和2-氯-1-丙醇為原料制備化合物![]() 的合成路線(其他無機試劑任選) __。
的合成路線(其他無機試劑任選) __。
【答案】甲苯 醚鍵、氯原子 氧化反應 CH2OHCH2Cl ![]() +
+![]() CH2Cl
CH2Cl![]()
![]() +HCl 19
+HCl 19 ![]()
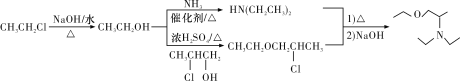
【解析】
(1)由A→B的反應條件以及B的組成可推知A為甲苯;由H的結構簡式可知,H中的官能團為醚鍵和氯原子;
(2)反應D→E屬于去氫加氧的反應,所以其反應類型為氧化反應;由F+G→H的反應條件(濃硫酸、加熱)以及產物中醚鍵的生成可知,該反應屬于羥基間的脫水成醚,故G的結構簡式為CH2OHCH2Cl;
(3)B為一氯甲苯,C為苯,結合D的結構簡式可得B+C→D的化學方程式為![]() +
+![]() CH2Cl
CH2Cl![]()
![]() +HCl;
+HCl;
(4)根據F的分子組成以及L遇FeCl3溶液顯紫色,說明分子中有一個酚羥基和一個甲基,相當于用一個酚羥基和一個甲基分別取代聯苯中的兩個氫原子,可以用定一移一的方法分析。先用一個酚羥基取代聯苯中一個氫的位置,可得三種結構,分別為![]() 、
、![]() 、
、![]() ,這三種結構中苯環上氫的種數分別為7種、7種、5種,說明甲基的取代位置有19種,即L可能的結構有19種。其中核磁共振氫譜為六組峰,峰面積之比為3∶2∶2∶2∶2∶1的分子結構應該對稱,結構簡式為
,這三種結構中苯環上氫的種數分別為7種、7種、5種,說明甲基的取代位置有19種,即L可能的結構有19種。其中核磁共振氫譜為六組峰,峰面積之比為3∶2∶2∶2∶2∶1的分子結構應該對稱,結構簡式為![]() ;
;
(5)先觀察目標產物的結構特點,發現目標產物與合成路線中J物質所含官能團相同,所以應結合題干中F→H→J的合成路線找出所需的反應物為HN(CH2CH3)2、乙醇和2-氯-1-丙醇,其中2-氯-1-丙醇為原料,乙醇可以由氯乙烷水解得到,HN(CH2CH3)2可由乙醇和氨反應得到(已知條件②),再按F→H→J的過程合成目標產物,合成路線為 。
。


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】已知25℃時部分弱電解質的電離平衡常數數據如表所示,回答下列問題:
化學式 | CH3COOH | H2CO3 | HClO |
電離平衡常數 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
(1)物質的量濃度均為0.1molL﹣1的四種溶液:pH由小到大排列的順序是___________(用編號填寫)
a.CH3COONab.Na2CO3 c.NaClOd.NaHCO3
(2)常溫下,0.1molL﹣1 CH3COOH溶液加水稀釋過程中,下列表達式的數據變大的是_________(填字母)
A.c(H+) B.![]() C.c(H+)c(OH﹣)
C.c(H+)c(OH﹣)
D.![]() E.
E.![]()
(3)寫出向次氯酸鈉溶液中通入少量二氧化碳的離子方程式:___________
(4)25℃時,CH3COOH與CH3COONa的混合溶液,若測得混合液pH=6,則溶液中c(CH3COO﹣)﹣c(Na+)=________(填準確數值).
(5)25℃時,將a molL﹣1的醋酸與b molL﹣1氫氧化鈉等體積混合,反應后溶液恰好顯中性,用a、b表示醋酸的電離平衡常數為_________________
(6)標準狀況下,將1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的濃度符號完成下列等式: c(OH﹣)=2c(H2CO3)+______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】

(1)圖I是實驗室制取蒸餾水的常用裝置,圖中明顯的錯誤是_________________。
(2)儀器A的名稱是_____________,儀器B的名稱是______________。
(3)實驗時A中除加入少量自來水外,還需加入少量__________,其作用是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黃血鹽[亞鐵氰化鉀,K4Fe(CN)6·3H2O]可用作食鹽添加劑,一種制備黃血鹽的工藝如下所示:

下列說法錯誤的是
A. HCN溶液有劇毒,含CN-的廢水必須處理后才能排放
B. “廢水”中含量較多的溶質為CaCl2
C. “試劑 X”可能是K2CO3
D. “系列操作”為蒸發結晶、過濾、洗滌、干燥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】疊氮化鈉(NaN3)是一種白色劇毒晶體,是汽車安全氣囊的主要成分。NaN3易溶于水,微溶于乙醇,水溶液呈弱堿性,能與酸發生反應產生具有爆炸性的有毒氣體疊氮化氫。實驗室可利用亞硝酸叔丁酯(t-BuNO2,以t-Bu表示叔丁基)與N2H4、氫氧化鈉溶液混合反應制備疊氮化鈉。
(1)制備亞硝酸叔丁酯
取一定NaNO2溶液與50%硫酸混合,發生反應H2SO4+2NaNO2===2HNO2+Na2SO4。可利用亞硝酸與叔丁醇(t-BuOH)在40 ℃左右制備亞硝酸叔丁酯,試寫出該反應的化學方程式:________________。
(2)制備疊氮化鈉(NaN3)
按如圖所示組裝儀器(加熱裝置略)進行反應,反應方程式為:t-BuNO2+NaOH+N2H4===NaN3+2H2O+t-BuOH。

①裝置a的名稱是________________;
②該反應需控制溫度在65 ℃,采用的實驗措施是____________________;
③反應后溶液在0 ℃下冷卻至有大量晶體析出后過濾,所得晶體使用無水乙醇洗滌。試解釋低溫下過濾和使用無水乙醇洗滌晶體的原因是______________________________________________。
(3)產率計算
①稱取2.0 g疊氮化鈉試樣,配成100 mL溶液,并量取10.00 mL溶液于錐形瓶中。
②用滴定管加入0.10 mol·L-1六硝酸鈰銨[(NH4)2Ce(NO3)6]溶液40.00 mL[發生的反應為2(NH4)2Ce(NO3)6+2NaN3===4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](假設雜質均不參與反應)。
③充分反應后將溶液稀釋并酸化,滴入2滴鄰菲羅啉指示液,并用0.10 mol·L-1硫酸亞鐵銨[(NH4)2Fe(SO4)2]為標準液,滴定過量的Ce4+,終點時消耗標準溶液20.00 mL(滴定原理:Ce4++Fe2+===Ce3++Fe3+)。計算可知疊氮化鈉的質量分數為__________(保留2位有效數字)。若其他操作及讀數均正確,滴定到終點后,下列操作會導致所測定樣品中疊氮化鈉質量分數偏大的是______(填字母代號)。
A.錐形瓶使用疊氮化鈉溶液潤洗
B.滴加六硝酸鈰銨溶液時,滴加前仰視讀數,滴加后俯視讀數
C.滴加硫酸亞鐵銨標準溶液時,開始時尖嘴處無氣泡,結束時出現氣泡
D.滴定過程中,將掛在錐形瓶壁上的硫酸亞鐵銨標準液滴用蒸餾水沖進瓶內
(4)疊氮化鈉有毒,可以使用次氯酸鈉溶液對含有疊氮化鈉的溶液進行銷毀,反應后溶液堿性明顯增強,且產生無色無味的無毒氣體,試寫出反應的離子方程式:____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是兩種氣態烴組成的混合氣體完全燃燒所得的CO2和H2O的物質的量(單位:mol)的變化關系。下列判斷不正確的是:
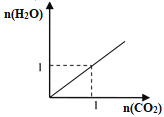
A. 一定含有甲烷
B. 可能含有乙烷
C. 可能含有乙炔
D. 若120℃不變,反應前后氣體體積不一定發生變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】游離態氮稱為惰性氮,游離態氮轉化為化合態氮稱之為氮的活化,在氮的循環系統中,氮的過量“活化”,則活化氮開始向大氣和水體過量遷移,氮的循環平衡被打破,導致全球環境問題。
Ⅰ. 氮的活化
工業合成氨是氮的活化重要途徑之一,在一定條件下,將N2 和 H2 通入到體積為0.5L的恒容容器中,反應過程中各物質的物質的量變化如圖所示:

(1)10min內用NH3表示該反應的平均速率,v(NH3)=____________。
(2)在第10min和第25min改變的條件可能分別是_________、________(填字母)。
A.加了催化劑 B. 升高溫度 C. 增加NH3的物質的量
D.壓縮體積 E.分離出氨氣
(3)下列說法能說明該可逆反應達到平衡狀態的是__________(填字母)。
A. 容器中氣體密度不變 B. 容器中壓強不變
C. 3v(H2)正=2v(NH3)逆 D. N2、H2、NH3分子數之比為1∶3∶2
Ⅱ.催化轉化為惰性氮 已知:SO2、CO、NH3等都可以催化還原氮氧化物生成惰性氮。
(4)在250C、101KPa時,N2(g)+3H2(g) ![]() 2NH3(g) △H1= -92.4kJ/mol.
2NH3(g) △H1= -92.4kJ/mol.
2H2(g)+O2(g)=2H2O(l) △H2= -571.6 kJ/mol
N2(g)+O2(g)=2NO(g) △H3= +180kJ/mol
則NO與NH3反應生成惰性氮的熱化學方程式______________________________。
(5)在有氧條件下,新型催化劑M能催化CO與NOx反應生成N2。現向某密閉容器中充入等物質的量濃度的NO2和CO氣體,維持恒溫恒容,在催化劑作用下發生反應:
4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) △H<0,相關數據如下:
N2(g)+4CO2(g) △H<0,相關數據如下:
0min | 5min | 10min | 15min | 20min | |
c(NO2) /mol·L-1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2) /mol·L-1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①計算此溫度下的化學平衡常數K=______,
②實驗室模擬電解法吸收NOx裝置如圖,(圖中電極均為石墨電極)。若用NO2氣體進行模擬電解法吸收實驗(a<b),電解時NO2發生反應的電極反應式:_________________________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼及硼的化合物有著廣泛的用途。請回答下列問題:
(1)硼在元素周期表中的位置為_________,電子排布式是________,硼元素有兩種天然同位素10B和11B,硼元素的近似相對原子質量為10.8,則兩種同位素原子的原子個數之比為_______。
(2)單質硼(B)在一定條件下與NaOH溶液反應生成NaBO2和一種氣體,請寫出該反應的化學方程式________________。
(3)與B一個周期的元素Be和C,它們的電離能由小到達的順序 _______________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com