
【題目】實驗室需要0.1mol/L的NaOH溶液450ml。根據這種溶液的配制情況回答下列問題:
(1)在如圖所示儀器中,配制上述溶液肯定不需要的是___(填序號),除圖中已有儀器外,配制上述溶液還需要到的玻璃儀器是___。
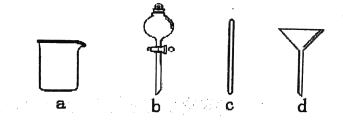
(2)配制時,其正確的操作順序是(用字母表示,每個操作只用一次)___。
A.用少量水洗滌燒杯2次~3次,洗滌液均注入容量瓶,振蕩
B.在盛有NaOH固體的燒杯中加入適量水稀釋
C.將燒杯中已冷卻的溶液沿玻璃棒注入容量瓶中
D.將容量瓶蓋緊,反復上下顛倒,搖勻
E.改用膠頭滴管加水,使溶液凹面恰好與刻度相切
F.繼續往容量瓶內小心加水,直到液面接近刻度1~2cm處
(3)實驗兩次用到玻璃棒,其作用分別是:先用于___、后用于___。
(4)關于容量瓶的四種敘述:①是配制準確濃度溶液的儀器;②不宜貯存溶液;③不能用來加熱;④使用之前要檢查是否漏水。這些敘述中正確的是___
A.①②③④ B.②③ C.①②④ D.②③④
(5)根據計算用托盤天平稱取的質量為___g。
II.若配制1mol/L的稀硫酸溶液500mL。
(6)根據計算得知,所需質量分數為98%、密度為1.84g/cm3的濃硫酸的體積為:___mL(計算結果保留一位小數)。如果實驗室有15mL、20mL、50mL量筒,應選用__mL的量筒最好。
(7)下列操作所造成硫酸濃度偏高的是___。
A.溶解后溶液沒有冷卻到室溫就轉移
B.轉移時沒有洗滌燒杯、玻璃棒
C.向容量瓶加水定容時眼睛俯視刻度線
D.用量筒量取濃硫酸后洗滌量筒并把洗滌液轉移到容量瓶中
E.搖勻后發現液面低于刻度線,又加蒸餾水至刻度線
【答案】bd 500ml容量瓶 膠頭滴管 BCAFED 攪拌 引流 A 2.0 27.2 50 ACD
【解析】
(1)根據配制一定物質的量濃度溶液用到儀器進行解答;
(2)依據配制一定物質的量濃度溶液一般步驟排序;
(3)溶解過程中用玻璃棒不斷攪拌加速固體溶解,移液時用玻璃棒引流;
(4)依據容量瓶構造及使用方法解答;
(5)依據m=CVM計算需要溶質的質量;
(6)依據c=![]() 計算濃硫酸的物質的濃度,依據溶液稀釋過程溶質的物質的量不變計算需要濃硫酸體積;依據濃硫酸體積選擇合適規格量筒;
計算濃硫酸的物質的濃度,依據溶液稀釋過程溶質的物質的量不變計算需要濃硫酸體積;依據濃硫酸體積選擇合適規格量筒;
(7)分析操作對溶質的物質的量和溶液體積的影響,依據c=![]() 進行誤差分析。
進行誤差分析。
(1)實驗室需要0.1mol.L的NaOH溶液450ml,應選擇500mL的容量瓶,已知配制一定物質的量濃度的溶液的步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶,可知用到的儀器:天平、燒杯、玻璃棒、500mL的容量瓶、膠頭滴管,則用不到下圖所示儀器中的分液漏斗和三角漏斗,即bd,還缺少的玻璃儀器是500mL的容量瓶、膠頭滴管;
(2)根據配制步驟計算、稱量(量取)、溶解、冷卻、移液、洗滌、定容、搖勻,所以正確的操作順序為BCAFED;
(3)溶解過程中用玻璃棒不斷攪拌加速固體溶解,移液時用玻璃棒引流;
(4)容量瓶是配制準確的一定物質的量濃度的溶液用的精確儀器.它是一種帶有磨口玻璃塞的細長頸、梨形的瓶底玻璃瓶,頸上有刻度;使用時要先檢驗密閉性,不能在容量瓶里進行溶質的溶解,容量瓶不能進行加熱,容量瓶只能用于配制溶液,不能長時間或長期儲存溶液;故答案為A;
(5)配制0.1molL-1NaOH溶液500mL,需要溶質的質量為:0.1mol/L×0.5L×40g/mol=2.0g;
II. (6)質量分數為98%、密度為1.84g/cm3的濃硫酸,物質的量濃度c=![]() mol/L=18.4mol/L,設需要濃硫酸體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:18.4mol/L×V=1mol/L×500mL,解得V=27.2mL;應選擇50mL量筒;
mol/L=18.4mol/L,設需要濃硫酸體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:18.4mol/L×V=1mol/L×500mL,解得V=27.2mL;應選擇50mL量筒;
(7)A.溶解后溶液沒有冷卻到室溫就轉移,冷卻后,溶液體積偏小,溶液濃度偏高,故A正確;
B.轉移時沒有洗滌燒杯、玻璃棒,導致部分溶質損耗溶質的物質的量偏小,溶液濃度偏低,故B錯誤;
C.向容量瓶加水定容時眼睛俯視液面,導致溶液體積偏低,溶液濃度偏高,故C正確;
D.用量筒量取濃硫酸后洗滌量筒并把洗滌液轉移到容量瓶,導致量取的濃硫酸體積偏大,溶質的物質的量偏大,溶液濃度偏高,故D正確;
E.搖勻后發現液面低于刻度線,又加蒸餾水至刻度線,導致溶液體積偏大,溶液濃度偏低,故E錯誤;
故答案為ACD。


 優質課堂快樂成長系列答案
優質課堂快樂成長系列答案科目:高中化學 來源: 題型:
【題目】下列實驗所用試劑、現象和結論均正確的是
選項 | 實驗裝置 | 現象 | 結論 |
A |
| 裝置Ⅲ中有淺黃色沉淀 | 苯和濃溴水發生取代反應 |
B |
| 高錳酸鉀溶液褪色,溴的四氯化碳溶液褪色 | 石蠟油的分解產物中含有不飽和烴 |
C |
| 盛有飽和碳酸鈉溶液的試管中,上方出現油狀液體 | 制備乙酸乙酯 |
D |
| 甲醚有氣泡 | 鑒別乙醇與甲醚(CH3OCH3) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知可逆反應:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反應物起始物質的量相同,下列關于該反應的示意圖不正確的是( )
4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反應物起始物質的量相同,下列關于該反應的示意圖不正確的是( )
A. 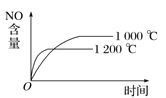 B.
B. 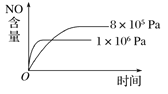
C. 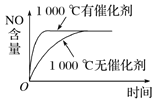 D.
D. 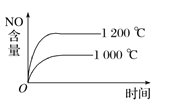
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在反應11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,已知Cu3P中P為-3價,則15molCuSO4可氧化的P的物質的量為
A. 1.5mol B. 5.5mol C. 3mol D. 2.5mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子在指定的溶液中能大量共存的是
A. 常溫下,水電離的c(OH-)=1×10-12mo1·L-1的溶液中:NH4+、Fe2+、SO42-、NO3-
B. 常溫下,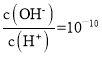 的溶液中:K+、Na+、I-、SO42-
的溶液中:K+、Na+、I-、SO42-
C. 能使酚酞變紅的溶液中:Na+、Ba2+、HSO3-、Cl-
D. 0.1 mol·L1 KI溶液:Na+、K+、ClO、OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔為主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡膠,如圖所示是有關合成路線圖.
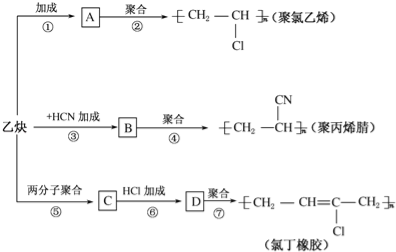
已知反應:nCH2═CH﹣CH═CH2![]()
![]()
請完成下列各題:
(1)寫出物質的結構簡式:A ,C .
(2)寫出反應的化學方程式
反應②: ;
反應③: ;
反應⑥: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分別用濃度均為0.5 mol/L的NH3·H2O和NaOH溶液,滴定20 mL 0.01 mol/L Al2(SO4)3溶液,隨滴定溶液體積的增大,溶液的導電能力變化曲線如圖所示,下列說法中正確的是
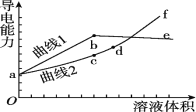
A. 曲線2 代表滴加NH3·H2O溶液的變化曲線
B. b和d點對應的溶液均顯堿性
C. b點溶液中c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D. d~f段導電能力升高的原因是發生了反應Al(OH)3+OH-===2H2O+AlO2-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,0.1 mol/L某一元酸(HA)溶液中c(H+)=1×10-3 mol/L,下列敘述正確的是( )
A. 該溶液中由水電離出的c(H+)=1×10-11 mol/L
B. 該一元酸溶液的pH=1
C. 該溶液中水電離的c(H+)=1×10-3 mol/L
D. 用pH=11的NaOH溶液V1 L和V2 L 0.1 mol/L該一元酸(HA)溶液混合,若恰好反應,則V1=V2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是利用陰離子交換膜和過濾膜制備高純度的Cu的裝置示意圖,下列有關敘述不正確的是
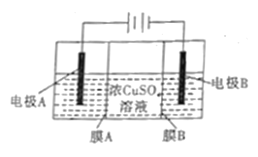
A. 電極A是粗銅,電極B是純銅
B. 電路中通過1mol電子,生成32g銅
C. 溶液中SO42-向電極A遷移
D. 膜B是過濾膜,阻止陽極泥及雜質進入陰極區
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com