
【題目】醇的官能團名稱是______,結構簡式為______;羧酸的官能團名稱是______,結構簡式為_______。二者在一定條件下發生反應的類型是______,寫出乙酸和乙醇反應的化學方程式___________________________________。
科目:高中化學 來源: 題型:
【題目】已知反應mX(g)+nY(g)![]() qZ(g)的△H<0,m+n>q,在恒容密閉容器中反應達到平衡時,下列說法正確的是
qZ(g)的△H<0,m+n>q,在恒容密閉容器中反應達到平衡時,下列說法正確的是
A. X的正反應速率是Y的逆反應速率的m/n倍
B. 通入稀有氣體使壓強增大,平衡將正向移動
C. 降低溫度,混合氣體的平均相對分子質量變小
D. 增加X的物質的量,Y的轉化率降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸亞鐵銨[(NH4)2Fe(SO4)2·6H2O較硫酸亞鐵不易被氧氣氧化,是分析化學中重要的試劑,常用于代替硫酸亞鐵。硫酸亞鐵銨在500℃時隔絕空氣加熱完全分解,回答下列問題:
(1)硫酸亞鐵銨隔絕空氣加熱完全分解發生了氧化還原反應,固體產物可能有FeO和Fe2O3,氣體產物可能有NH3、SO3、H2O、N2和_________。
(2)為檢驗分解產物的成分,設計如下實驗裝置進行實驗,加熱A中的硫酸亞鐵銨至分解完全。
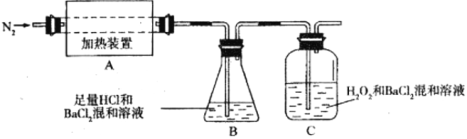
①為驗證A中殘留物是否含有FeO,需要選用的試劑有_________。
A.KSCN溶液 B.稀硫酸 C.濃鹽酸 D.KMnO4溶液
②裝置B中BaCl2溶液的作用是為了檢驗分解產物中是否有_________氣體生成,若含有該氣體,觀察到的現象為___________________。
③若A中分解產物有N2,固體殘留物只有Fe2O3,Fe2O3的物質的量為bmol,C中沉淀物質的量為amol,則b_________a(填“大于”、“小于”或“等于”)
④實驗中,觀察到C中有白色沉淀生成,則C中發生反應的離子方程式為________________。
(3)為測定某固體樣品中(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的含量,某實驗小組做了如下實驗:MnO4-+Fe2++H+=Mn2++Fe3++H2O(方程式未配平)
測定步驟:
步驟一:準確稱量20.00g硫酸亞鐵銨晶體,配制成100mL溶液。
步驟二:取所配溶液25.00mL于錐形瓶中,加稀H2SO4酸化,用0.1000mol·L-1KMnO4溶液滴定至終點,重復兩次,平均消耗KMnO4溶液16.00mL。
①步驟二達到滴定終點的標志為________________________;
②產品中(NH4)2Fe(SO4)2·6H2O的質量分數為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上制備純硅反應的熱化學方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) △H=+QkJ·mol-1(Q>0),某溫度、壓強下,將一定量的反應物通入密閉容器中進行以上的反應(此條件下為可逆反應),下列敘述正確的是
Si(s)+4HCl(g) △H=+QkJ·mol-1(Q>0),某溫度、壓強下,將一定量的反應物通入密閉容器中進行以上的反應(此條件下為可逆反應),下列敘述正確的是
A. 反應過程中,若增大壓強能提高SiCl4的轉化率
B. 若反應開始時SiCl4為1mol,則達到平衡時,吸收熱量為QkJ
C. 反應至4min時,若HCl的濃度為0.12mol·L-1,則H2的反應速率為0.03mol/(L·min
D. 當反應吸熱為0.025QkJ時,生成的HCl與100mL1mol·L-1的NaOH溶液恰好反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積固定的密閉容器中充入一定量的X、Y兩種氣體,一定條件下發生反應并達到平衡:3X(g) + Y(g)![]() 2Z(g) △H<0。若測得平衡時X的轉化率為37.5 %,Y的轉化率是X的2/3,則下列敘述正確的是
2Z(g) △H<0。若測得平衡時X的轉化率為37.5 %,Y的轉化率是X的2/3,則下列敘述正確的是
A. 若以X表示的反應速率為0.2 mol/(L·s),則以Z表示的反應速率為0.3 mol/(L·s)
B. 充入氦氣增大容器內的壓強,Y的轉化率提高
C. 升高溫度,平衡向正反應方向移動
D. 起始時刻n(X) : n(Y)= 2 : 1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學用下列裝置制備并檢驗Cl2的性質,相關說法正確的是
A. 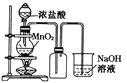 如果MnO2過量,濃鹽酸就可全部被消耗
如果MnO2過量,濃鹽酸就可全部被消耗
B. 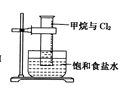 量筒中發生了取代反應
量筒中發生了取代反應
C. 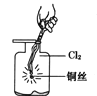 生成藍色的煙
生成藍色的煙
D. 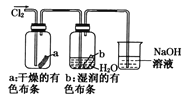 濕潤的有色布條褪色說明了Cl2具有漂白性
濕潤的有色布條褪色說明了Cl2具有漂白性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子一定能大量共存的是( )
A.H+、Fe2+、SO42-、NO3-B.Fe3+、NH4+、Cl-、SCN-
C.NH4+、Al3+、OH-、SO42-D.Na+、K+、NO3-、CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中,反應X2(g)+Y2(g)2XY(g)△H>0,達到甲平衡.在僅改變某一條件后,達到乙平衡,對此過程的分析正確的是
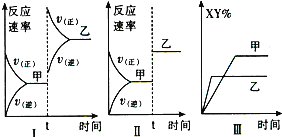
A. 圖I是升高溫度的變化情況
B. 圖Ⅱ是擴大容器體積的變化情況
C. 圖Ⅲ是增大壓強的變化情況
D. 圖Ⅲ是升高溫度的變化情況
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com