
| A. | 飽和Na2CO3溶液中BaSO4沉淀轉化為BaCO3沉淀 | |
| B. | 升高溫度,化學平衡發生移動是因為平衡常數改變 | |
| C. | 持續加熱,水中MgCO3逐漸轉化為更難溶的Mg(OH)2 | |
| D. | 改變一個影響因素使化學平衡發生移動,則平衡常數K值一定變化 |
分析 A.如滿足c(Ba2+)c(CO32-)>Ksp(BaCO3),可生成沉淀;
B.升高溫度,平衡常數變化,則平衡狀態發生改變;
C.升高溫度,促進鎂離子的水解;
D.平衡發生移動,平衡常數不一定變化.
解答 解:A.如滿足c(Ba2+)c(CO32-)>Ksp(BaCO3),則硫酸鋇可轉化生成碳酸鋇沉淀,故A正確;
B.升高溫度,平衡常數變化,則平衡狀態發生改變,正逆反應速率不等,則平衡發生移動,故B正確;
C.升高溫度,促進鎂離子的水解,可使碳酸鎂轉化生成氫氧化鎂沉淀,故C正確;
D.平衡發生移動,如溫度不變,則平衡常數不變化,故D錯誤.
故選D.
點評 本題考查化學平衡的影響因素,為高頻考點,側重于學生的分析能力的考查,注意把握化學平衡的影響因素,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ①②④ | C. | ②④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過氧化鈉用作呼吸面具中的供氧劑,每生成0.1molO2,轉移電子的數目為0.4NA | |
| B. | 將1mL1mol/LFeCl3溶液逐滴加入沸水,制得紅褐色Fe(OH)3膠體,所含膠粒的數目是1×10-3NA | |
| C. | 標準狀況下,0.1molCl2溶于水,轉移電子的數目為0.1NA | |
| D. | 7.8gNa2S和Na2O2的混合物中,含有的陰離子數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:200 | B. | 200:1 | C. | 100:1 | D. | 1:100 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該同學的葡萄糖的濃度偏高 | |
| B. | 該同學的葡萄糖的濃度比總膽紅素的濃度高 | |
| C. | 該同學的總膽紅素的濃度比葡萄糖的濃度高 | |
| D. | 該同學的總膽紅素的濃度出現異常 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
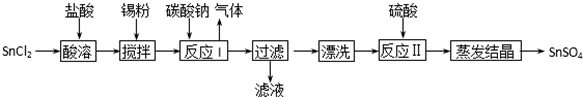
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 硫酸是工業生產中重要的產品之一,在很多領域都有重要用途.回答下列問題:
硫酸是工業生產中重要的產品之一,在很多領域都有重要用途.回答下列問題:| 壓強 SO2轉化率 溫度 | 1.0×105Pa | 5.0×105Pa | 1.0×106Pa | 1.5×106Pa |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9989 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8528 | 0.8897 | 0.9276 | 0.9468 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 實驗目的 | 實驗操作 | 現象 | 結論 |
| 自來水中離子檢驗 | 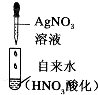 | 出現不溶于稀HNO3的沉淀 | 自來水中含氯離子 |
| 水的提純 | 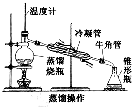 | 蒸餾燒瓶中水沸騰,冷凝管中有無色液體凝結,并通過冷凝管流入錐形瓶中 | 錐形瓶中收集到無色液體 |
| 蒸餾水中雜質離子的檢驗 | 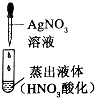 | 無明顯現象 | 蒸餾水中不含氯離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應是放熱反應,降低溫度將縮短反應達到平衡的時間 | |
| B. | 其他條件不變,使用高效催化劑,廢氣中氮氧化物的轉化率增大 | |
| C. | 單位時間內消耗NO和N2的物質的量比為6:5時,反應達到平衡 | |
| D. | 平衡時,其他條件不變,升高溫度可使該反應的平衡常數增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com