
【題目】常溫下,將Cl2緩慢通入水中至飽和,然后再滴加0.1 mol·L-1的NaOH溶液,整個過程中溶液的pH變化曲線如圖所示。下列選項正確的是( )
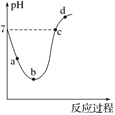
A. a點所示的溶液中c(H+)=c(Cl-)+c(HClO)+c(OH-)
B. b點所示的溶液中c(H+)>c(Cl-)>c(HClO)>c(ClO-)
C. c點所示的溶液中c(Na+)=c(HClO)+c(ClO-)
D. d點所示的溶液中c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
【答案】B
【解析】A.a點溶液呈酸性,根據電荷守恒得c(H+)=c(Cl-)+c(Cl0-)+c(OH-),故A錯誤;B.b點溶液酸性最強,根據電荷守恒得c(H+)=c(Cl-)+c(Cl0-)+c(OH-),所以c(H+)>c(Cl-),酸性越強,次氯酸的電離程度越小,所以c(HClO)>c(ClO-),所以離子濃度大小順序是c(H+)>c(Cl-)>c(HClO)>c(ClO-),故B正確;C.c點溶液呈中性,則c(H+)=c(OH-),根據電荷守恒得c(H+)+c(Na+)=c(Cl-)+c(Cl0-)+c(OH-),所以c(Na+)=c(Cl-)+c(ClO-),根據物料守恒得c(Cl-)=c(ClO-)+c(HClO),所以c(Na+)=c(HClO)+2c(ClO-),故C錯誤;D.d點溶液呈堿性,則c(H+)<c(OH-),根據電荷守恒得c(H+)+c(Na+)=c(Cl-)+c(Cl0-)+c(OH-),所以c(Na+)>c(Cl-)+c(Cl0-),根據物料守恒得c(Cl-)=c(ClO-)+c(HClO),所以c(Cl-)>c(ClO-),故D錯誤;故選B。


 寶貝計劃期末沖刺奪100分系列答案
寶貝計劃期末沖刺奪100分系列答案 能考試全能100分系列答案
能考試全能100分系列答案科目:高中化學 來源: 題型:
【題目】如圖是A、B、C三種固體物質的溶解度曲線。下列說法正確的是( )
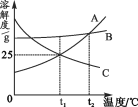
A. t1℃時,A的飽和溶液中溶質質量分數為25%
B. t2℃時,A、B、C三種物質的溶解度大小關系為A=B>C
C. 將t1℃時A、C的飽和溶液升溫到t2℃時,A、C兩溶液都會變成不飽和溶液
D. B中含有少量A,要提純B可采用冷卻熱飽和溶液、趁熱過濾的方法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、目前世界上60%的鎂是從海水中提取的。海水提鎂的主要流程如下:
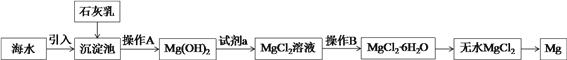
操作A是____________,下列儀器中操作B必須使用的有__________(填字母符號)。
A、錐形瓶 B、玻璃棒 C、表面皿 D、蒸發皿 E、坩堝
Ⅱ、乙醇鎂[(CH3CH2O)2Mg] 為白色固體,難溶于乙醚和烴類,略溶于乙醇,在空氣中會水解,常用作烯烴聚合催化劑載體和制備精密陶瓷的原料。某小組同學用鎂粉(受潮會發生自燃、自爆)與乙醇在實驗室中制備乙醇鎂:
(1)干燥管中盛裝的試劑為_____________,其作用為__________________________。
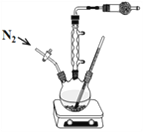
(2)下列操作的合理順序為:______________。
a、將干燥的氮氣通入裝置,連續操作數次;
b、稱取鎂粉,量取無水乙醇加入反應器內;
c、加熱回流,控制溫度在80℃,反應1小時;
d、開啟冷凝水和磁力攪拌器。
(3)將溫度控制在80℃的原因是________________,寫出生成乙醇鎂的化學方程式____________________________。
(4)請你設計實驗證明有乙醇鎂生成(簡述實驗的方法):_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是應用最廣泛的金屬,鐵的氧化物、鹵化物以及硫酸鹽均為重要化合物。
(1)氧化鐵為紅棕色粉末,該物質難溶于水,易溶于鹽酸中,請寫出該物質與鹽酸反應的離子方程式______________________________。
(2)鐵在氯氣中劇烈燃燒,產生紅棕色的煙,將燃燒所得的三氯化鐵溶于水,所得溶液的質量分數為16.25%,其密度為6.0g· mL-1,則該溶液中氯離子的物質的量濃度為________________;將上述所配制的溶液稀釋為0.15mol/L 的稀溶液480mL,需要的儀器除燒杯、玻璃棒、量筒、膠頭滴管之外,還需要________________;量取該溶液的體積是_______________mL;在配制過程中如果定容時俯視刻度線,會造成所配溶液濃度________(填“偏高”、“偏低”或“無影響”)。
(3)將飽和FeCl3溶液滴入沸騰的蒸餾水中,可以制得Fe(OH)3膠體,請寫出該過程的化學反應方程式_______________________,以下關丁Fe(OH)3膠體的說法中不正確的有_____________(填序號。
A. Fe(OH)3膠體是一種紅褐色、澄清、透明的混合物
B. Fe(OH)3膠體中分散質的微粒直徑在10-9m~10-7m 之間
C.用滲析法鑒別Fe(OH)3膠體和FeCl3 溶液,用丁達爾效應分離Fe(OH)3膠體和FeCl3 溶液
D.取少量Fe(OH)3膠體置于試管中,向試管中逐滴滴加稀硫酸,可看到先產生紅褐色沉淀,隨后沉淀溶解,最終得到黃色的溶液
E.將其裝入U 形管內,用石墨作電極,接通直流電,通電一段時間后發現靠近正極區附近的顏色逐漸變深
(4)在硫酸鐵溶液中,逐滴加入等濃度的氫氧化鋇溶液,其溶液的導電性隨氫氧化鋇溶液體積增加而變化的圖象是(_______)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列裝置能達到實驗目的的是
A. 碳酸氫鈉溶液直接蒸干得到碳酸氫鈉固體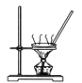
B. 制備Fe(OH)2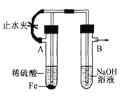
C. 除去CO2中含有的少量HCl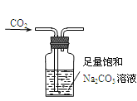
D. 配制100mL 0.1mol/L的稀硫酸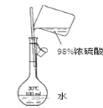
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近期發現,H2S是繼NO、CO之后第三個生命體系氣體信號分子,它具有參與調節神經信號傳遞、舒張血管減輕高血壓的功能。回答下列問題:
(1)下圖是通過熱化學循環在較低溫度下由水或硫化氫分解制備氫氣的反應系統原理。

通過計算,可知系統(Ⅰ)和系統(Ⅱ)制氫的熱化學方程式分別為________________、______________,制得等量H2所需能量較少的是_____________(填“系統(Ⅰ)”或“系統(Ⅱ)”)。
(2)羰基硫(COS)可作為一種糧食熏蒸劑,能防止某些昆蟲、線蟲和真菌的危害。H2S與CO2在高溫下發生反應:H2S(g)+CO2(g)![]() COS(g) +H2O(g)。在610 k時,將1 mol CO2與1 mol H2S充入2 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
COS(g) +H2O(g)。在610 k時,將1 mol CO2與1 mol H2S充入2 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
①H2S的平衡轉化率![]() =_______%,反應平衡常數K=________。
=_______%,反應平衡常數K=________。
②在620 K重復試驗,平衡后水的物質的量分數為0.03,H2S的轉化率![]() _____
_____![]() ,該反應的
,該反應的![]() H_____0。(填“>”“<”或“=”)
H_____0。(填“>”“<”或“=”)
③向反應器中再分別充入下列氣體,能使H2S轉化率增大的是________(填標號)
A.N2 B.H2S C.COS D.CO2
(3)25℃,在0.10mol·L-1H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-) 關系如右圖(忽略溶液體積的變化、H2S的揮發)。

①pH=13時,溶液中的c( H2S ) + c( HS- )=_____mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,當溶液pH=______時,Mn2+開始沉淀。[已知:Ksp(MnS)=2.8×10-13 ]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米TiO2在涂料、光催化、化妝品等領域有著極其廣泛的應用。
制備納米TiO2的方法之一是TiCl4水解生成TiO2xH2O,經過濾、水洗除去其中的Cl-,再烘干、焙燒除去水分得到粉體TiO2。
用氧化還原滴定法測定TiO2的質量分數:一定條件下,將TiO2溶解并還原為Ti3+,再以KSCN溶液作指示劑,用NH4Fe(SO4)2標準溶液滴定Ti3+至全部生成Ti4+。
請回答下列問題:
(1)TiCl4水解生成TiO2xH2O的化學方程式為______________________________。
(2)檢驗TiO2xH2O中Cl-是否被除凈的方法是______________________________。
(3)配制NH4Fe(SO4)2標準溶液時,加入一定量H2SO4的原因是__________;使用的儀器除天平、藥匙、玻璃棒、燒杯、量筒外,還需要下圖中的__________(填字母代號)。
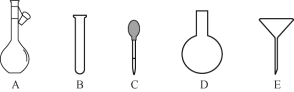
(4)滴定終點的判定現象是________________________________________。
(5)滴定分析時,稱取TiO2(摩爾質量為Mg/mol)試樣wg,消耗cmol/LNH4Fe(SO4)2 標準溶液VmL,則TiO2質量分數表達式為______________________________。
(6)判斷下列操作對TiO2質量分數測定結果的影響(填“偏高”“偏低”或“無影響”)。
①若在配制標準溶液過程中,燒杯中的NH4Fe(SO4)2溶液有少量濺出,使測定結果__________。
②若在滴定終點讀取滴定管刻度時,俯視標準液液面,使測定結果__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1994年度諾貝爾化學獎授予為研究臭氧做出貢獻的化學家。臭氧能吸收有害紫外線,保護人類賴以生存的空間。O3分子的結構如圖:呈V形,兩個O—O鍵的夾角為116.5°。三個原子以一個O原子為中心,與另外兩個O原子分別構成非極性共價鍵;中間O原子提供2個電子,旁邊兩個O原子各提供1個電子,構成一個特殊的化學鍵(虛線內部)——三個O原子均等地享有這4個電子。請回答:
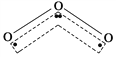
(1)題中非極性共價鍵是________鍵,特殊的化學鍵是________鍵。
(2)臭氧與氧氣的關系是____________________。
(3)下列分子中與O3分子的結構最相似的是(____)
A.H2O B.CO2 C.SO2 D.BeCl2
(4)分子中某原子有一對或幾對沒有跟其他原子共用的價電子叫孤對電子,那么O3分子有______對孤對電子。
(5)O3具有強氧化性,它能把PbS氧化為PbSO4而O2不能,試配平:___PbS+___O3===___PbSO4+____O2,生成1 mol O2,轉移電子的物質的量為______mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下列裝置進行相關實驗,操作正確且能達到實驗目的的是
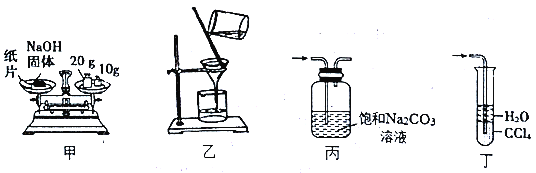
A. 甲裝置:稱30.0gNaOH固體 B. 乙裝置:過濾除去溶液中的不溶性雜質
C. 丙裝置:除去CO2中混有的HCl氣體 D. 丁裝置:吸收實驗室制NH3的尾氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com