
分析 (1)根據“Cu+2AgNO3═2Ag+Cu(NO3)2”知,該反應中Cu元素化合價由0價變為+2價、Ag元素化合價由+1價變為0價,則Cu失電子發生氧化反應、銀離子得電子發生還原反應,所以Cu作負極、不如Cu活潑的金屬或導電的非金屬作正極,硝酸銀為電解質;
(2)正極上銀離子得電子發生還原反應、負極上Cu失電子發生氧化反應;
(3)放電時,電解質溶液中陰離子向負極移動,陽離子向正極移動,電子從負極沿導線流向正極.
解答 解:(1)根據“Cu+2AgNO3═2Ag+Cu(NO3)2”知,在原電池中失電子的金屬作負極,所以Cu作負極;不如Cu活潑的金屬或導電的非金屬作正極,如Ag等,硝酸銀為電解質,
故答案為:Ag等;Cu;AgNO3;
(2)正極上銀離子得電子發生還原反應、負極上Cu失電子發生氧化反應,正負極電極反應式分別為Ag++e-=Ag、Cu-2e-=Cu2+,
故答案為:Ag++e-=Ag;Cu-2e-=Cu2+;
(3)放電時,電解質溶液中陰離子向負極移動,陽離子向正極移動,負極上失電子、正極上得電子,所以電子從負極沿導線流向正極,
故答案為:正;負;正.
點評 本題考查原電池設計,為高頻考點,明確正負極與反應類型的關系是解本題關鍵,難點是電解質溶液的確定,注意放電時電解質溶液中陰陽離子移動方向,為易錯點.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
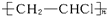 .
.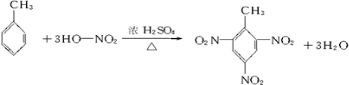 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙酸與碳酸鈉溶液反應:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O | |
| B. | 醋酸溶液與新制氫氧化銅反應:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚鈉溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO | |
| D. | 甲醛溶液與足量的銀氨溶液共熱HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ①②③④ | C. | ③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
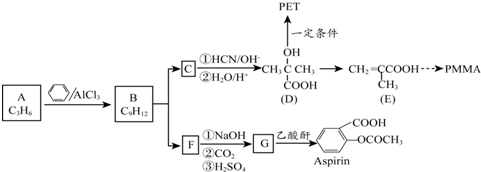
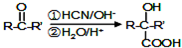
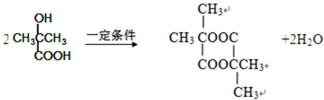 .1mol Aspirin分子與足量的NaOH反應的化學方程式是
.1mol Aspirin分子與足量的NaOH反應的化學方程式是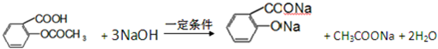 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯水、二氧化硫、活性炭的漂白或脫色原理雖然不同,但它們都能使品紅或墨跡褪色 | |
| B. | 等物質的量的Cl2和SO2同時與潮濕的紅布條作用,紅布條立即褪色 | |
| C. | 反應CuSO4+H2S=CuS↓+H2SO4能進行,說明硫化銅既不溶于水,也不溶于稀硫酸 | |
| D. | 經Cl2和SO2漂白的物質,日后都會恢復原來的顏色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com