
【題目】以甲烷為原料合成部分化工產品流程如圖(部分反應條件已略去) ,已知 A 和甲是來自石油和煤的兩種基本化工原料。A 是氣態烴,甲是液態烴。A 是常見的植物生長調節劑,75% 的B 溶液可用于殺死“新冠”病毒,D 是高分子化合物。
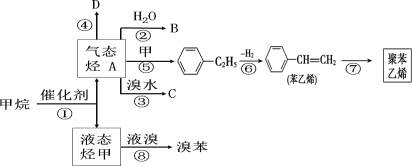
(1)A 的結構簡式為_______,B 中官能團名稱為_____,C 的名稱為_____。
(2)在反應②、③、⑥、⑧中,屬于加成反應的是_____,屬于取代反應的是_____。(填序號)
(3)寫出下列反應的化學方程式并注明反應條件。
反應②:_____;
反應⑦:_____;
反應⑧:_____。
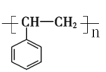
【答案】CH2=CH2 羥基 1,2-二溴乙烷 ②③ ⑧ CH2=CH2+H2O![]() CH3CH2OH n
CH3CH2OH n![]()
![]()
![]() +Br2
+Br2![]()
![]() +HBr
+HBr
【解析】
根據題干信息,A和甲是來自石油和煤的兩種基本化工原料,A是氣態烴,甲是液態烴,A是常見的植物生長調節劑,則A為乙烯(CH2=CH2),由轉化關系,液態烴甲與液溴生成溴苯,則烴甲為苯,氣態烴A與H2O可發生加成反應生成B,75%的B溶液可用于殺死“新冠”病毒,則B為CH3CH2OH,D是高分子化合物,則D為聚乙烯,乙烯與溴水發生加成反應生成BrCH2CH2Br,A與甲發生反應生成![]() ,
,![]() 發生消去反應得到苯乙烯,苯乙烯發生加聚反應生成聚苯乙烯,據此分析解答。
發生消去反應得到苯乙烯,苯乙烯發生加聚反應生成聚苯乙烯,據此分析解答。
(1)根據上述分析可知,A為乙烯,其結構簡式為CH2=CH2,B為CH3CH2OH,含有的官能團為羥基,C為BrCH2CH2Br,名稱為1,2-二溴乙烷,故答案為:CH2=CH2;羥基;1,2-二溴乙烷;
(2)反應②為CH2=CH2與H2O可發生加成反應生成CH3CH2OH,反應③為乙烯與溴水發生加成反應生成BrCH2CH2Br,反應⑥為![]() 發生消去反應得到苯乙烯,反應⑦為苯與液溴發生取代反應生成溴苯,因此屬于加成反應的是②③,屬于取代反應的為⑧,故答案為:②③;⑧;
發生消去反應得到苯乙烯,反應⑦為苯與液溴發生取代反應生成溴苯,因此屬于加成反應的是②③,屬于取代反應的為⑧,故答案為:②③;⑧;
(3)反應②CH2=CH2與H2O可發生加成反應生成CH3CH2OH,反應方程式為CH2=CH2+H2O![]() CH3CH2OH,反應⑦為苯乙烯發生加聚反應生成聚苯乙烯,反應方程式為n
CH3CH2OH,反應⑦為苯乙烯發生加聚反應生成聚苯乙烯,反應方程式為n![]()
![]()
 ,反應⑧為苯與液溴發生取代反應生成溴苯,反應方程式為
,反應⑧為苯與液溴發生取代反應生成溴苯,反應方程式為![]() +Br2
+Br2![]()
![]() +HBr,故答案為:CH2=CH2+H2O
+HBr,故答案為:CH2=CH2+H2O![]() CH3CH2OH;n
CH3CH2OH;n![]()
![]()
 ;
;![]() +Br2
+Br2![]()
![]() +HBr。
+HBr。


 小學能力測試卷系列答案
小學能力測試卷系列答案科目:高中化學 來源: 題型:
【題目】短周期主族元素及其化合物在生產生活中至關重要。
(1)BF3與一定量水形成(H2O)2·BF3晶體Q,Q在一定條件下可轉化為R:

晶體Q中含有的化學鍵包括____________________。
(2) NF3與NH3的空間構型相同,但NF3不易與Cu2+等形成配位鍵,其原因是___________。
(3)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148 ℃液化,形成一種能導電的熔體,測得其中含有陰陽離子各一種,結構是正四面體型離子和正八面體型離子;正八面體型離子的化學式為_________________________;正四面體型離子中鍵角大于PCl3的鍵角原因為______________________________________________________。
(4)氯化鈉的晶胞結構如圖所示,圖是氯化鈉的晶胞截面圖(圖中球大小代表半徑大小)。已知NA代表阿伏加德羅常數的值,氯化鈉晶體的密度為d g·cm-3。則Na+半徑為____________pm(只需列出計算式)。
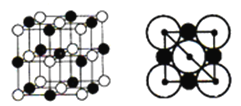
(5)砷化硼為立方晶系晶體,該晶胞中原子的分數坐標為:
B: (0,0,0); (![]() ,
,![]() ,0);(
,0);(![]() ,0,
,0,![]() );(0,
);(0,![]() ,
,![]() );……
);……
As:(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );……
);……
①請在圖中畫出砷化硼晶胞的俯視圖______。
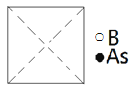
②砷原子緊鄰的硼原子有________個,與每個硼原子緊鄰的硼原子有______個。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】全世界每年因鋼鐵銹蝕造成了巨大的損失,下列有關說法不正確的是
A.鋼鐵腐蝕時化學能不能全部轉化為電能
B.鋼鐵腐蝕的負極反應式為Fe-2e-=Fe2+
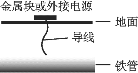
C.如圖所示,將導線與金屬鋅相連可保護地下鐵管
D.如圖所示,將導線與外接電源的正極相連可保護地下鐵管
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物K是治療急、慢性支氣管炎及支氣管擴張、肺氣腫、肺結核等疾病藥物的中間體,其合成路線如下,回答下列問題:
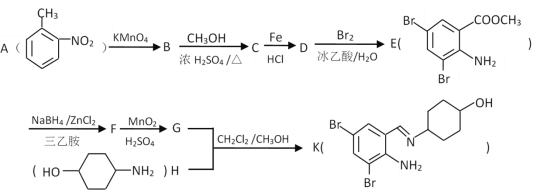
已知信息:
① 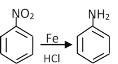
②![]()
③R1CHO+R2NH2 →R1CH=NR2
(1)B→C的反應類型為____________, H中官能團的名稱為__________________。
(2)G的結構簡式為______________,F→G的反應類型為_______________。
(3)D→E的反應方程式為___________________________________________。
(4)寫出化合物D同時符合下列條件的同分異構體的結構簡式_____________。
①苯環上有兩個取代基,官能團與D相同,苯環上的一氯代物有兩種
②核磁共振氫譜顯示峰面積比為2:2:2:3
(5)已知:通常在同一個碳原子上連有兩個羥基不穩定,易脫水形成羰基。寫出以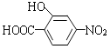 和
和![]() 為原料制備
為原料制備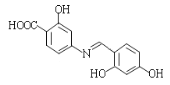 的合成路線______________________(其他試劑任選)。
的合成路線______________________(其他試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某“84消毒液”瓶體部分標簽如圖所示,該“84消毒液”通常稀釋100倍(體積之比)后使用。請回答下列問題:

(1)該“84消毒液”的物質的量濃度約為________mol·L-1。(保留小數點后一位)
(2)某同學取100 mL該“84消毒液”,稀釋后用于消毒,稀釋后的溶液中c(Na+)=________mol·L-1。
(3)該同學參閱該“84消毒液”的配方,欲用NaClO固體配制480 mL含NaClO質量分數為25%的消毒液。下列說法正確的是________(填字母)。
A、容量瓶用蒸餾水洗凈后,應烘干后才能用于溶液配制
B、配制過程中,未用蒸餾水洗滌燒杯和玻璃棒可能導致結果偏低
C、需要稱量NaClO固體的質量為143.0 g
(4)“84消毒液”與稀硫酸混合使用可增強消毒能力,某消毒小組人員用98%(密度為1.84 g·cm-3)的濃硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增強“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物質的量濃度為________mol·L-1。
②需用濃硫酸的體積為________mL。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗內容能達到實驗目的的是
實驗目的 | 實驗內容 | |
A | 鑒別乙醇與乙醛 |
|
B | 比較乙酸、碳酸、苯酚的酸性 |
|
C | 說明烴基對羥基上氫原子活性的影響 | |
D | 說明苯環對取代基上氫原子活性的影響 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】同溫同壓下,某容器充滿N2重114g,若充滿CO2重122g,現充滿某氣體重108g,則某氣體的相對分子質量為
A.28B.32C.44D.16
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ由白色和黑色固體組成的混合物A,可以發生如下框圖所示的一系列變化:
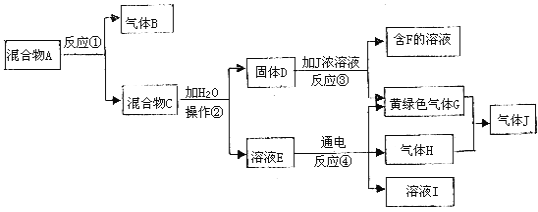
(1)寫出反應③的化學方程式:_____________________________________________。寫出反應④的離子方程式:_____________________________________________。
(2)在操作②中所使用的玻璃儀器的名稱是:____________________________。
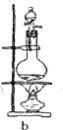
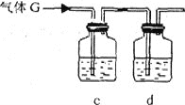
(3)下列實驗裝置中可用于實驗室制取氣體G的發生裝置是______;(用字母表示)為了得到純凈干燥的氣體G,可將氣體通過c和d裝置,c裝置中存放的試劑_____,d裝置中存放的試劑______。

(4)氣體G有毒,為了防止污染環境,必須將尾氣進行處理,請寫出實驗室利用燒堿溶液吸收氣體G的離子方程式:____________________________。
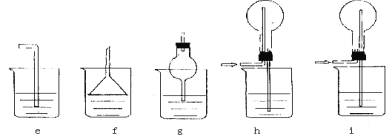
(5)J是一種極易溶于水的氣體,為了防止倒吸,下列e~i裝置中,可用于吸收J的是____________。
Ⅱ.某研究性學習小組利用下列裝置制備漂白粉,并進行漂白粉有效成分的質量分數的測定。

(1)裝置③中發生反應的化學方程式為________________________________________
(2)測定漂白粉有效成分的質量分數:稱取1.000 g漂白粉于錐形瓶中,加水溶解,調節溶液的pH,以淀粉為指示劑,用0.100 0 mol·L-1KI溶液進行滴定,溶液出現穩定淺藍色時為滴定終點。
反應原理為3ClO-+I-===3Cl-+IO3- IO3-+5I-+3H2O===6OH-+3I2
實驗測得數據如下表所示。該漂白粉中有效成分的質量分數為________________。
滴定次數 | 1 | 2 | 3 |
KI溶液體積/mL | 19.98 | 20.02 | 20.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com