
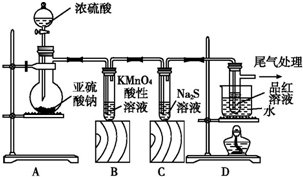
分析 (1)根據化學常用儀器及儀器的名稱來分析;制備二氧化硫的方法是利用亞硫酸鈉和濃硫酸反應生成;
(2)利用二氧化硫與高錳酸鉀溶液,二氧化硫與硫化鈉的氧化還原反應來分析反應現象和性質,依據離子性質和電荷守恒,原子守恒配平書寫離子方程式;
(3)根據二氧化硫能使品紅褪色,但加熱褪色后的溶液又可恢復紅色來解答;
(4)利用二氧化硫的性質來分析尾氣處理,利用發生的化學反應來書寫吸收尾氣的離子反應;
(5)二氧化硫是還原性的酸性氧化物,過氧化鈉具有氧化性來分析解答.
解答 解:(1)裝置A中盛放亞硫酸鈉的儀器名稱是蒸餾燒瓶,其中發生反應的化學方程式為:Na2SO3+H2SO4(濃)=Na2SO4+SO2↑+H2O,
故答案為:蒸餾燒瓶;Na2SO3+H2SO4(濃)=Na2SO4+SO2↑+H2O;
(2)高錳酸鉀溶液為紫紅色,具有氧化性,二氧化硫具有還原性,二者發生氧化還原反應,則觀察到紅色逐漸變淺直至完全褪去,二氧化硫進入硫化鈉溶液中發生的氧化還原反應為2S2-+SO2+2H2O=3S↓+4OH-,則觀察到出現黃色渾濁,B中S元素的化合價升高,表現還原性,C中二氧化硫中硫元素的化合價降低,表現氧化性,高錳酸鉀溶液和二氧化硫氣體發生的離子反應為:2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+,
故答案為:溶液由紫紅色變為無色;還原性;2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+;氧化性;
(3)因二氧化硫能使品紅褪色,但加熱褪色后的溶液又可恢復紅色,則操作為待品紅溶液完全褪色后,關閉分液漏斗的旋塞,點燃酒精燈加熱,觀察到的現象為無色溶液恢復為紅色,故答案為:待品紅溶液完全褪色后,關閉分液漏斗的旋塞,點燃酒精燈加熱;無色溶液恢復為紅色;
(4)利用氫氧化鈉溶液來吸收尾氣,發生的離子反應為SO2+2OH-=SO32-+H2O,故答案為:NaOH;
(5)理由二氧化硫與二氧化碳類似,都為酸性氧化物,可能的反應2Na2O2+2SO2=2Na2SO3+O2;過氧化鈉具有氧化性,亞硫酸鈉還可被氧化為硫酸鈉,可能的反應Na2O2+SO2=Na2SO4,故答案為:2Na2O2+2SO2=2Na2SO3+O2;二氧化硫與二氧化碳類似,都為酸性氧化物.
點評 本題為實驗習題,考查二氧化硫的制取及二氧化硫的性質實驗,明確反應原理、二氧化硫的性質是解答本題的關鍵,難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
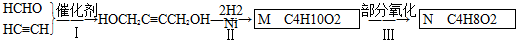
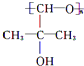

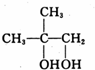 ,B中的官能團名稱是醛基和醇羥基.
,B中的官能團名稱是醛基和醇羥基.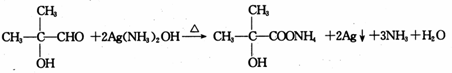 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④⑤⑥ | B. | ①②③④⑤ | C. | ①②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 預期現象與結論 |
| 步驟1: | 部分固體不溶解 |
| 步驟2: | |
| 步驟3:繼續步驟2中的(2),進行固液分離,用蒸餾水洗滌固體至洗滌液無色.取少量固體于試管中,滴加過量HCl后,靜置,取上層清液,滴加適量H2O2,充分振蕩后滴加KSCN. |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | B | |
| C | D |
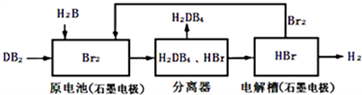
| 化學鍵 | H-H | Br-Br | H-Br |
| 鍵能(kJ/mol) | 436 | 194 | 362 |
| 化學式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
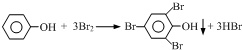
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com