
| A. | 熱穩定性:PH3>H2S>HBr>NH3 | |
| B. | 物質的熔點:石英>食鹽>冰>汞 | |
| C. | 結合質子的能力:CO32->CH3COO->SO42- | |
| D. | 分散系中分散質粒子的直徑:Fe(OH)3懸濁液>Fe(OH)3膠體>FeCl3溶液 |
分析 A.非金屬性越強,氣態氫化物越穩定;
B.熔點一般為原子晶體>離子晶體>金屬晶體>分子晶體;
C.越不容易電離成質子的物質,說明結合質子能力越強;
D.根據分散系中分散質粒子的直徑大小來分析.
解答 解:A.因非金屬性N>Br>S>P,則穩定性NH3>HBr>H2S>PH3,故A錯誤;
B.熔點一般為原子晶體>離子晶體>金屬晶體>分子晶體,但汞常溫下為液體,熔點比冰的低,所以物質的熔點為石英(原子晶體)>食鹽(離子晶體)>冰>汞,故B正確;
C.當結合氫離子后,CO32-、CH3COO-、SO42-分別生成的物質是碳酸、醋酸、硫酸,硫酸是強電解質極容易電離,醋酸是弱電解質較容易電離,碳酸是弱電解質比較難電離,所以這三種離子結合質子的能力大小為CO32->CH3COO->SO42-,故C正確;
D.濁液中分散質的直徑大于100nm,溶液中分散質的直徑小于1nm,膠體中分散質的直徑在1nm~100nm之間,則分散系中分散質粒子的直徑:Fe(OH)3懸濁液>Fe(OH)3膠體>FeCl3溶液,故D正確;
故選A.
點評 本題考查知識點較多,綜合性較強,注重對考試常考考點的考查,學生應注意歸納規律性知識來解答,題目難度較大.


科目:高中化學 來源: 題型:選擇題
| A. | 含大量OH-的溶液中:CO32-、Cl-、F-、K+ | |
| B. | 甲基橙呈黃色的溶液中;I-、Cl-、NO3-、Na+ | |
| C. | 石蕊呈藍色的溶液中:Na+、AlO2-、NO3-、HCO3- | |
| D. | 含大量Al3+的溶液中:K+、Na+、NO3-、ClO- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 茶葉中含咖啡堿,能溶于水、乙醇,更易溶于氯仿(CHCl3),178℃時快速升華.另外茶葉中還含有11%~12%的丹寧酸,也易升華,易溶于水及乙醇,但不溶于氯仿.現從茶葉中提取咖啡堿流程如下:
茶葉中含咖啡堿,能溶于水、乙醇,更易溶于氯仿(CHCl3),178℃時快速升華.另外茶葉中還含有11%~12%的丹寧酸,也易升華,易溶于水及乙醇,但不溶于氯仿.現從茶葉中提取咖啡堿流程如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水小 | |
| B. | H2A溶液在不同pH環境中各微粒的分布不同,電離平衡常數也不同 | |
| C. | 溶液的pH=4.5時,存在如下關系:C(Na+)>C(HA-)>C(A2-)>C(H+)>C(OH-) | |
| D. | 已知HClO的電離平衡常數為10-7.5將少量H2A 的溶液加入足量NaClO溶液中,發生的反應為:H2A+ClO-═HClO+HA- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C的物質的量濃度 | B. | 混合氣體的密度 | ||
| C. | 容器內壓強 | D. | 混合氣體的平均分子量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 滴加甲基橙試劑呈紅色的溶液:Fe2+、NH4+、Cl-、NO3- | |
| B. | pH為11的溶液:S2-、SO32-、S2O32-、Na+ | |
| C. | 水電離出來的c (OH-)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| D. | 無色透明的溶液:K+、SiO32-、NO3-、Al3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
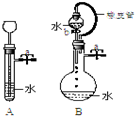 根據如圖描述回答下列問題:
根據如圖描述回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com