

分析 (1)依據氯氣不具有漂白性及次氯酸具有漂白性,氯氣與碘化鉀反應生成碘,碘易溶于四氯化碳,分層的液體采用分液的方法分離;
(2)根據針頭的作用判斷壓強的大小,氣體的壓強有利于分液漏斗內的液體順利流下;
(3)二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣和水.
解答 解:(1)Cl2與干紅布條不反應(乙中),沒有次氯酸生成,所以有色布條不褪色;Cl2與H2O反應生成的HClO起漂白作用,所以丙中紅色布條褪色;Cl2與KI溶液反應生成I2單質,CCl4萃取碘單質,溶液分層,采用分液的方法分離;
故答案為:無明顯變化;紅布條褪色;用分液漏斗分液;
(2)利用針頭的橡皮管連接后,分液漏斗與燒瓶內氣壓相等,有利于液體流下,
故答案為:等于;保證分液漏斗液面上、下兩邊壓強相等,便于分液漏斗中液體順利流下;
(3)二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣和水,化學方程式為:4HCl(濃)+Mn02 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+C12↑+2H20;
故答案為:4HCl(濃)+Mn02 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+C12↑+2H20.
點評 本題考查了氯氣的制取、性質及次氯酸的探究性實驗的設計,明確氯氣和次氯酸的性質是解題關鍵,注意分離物質方法選擇的原則,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
 Ⅰ.短周期元素X、Y、Z、W在元素周期表中相對位置如圖所示,其中Y所處的周期序數與族序數相等.按要求回答下列問題:
Ⅰ.短周期元素X、Y、Z、W在元素周期表中相對位置如圖所示,其中Y所處的周期序數與族序數相等.按要求回答下列問題: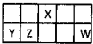
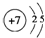 .
.| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業制金屬鈉:電解飽和食鹽水 | |
| B. | 工業制溴:某些植物有富集溴的能力,從海產品中提取溴是工業上獲取溴的重要途徑 | |
| C. | 冶煉鋁:電解Al2O3,同時加入冰晶石(Na3AlF6),目的是為了降低Al2O3熔融溫度 | |
| D. | 硫酸工業:在氧氣充足的情況下,從接觸室進入吸收塔的氣體中不可能含有SO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
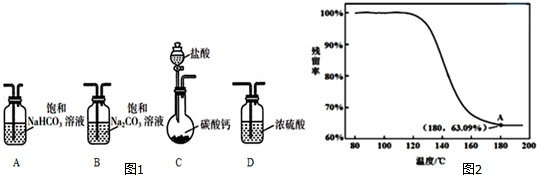
NaHCO3溶液 BaCl2濃度 | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | 渾濁 | 渾濁 | 少許渾濁 |
| 0.1mol•L-1 | 渾濁 | 少許渾濁 | 無現象 |
| 0.02mol•L-1 | 少許渾濁 | 無現象 | 無現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 6.72L CO | B. | 6.6g CO2 | C. | 8 g SO2 | D. | 9.6g H2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,0.1mol D216O中含中子數、質子數、電子數均為NA | |
| B. | 比黃金還貴的18O2和普通的16O2是兩種不同的核素 | |
| C. | 標準狀況下,2.24LCl2溶于水,轉移的電子數目為0.1NA | |
| D. | 1L2mol•L-1的Al(NO3)3溶液中含Al3+個數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 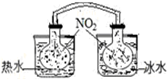 依據兩容器內氣體顏色變化,判斷反應2NO2(g)?N2O4(g)平衡移動的方向 | |
| B. | 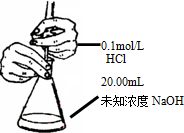 測定錐形瓶內的NaOH的濃度 | |
| C. | 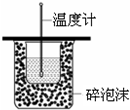 測定中和熱 | |
| D. | 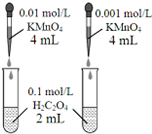 依據褪色快慢比較濃度對反應速率的影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C1>C2 | B. | C1=C2 | C. | C1<C2 | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;③C、D形成的化合物的電子式
;③C、D形成的化合物的電子式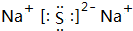 ;
;查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com