
+ 4 |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:閱讀理解
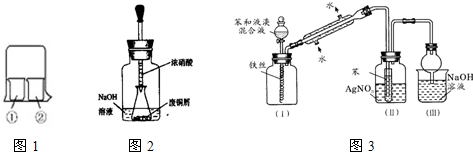
| 實驗編號 | ①中的物質 | ②中的物質 |
| 1 | 淀粉碘化鉀溶液 | 濃硝酸 |
| 2 | 酚酞溶液 | 濃硫酸 |
| 3 | 氯化鋁溶液 | 濃氨水 |
| 4 | 濕潤的紅紙 | 飽和氯水 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
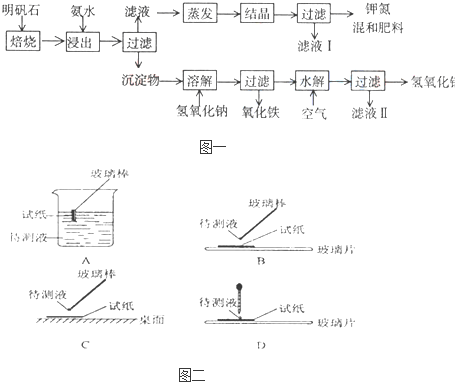
| (m-132n) |
| 42 |
| (m-132n) |
| 42 |
查看答案和解析>>
科目:高中化學 來源: 題型:
已知有關物質的溶、沸點數據如下表所示:
| 化合物 | MgO | Al2O3 | MgCl 2 | AlCl3 |
| 熔點/℃ | 2852 | 2072 | 714 | 190(2.5*105Pa) |
| 沸點/℃ | 3600 | 2980 | 1412 | 182.7 |
請參考上述數據填空和回答問題:
(1)工業上常用電解熔融MgCl 2的方法生產金屬鎂,電解Al2O3與冰晶石熔融混合物的方法生產鋁。為什么不用電解MgO的方法生產鎂,也不用電解AlCl3的方法生產鋁?
答:__________________________________________________________________
(2)氯化鋁是________________(填晶體類型)
(3)在500K和1.01*105Pa時,氯化鋁的蒸氣密度(換算為標準狀況時)為11.92g/L,試確定氯化鋁在蒸氣狀態時的化學式為___________________
(4)無水氯化鋁在空氣中劇烈“發煙”,其原因是________________
(5)設計可靠的實驗證明MgCl 2、AlCl3所屬的晶體類型,其實驗方法是_____________.
查看答案和解析>>
科目:高中化學 來源:2012-2013學年河北省邯鄲市高三第一次模擬考試理綜化學試卷(解析版) 題型:實驗題
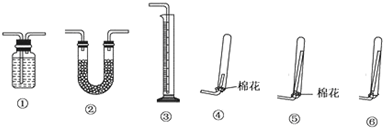
無水氯化鋁是有機化工常用催化劑,其外觀為白色固體,178℃時升華,極易潮解,遇水后會發熱并產生白霧。實驗室用如下裝置制備少量無水氯化鋁,其反應原理為: 2Al+ 6HCl(g) → 2A1Cl3 + 3H2。

完成下列填空:
(1)寫出燒瓶中(B處)發生反應的化學方程式:_____________
(2)C中盛有的試劑為_____。進行實驗時應先點燃_____(選填“B”或“D”)處酒精燈。
(3)用粗短導管連接D、E的目的是_______ (選填序號)。
a.防堵塞 b.防倒吸 c.平衡氣壓 d.冷凝回流
E瓶的作用是_______。
(4)F中盛有堿石灰,其目的是_______(選填序號)。
a.吸收HCl b.吸收Cl2 c.吸收CO2 d.吸收H2O
(5)將D中固體改為市售氯化鋁(AlCl3·6H2O)也能進行無水氯化鋁的制備,此時通入HCl氣體的目的是_______。若實驗條件控制不當,最終得到的物質是堿式氯化鋁[化學式為Al2(OH)nCl(6-n)],且質量是原市售氯化鋁的40%,則可推算n的值為_______。
(6)有人建議將上述裝置A、B中的試劑改為濃鹽酸和二氧化錳,其余裝置和試劑均不變, 也能制備無水AlCl3。事實證明這樣做比較危險,請簡述理由_______
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com