
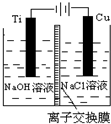
 納米級Cu2O由于具有優良的催化性能而受到關注.采用離子交換膜控制陽極電解液中OH-的濃度制備納米級Cu2O的裝置如圖所示,總反應為2Cu+H2O$\frac{\underline{\;電解\;}}{\;}$Cu2O+H2↑.下列說法不正確的是( )
納米級Cu2O由于具有優良的催化性能而受到關注.采用離子交換膜控制陽極電解液中OH-的濃度制備納米級Cu2O的裝置如圖所示,總反應為2Cu+H2O$\frac{\underline{\;電解\;}}{\;}$Cu2O+H2↑.下列說法不正確的是( )| A. | 鈦(Ti)電極表面發生氧化反應 | |
| B. | 陽極附近溶液的pH逐漸減小 | |
| C. | 離子交換膜宜采用陰離子交換膜 | |
| D. | 陽極表面總反應式是:2Cu+2OH--2e-═Cu2O+H2O |
分析 電解池中,Ti電極為陰極,陰極上氫離子得電子生成氫氣,Cu為陽極,陽極上Cu失電子生成氧化亞銅,氫氧根離子通過離子交換膜進入右側陽極室,所以應該用陰離子交換膜,據此分析.
解答 解:A、鈦極與電源負極相連是陰極發生氫離子得電子的還原反應,故A錯誤;
B、根據總反應,則陽極反應為2Cu-2e-+2OH-=Cu2O+H2O,消耗氫氧根,pH值減小,故B正確;
C、根據總反應,則陽極反應為2Cu-2e-+2OH-=Cu2O+H2O,所以離子交換膜應采用陰離子交換膜,故C正確;
D、在電解池中,當陽極是活潑電極時,該電極本身發生失電子的還原反應,在堿性環境下,金屬銅失去電子的電極反應為2Cu-2e-+2OH-=Cu2O+H2O,故D正確;
故選:A.
點評 本題考查了電解原理的應用,在電解中電極反應與電解質溶液有關,電極相同,電解質溶液的性質不同,電極反應不同,這是很容易出錯的問題,難度不大.


 浙大優學小學年級銜接捷徑浙江大學出版社系列答案
浙大優學小學年級銜接捷徑浙江大學出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | H2O2分子的空間構型為直線形 | |
| B. | CO2分子為非極性分子 | |
| C. | BF3分子中的B原子滿足8電子穩定結構 | |
| D. | CH3COOH分子中C原子均為sp3雜化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲醚(CH3OCH3)被稱為21試劑的新型燃料,它清潔、高效、具有優良的環保性能,甲醚是一種無色氣體,具有輕微的醚香味,其燃燒熱為1455kJ/mol,甲醚可作燃料電池的燃料.
甲醚(CH3OCH3)被稱為21試劑的新型燃料,它清潔、高效、具有優良的環保性能,甲醚是一種無色氣體,具有輕微的醚香味,其燃燒熱為1455kJ/mol,甲醚可作燃料電池的燃料.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗現象 | 實驗結論 |
| A | NaHCO3溶液與NaAlO2溶液混合 | 生成白色沉淀 | 結合H+的能力: CO32-<AlO2- |
| B | 常溫下,相同的鋁片分別投入足量的稀、濃硫酸中 | 濃硫酸中鋁片先溶解完 | 反應物濃度越大,反應速率越快 |
| C | 向2mL 2%的CuSO4溶液中加入0.5mL 1%的NaOH溶液,振蕩后加入幾滴有機試劑X的溶液,加熱 | 未出現磚紅色沉淀 | 有機試劑X中不含醛基 |
| D | 2mL 0.1mol/L的NaOH溶液中滴加2滴0.1mol/L的MgCl2溶液,再滴加2滴0.1mol/L的FeCl3溶液 | 白色沉淀轉化為紅褐色沉淀 | 溶解度: Mg(OH)2>Fe(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③>②>① | B. | ②>①>③ | C. | ①>②>③ | D. | ②>③>① |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
. ;
; .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 改變溫度對反應速率無影響 | |
| B. | 升高溫度能加快反應速率 | |
| C. | 使用催化劑能加快反應速率 | |
| D. | 該反應的化學方程式為:2CO+2NO═N2+2CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 根據如圖的物理模型,回答問題:
根據如圖的物理模型,回答問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com