
下列事實能說明氯的非金屬性比硫強的是
A.次氯酸的酸性比硫酸弱
B.氯氣能置換氫硫酸(H2S的水溶液)中的硫
C.氫硫酸是弱酸,而鹽酸是強酸
D.硫在常溫下為固態(tài),而氯氣為氣態(tài)
B
【解析】
試題分析:比較非金屬元素的非金屬性強弱,可根據單質之間的置換反應、對應最高價氧化物的水化物的酸性、氫化物的穩(wěn)定性等角度判斷。A、元素的非金屬性越強,對應最高價氧化物的水化物的酸性越強,HClO4酸性比H2SO4強,可說明氯元素的非金屬性比硫元素強。但次氯酸不是最高價氧化物對應的水化物,A不正確;B、元素的非金屬性越強,對應單質的氧化性越強,氯氣與H2S能發(fā)生置換反應生成單質S和氯化氫,說明氯氣的氧化性大于S,元素的非金屬性Cl大于S,故B正確;C、不能根據氫化物的水溶液的酸性強弱比較非金屬性,例如HF的酸性比HCl弱,但非金屬性F>Cl,氫硫酸的酸性比鹽酸弱,但非金屬性Cl>S,故C錯誤;D、元素的非金屬性強弱與其單質在常溫下的狀態(tài)無關系,故D不正確,答案選B。
考點:考查元素非金屬性強弱的判斷


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:閱讀理解
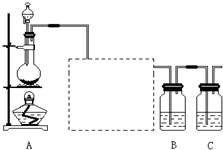 已知非金屬單質硫(S)是淡黃色固體粉末,難溶于水.為了驗證氯元素的非金屬性比硫元素的非金屬性強,某化學實驗小組設計了如下實驗,請回答下列問題:
已知非金屬單質硫(S)是淡黃色固體粉末,難溶于水.為了驗證氯元素的非金屬性比硫元素的非金屬性強,某化學實驗小組設計了如下實驗,請回答下列問題:

查看答案和解析>>
科目:高中化學 來源: 題型:
(15分)已知非金屬單質硫(S)是淡黃色固體粉末,難溶于水。為了驗證氯元素的非金屬性比硫元素的非金屬性強,某化學實驗小組設計了如下實驗,請回答下列問題:
(1)裝置A的分液漏斗中盛裝的試劑是 ,燒瓶中加入的試劑是 。
(2)虛線框內的實驗裝置圖,所加試劑為 ,說明裝置的作用 。
(3)裝置B中盛放的試劑是 (選填下列所給試劑的代碼),實驗現象為 ,
化學反應方程式是 ,
該反應屬于四種基本反應類型中的 反應。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)從原子結構的角度簡要分析氯元素的非金屬性比硫元素的非金屬性強的原因。
(5)還有哪些事實能夠說明氯元素的非金屬性比硫元素的非金屬性強(試舉一例)。
(6)裝置C中盛放燒堿溶液,目的是吸收反應后剩余的氣體,防止污染空氣。在該反應中,Cl元素的化合價既有升高又有降低,即在反應中Cl元素的原子既能獲得電子也能失去電子,能否說氯元素既具有金屬性又具有非金屬性?簡述你的理由。
。
查看答案和解析>>
科目:高中化學 來源:2013屆福建省高一下學期期中考試化學試卷 題型:實驗題
(15分)已知非金屬單質硫(S)是淡黃色固體粉末,難溶于水。為了驗證氯元素的非金屬性比硫元素的非金屬性強,某化學實驗小組設計了如下實驗,請回答下列問題:

(1)裝置A的分液漏斗中盛裝的試劑是 ,燒瓶中加入的試劑是 。
(2)虛線框內的實驗裝置圖,所加試劑為 ,說明裝置的作用 。
(3)裝置B中盛放的試劑是 (選填下列所給試劑的代碼),實驗現象為 ,
化學反應方程式是 ,
該反應屬于四種基本反應類型中的 反應。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)從原子結構的角度簡要分析氯元素的非金屬性比硫元素的非金屬性強的原因。
(5)還有哪些事實能夠說明氯元素的非金屬性比硫元素的非金屬性強(試舉一例)。
(6)裝置C中盛放燒堿溶液,目的是吸收反應后剩余的氣體,防止污染空氣。在該反應中,Cl元素的化合價既有升高又有降低,即在反應中Cl元素的原子既能獲得電子也能失去電子,能否說氯元素既具有金屬性又具有非金屬性?簡述你的理由。
。
查看答案和解析>>
科目:高中化學 來源:0112 期中題 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:
已知非金屬單質硫(S)是淡黃
色固體粉末,難溶于水。為了驗
 證氯元素的非金屬性比硫元素的
證氯元素的非金屬性比硫元素的
非金屬性強,某化學實驗小組設
計了如下實驗,請回答下列問題:
(1) 裝置A的分液漏斗中盛裝的試劑是 ,燒瓶中加入的試劑是 。
(2)畫出虛線框內的實驗裝置圖,并注明所加試劑,說明裝置的作用 。
(3) 裝置B中盛放的試劑是 (此空選填下列所給試劑的代碼),實驗現象為 ,化學反應方程式是 , 該反應屬于四種基本反應類型中的 反應。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4) 還有哪些事實能夠說明氯元素的非金屬性比硫元素的非金屬性強(試舉一例)。 。
(5) 裝置C中盛放燒堿溶液,目的是吸收反應后剩余的氣體,防止污染空氣。在該反應中,Cl元素的化合價既有升高又有降低,即在反應中Cl元素的原子既能獲得電子也能失去電子,能否說氯元素既具有金屬性又具有非金屬性?簡述你的理由。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com