
【題目】氯磺酸(HSO3Cl)在糖精、磺胺藥的生產中有重要的應用。常溫常壓下氯磺酸為無色油狀液體,沸點約為152℃,吸濕性和腐蝕性極強,在空氣中發煙。學習小組在實驗室用SO3和HCl來制備HSO3Cl并測定產品純度。設計如下實驗(夾持裝置略去)。請回答下列問題:
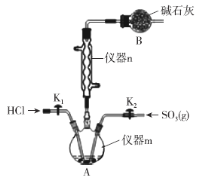
(1)儀器m的名稱為___。
(2)已知:HSO3Cl中硫元素為+6價,O原子和Cl原子的最外層均滿足8電子穩定結構,則HSO3Cl中的化學鍵為___ (填“離子鍵”、“極性鍵”或“非極性鍵”)。
(3)SO3可由五氧化二磷與濃硫酸共熱制備,發生反應的化學方程式為___。
(4)裝置B的作用為___。由儀器n可知制備HSO3Cl的反應為___ (填“放熱反應”或“吸熱反應”)。
(5)HSO3Cl純度的測定(儀器m中得到的HSO3Cl中常溶有少量的SO3):
i.取25.0g產品溶于水中,加入過量的Ba(NO3)2溶液充分反應后,過濾。
ii.向濾液中加入過量的AgNO3溶液,過濾、洗滌、干燥、稱量,測量所得沉淀AgCl的質量為28.7g。
①HSO3Cl遇水發生反應的化學方程式為___。
②產品HSO3Cl的純度為___。
【答案】三頸燒瓶 極性鍵 P2O5+3H2SO4(濃)![]() 3SO3↑+2H3PO4 防止空氣中的水蒸氣進 入反應裝置A中,并吸收揮發出來的HCl氣體 放熱反應 HSO3Cl+H2O=HCl+H2SO4 93.2%
3SO3↑+2H3PO4 防止空氣中的水蒸氣進 入反應裝置A中,并吸收揮發出來的HCl氣體 放熱反應 HSO3Cl+H2O=HCl+H2SO4 93.2%
【解析】
(1)儀器m的名稱為三頸燒瓶。故答案為:三頸燒瓶;
(2)HSO3Cl中硫元素為+6價,O原子和Cl原子的最外層均滿足8電子穩定結構,結構式為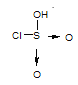 ,則HSO3Cl中的化學鍵為極性鍵 。故答案為:極性鍵;
,則HSO3Cl中的化學鍵為極性鍵 。故答案為:極性鍵;
(3)SO3可由五氧化二磷與濃硫酸共熱制備,發生反應的化學方程式為P2O5+3H2SO4(濃)![]() 3SO3↑+2H3PO4。故答案為:P2O5+3H2SO4(濃)
3SO3↑+2H3PO4。故答案為:P2O5+3H2SO4(濃)![]() 3SO3↑+2H3PO4;
3SO3↑+2H3PO4;
(4)HSO3Cl與水會劇烈反應,由儀器m中逸出的HCl污染空氣,裝置B的作用為防止空氣中的水蒸氣進入反應裝置A中,并吸收揮發出來的HCl氣體。儀器n的作用是冷凝回流HSO3Cl,可知制備HSO3Cl的反應為放熱反應。故答案為:防止空氣中的水蒸氣進入反應裝置A中,并吸收揮發出來的HCl氣體;放熱反應;
(5)①HSO3Cl遇水發生反應的化學方程式為HSO3Cl+H2O=HCl+H2SO4。
②根據題中信息:HSO3Cl~AgCl,生成HSO3Cl的純度為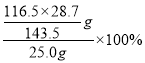 =93.2%。
=93.2%。
故答案為:HSO3Cl+H2O=HCl+H2SO4;93.2%。


科目:高中化學 來源: 題型:
【題目】短周期主族元素X、Y、Z、W的原子序數依次增大,它們原子的最外層電子數之和為14。Z是短周期主族元素中原子半徑最大的元素,Z與X原子的最外層電子數相同,Y與W同主族。下列說法正確的是( )
A.X與Y只能形成一種化合物
B.原子半徑:r(Y)<r(W)<r(Z)
C.W的簡單氣態氫化物的熱穩定性比Y的強
D.Z的最高價氧化物對應的水化物是酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2廣泛用于醫藥、硫酸工業等領域,回收廢氣中的SO2可用如下方法。
方法Ⅰ | 用堿式硫酸鋁Al2(SO4)x(OH)y溶液吸收富集SO2 |
方法Ⅱ | 在Fe2+或Fe3+催化下,用空氣(O2)將SO2氧化為H2SO4 |
(1)方法Ⅰ的過程如下。
① 制備Al2(SO4)x(OH)y。向Al2(SO4)3溶液中加入CaO粉末,調pH至3.6。 CaO的作用是______
② 吸收:Al2(SO4)x(OH)y吸收SO2后的產物是______(寫化學式)。
③ 解吸:加熱②中產物,產生SO2,Al2(SO4)x(OH)y再生。
(2)方法Ⅱ中,在Fe2+催化下,SO2、O2和H2O生成H2SO4的化學方程式是______。
(3)方法Ⅱ中,Fe2+的催化過程可表示如下:
ⅰ:2Fe2++O2+SO2=2Fe3++SO42-
ⅱ:……
① 寫出ⅱ的離子方程式:______。
② 下列實驗方案可證實上述催化過程。將實驗方案補充完整。
a.向FeCl2溶液滴入KSCN,無變化
b.向FeCl2溶液通入少量SO2,滴入KSCN,顏色變紅。
c.取b中溶液,______。
(4)方法Ⅱ中,催化氧化后,采用滴定法測定廢氣中殘留SO2的含量。將V L(已換算為標準狀況)廢氣中的SO2用1%的H2O2完全吸收,吸收液用如圖所示裝置滴定,共消耗a mL c mol/L NaOH標準液。

①H2O2氧化SO2的化學方程式______。
② 廢氣中殘留SO2的體積分數為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W均為短周期元素,它們在元素周期表中的位置如圖所示。若Y原子的最外層電子數是次外層電子數的3倍,下列說法中正確的是( )

A.原子半徑:W>Z>Y>X
B.最高價氧化物對應水化物的酸性:Z>W>X
C.四種元素的單質中,Z單質的熔、沸點最低
D.W的單質能與水反應,生成一種具有漂白性的物質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)乙基叔丁基醚(以ETBE表示)是一種性能優良的高辛烷值汽油調和劑。用乙醇與異丁烯(以IB表示)在催化劑HZSM-5催化下合成ETBE,反應的化學方程式為:C2H5OH(g)+IB(g)=ETBE(g) △H。回答下列問題:
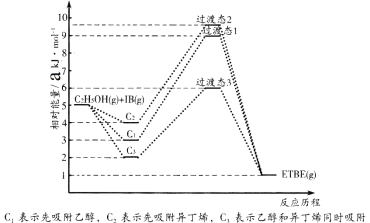
反應物被催化劑HZSM-5吸附的順序與反應歷程的關系如圖所示,該反應的△H=__________ kJ·mol-1。反應歷程的最優途徑是________(填C1、C2或C3)。
(2)開發清潔能源是當今化工研究的一個熱點問題。二甲醚(CH3OCH3)在未來可能替代柴油和液化氣作為潔凈液體燃料使用,工業上以CO和H2為原料生產CH3OCH3。工業制備二甲醚在催化反應室中(壓力2.0~10.0Mpa,溫度230~280℃)進行下列反應:
反應ⅰ:CO(g)+2H2(g)CH3OH(g) ΔH1=-99kJ·mol1
反應ⅱ:2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol1
反應ⅲ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH3=-41.2kJ·mol1
①在該條件下,若反應1的起始濃度分別為:c(CO)=0.6mol·L1,c(H2)=1.4mol·L1,8min后達到平衡,CO的轉化率為50%,則8min內H2的平均反應速率為__________。
②在t℃時,反應2的平衡常數為400,此溫度下,在1L的密閉容器中加入一定的甲醇,反應到某時刻測得各組分的物質的量濃度如下:
物質 | CH3OH | CH3OCH3 | H2O |
c(mol·L1) | 0.46 | 1.0 | 1.0 |
此時刻v正___v逆(填“>”“<”或“=”),平衡時c(CH3OCH3)的物質的量濃度是___。
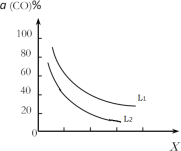
③催化反應室的總反應3CO(g)+3H2(g)CH3OCH3(g)+CO2(g),CO的平衡轉化率α(CO)與溫度、壓強的關系如圖所示,圖中X代表___(填“溫度”或“壓強”),且L1___L2(填“>”“<”或“=”)。
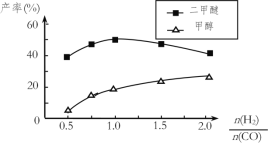
④在催化劑的作用下同時進行三個反應,發現隨著起始投料比![]() 的改變,二甲醚和甲醇的產率(產物中的碳原子占起始CO中碳原子的百分率)呈現如圖的變化趨勢。試解釋投料比大于1.0之后二甲醚產率和甲醇產率變化的原因:______________。
的改變,二甲醚和甲醇的產率(產物中的碳原子占起始CO中碳原子的百分率)呈現如圖的變化趨勢。試解釋投料比大于1.0之后二甲醚產率和甲醇產率變化的原因:______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅的多種化合物在生產生活中都有廣泛用途。請回答下列問題:
(1)Cu2O和CuO是銅的兩種氧化物,可互相轉化。已知:
i.2Cu2O(s)+O2(g)=4CuO(s) △H=-292.0kJ·mol-1
ii.C(s)+2CuO(s)=Cu2O(s)+CO(g) △H=+35.5kJ·mol-1
若CO的燃燒熱為283.0kJ·mol-1,則C(s)的燃燒熱為___。
(2)Cu2O和CuO常用作催化劑。
①質子交換膜燃料電池(PEMFC)的燃料氣中除含有H2外還含有少量的CO和CO2,其中CO是PEMFC催化劑的嚴重毒化劑,可用CuO/CeO2作催化劑優先氧化脫除CO。160℃、用CuO/CeO2作催化劑時,氧化CO的化學方程式為___;分別用HIO3和H3PO4對CuO/CeO2進行處理,在一定條件下,利用不同催化劑進行CO氧化的對比實驗,得如圖曲線,其中催化劑___ (填“b”或“c”)催化性能最好;120℃使用催化劑b進行氧化,若燃料氣中CO的體積分數為0.71%,氣體流速為2000mL·h-1,則1h后,CO體積為___mL。

②在Cu2O催化作用下合成CH3OH,反應如下:CO(g)+2H2(g)![]() CH3OH(g) △H=-90.0kJ·mol-1,有利于提高該反應CO的平衡轉化率的條件是___(填標號)。
CH3OH(g) △H=-90.0kJ·mol-1,有利于提高該反應CO的平衡轉化率的條件是___(填標號)。
A.高溫低壓 B.低溫高壓 C.高溫高壓 D.低溫低壓
T℃時,將CO和H2按一定比例混合后投入容積為2L的恒容密閉容器中,CO的起始濃度為1.0mol·L-1,平衡時,測得體系中,n(H2)=1.4mol,n(CH3OH)=1.7mol,反應達到平衡時CO的轉化率為___,若反應達到平衡狀態后,保持其他條件不變,再充入0.2molCO和0.2molCH3OH,平衡向___(填“正”或“逆”)反應方向移動,理由是___。
(3)CuS呈黑色,是最難溶的物質之一,由于它的難溶性使得一些看似不可能的反應可以發生。向0.01mol·L-1CuSO4溶液中,持續通入H2S維持飽和(H2S飽和濃度為0.1mol·L-1),發生反應:H2S(aq)+Cu2+(aq)![]() CuS(s)+2H+(aq),該反應的化學平衡常數K為___(保留2位有效數字)。已知:Ka1(H2S)=1.1×10-7,Ka2(H2S)=1.3×10-13,Ksp(CuS)=6.3×10-36。
CuS(s)+2H+(aq),該反應的化學平衡常數K為___(保留2位有效數字)。已知:Ka1(H2S)=1.1×10-7,Ka2(H2S)=1.3×10-13,Ksp(CuS)=6.3×10-36。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某試液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干種離子,離子濃度均為0.1mol·L-1,某同學進行了如下實驗,下列說法正確的是

A. 無法確定原試液中是否含有Al3+、Cl-
B. 原溶液中存在NH4+、Fe2+、Cl-、SO42-
C. 無法確定沉淀C的成分
D. 濾液X中大量存在的陽離子有NH4+、Fe2+和Ba2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂稀土合金廣泛應用于航空、航天、電子、通訊和汽車制造業等領域。熔鹽電解法是一種高效制備鎂稀土合金的方法,實驗室制取Mg-Gd合金(物質的量比為1:1)的電解槽示意圖如下(相對原子質量Mg—24,Gd—157),下列說法正確的是

A.添加LiF、BaF2的作用是催化劑
B.陽極的電極反應式為2F——2e—= F2 ↑
C.當電路中通過0.1mol電子時,生成Mg- Gd合金的質量為3.62 g
D.電解結束后,鋁、碳電極質量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素X、Y、Z在元素周期表中的位置如圖所示,下列說法正確的是( )
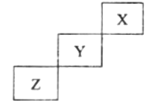
A.非金屬性強弱: Z> Y
B.氣態氫化物的穩定性: Y>Z
C.最高價氧化物的水化物酸性: Y>Z
D.常壓下X的單質化學性質非常活潑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com