
【題目】將一定質量的鎂、銅合金加入到稀硝酸溶液中,兩者恰好完全反應,假設反應過程中還原產物全部是NO,向所得溶液中加入物質的量濃度為3 mol·L-1的NaOH溶液至沉淀完全,測得生成沉淀的質量比原合金的質量增加5.1g,則下列有關敘述中正確的是( )
A. 開始加入合金的質量可能為3.6g
B. 參加反應的硝酸的物質的量為0.1mol
C. 沉淀完全時消耗NaOH溶液的體積為100mL
D. 溶解合金時產生NO的體積為2.24L
【答案】C
【解析】試題分析:將一定量的鎂和銅合金加入到稀HNO3中,二者恰好反應,金屬、硝酸都沒有剩余,反應中還原產物只有NO,發生反應:3Mg+8HNO3(稀)═3Mg(NO3)2+2NO↑+4H2O、3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;
向反應后的溶液中加入3mol/L NaOH溶液至沉淀完全,發生反應:Mg(NO3)2+2NaOH═Mg(OH)2↓+2NaNO3、Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3,沉淀為氫氧化鎂和氫氧化銅,生成沉淀的質量比原合金的質量增加5.1g,則氫氧化鎂和氫氧化銅含有氫氧根的質量為5.1g,氫氧根的物質的量為![]() =0.3mol,根據電子轉移守恒,則鎂和銅的總的物質的量為0.15mol,生成NO為0.1mol,
=0.3mol,根據電子轉移守恒,則鎂和銅的總的物質的量為0.15mol,生成NO為0.1mol,
A.金屬的總質量與金屬的含量有關,假定全為鎂、全為銅計算確定金屬的質量范圍;
B.根據方程式可知參加反應的n反應(HNO3)=![]() n(金屬);
n(金屬);
C.根據V=![]() 計算加入的氫氧化鈉溶液的體積;
計算加入的氫氧化鈉溶液的體積;
D.根據V=nVm計算NO的體積.
解:將一定量的鎂和銅合金加入到稀HNO3中,二者恰好反應,金屬、硝酸都沒有剩余,反應中還原產物只有NO,發生反應:3Mg+8HNO3(稀)═3Mg(NO3)2+2NO↑+4H2O、3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;
向反應后的溶液中加入3mol/L NaOH溶液至沉淀完全,發生反應:Mg(NO3)2+2NaOH═Mg(OH)2↓+2NaNO3、Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3,
沉淀為氫氧化鎂和氫氧化銅,生成沉淀的質量比原合金的質量增加5.1g,
則氫氧化鎂和氫氧化銅含有氫氧根的質量為5.1g,氫氧根的物質的量為![]() =0.3mol,
=0.3mol,
根據電子轉移守恒,則鎂和銅的總的物質的量為![]() =0.15mol,生成NO為
=0.15mol,生成NO為![]() =0.1mol,
=0.1mol,
A.鎂和銅的總的物質的量為0.15mol,假定全為鎂,質量為0.15mol×24g/mol=3.6g,若全為銅,質量為0.15mol×64g/mol=9.6g,所以參加反應的金屬的總質量(m)為3.6g<m<9.6g,故A錯誤;
B.根據方程式可知參加反應的n反應(HNO3)=![]() n(金屬)=
n(金屬)=![]() ×0.15mol=0.4mol,故B錯誤;
×0.15mol=0.4mol,故B錯誤;
C.加入的氫氧化鈉恰好與硝酸鎂、硝酸銅反應,由上述分析可知,加入的NaOH為0.3mol,故加入NaO溶液的體積為![]() =0.1L=100mL,故C正確;
=0.1L=100mL,故C正確;
D.標況下NO的體積為0.1mol×22.4L/mol=2.24L,而狀態不知,故D錯誤,
故選:C.


科目:高中化學 來源: 題型:
【題目】聯芐(![]() )是一種重要的有機合成中間體,實驗室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)為原料,在無水AlCl3催化下加熱制得,其制取步驟為:
)是一種重要的有機合成中間體,實驗室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)為原料,在無水AlCl3催化下加熱制得,其制取步驟為:
(一)催化劑的制備:下圖是實驗室制取少量無水AlCl3的相關實驗裝置的儀器和藥品:

(1)將上述儀器連接成一套制備并保存無水AlCl3的裝置,各管口標號連接順序為:d接e,_______接_______,_________接________,_________接________。
(2)有人建議將上述裝置中D去掉,其余裝置和試劑不變,也能制備無水AlCl3。你認為這樣做是否可行__________(填“可行”或“不可行”),你的理由是________________。
(3)裝置A中隱藏著一種安全隱患,請提出一種改進方案:_____________。
(二)聯芐的制備
聯芐的制取原理為:![]()
反應最佳條件為n(苯) :n(1,2-二氯乙烷)=10 :1,反應溫度在60-65℃之間。
實驗室制取聯芐的裝置如下圖所示(加熱和加持儀器略去):
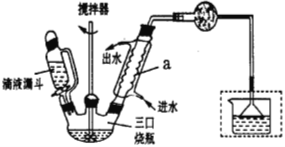
實驗步驟:
在三口燒瓶中加入120.0mL苯和適量無水AlCl3,由滴液漏斗滴加10.7 mL1,2-二氯乙烷,控制反應溫度在60-65℃,反應約60min。將反應后的混合物依次用稀鹽酸、2%Na2CO3溶液和H2O洗滌分離,在所得產物中加入少量無水MgSO4固體,靜止、過濾,先常壓蒸餾,再減壓蒸餾收集170~172℃的餾分,得聯芐18.2 g。
相關物理常數和物理性質如下表
名稱 | 相對分子質量 | 密度/(gcm-1) | 熔點/℃ | 沸點/℃ | 溶解性 |
苯 | 78 | 0.88 | 5.5 | 80.1 | 難溶水,易溶乙醇 |
1,2-二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 難溶水,可溶苯 |
無水氯化鋁 | 133.5 | 2.44 | 178(升華) | 遇水水解,微溶苯 | |
聯芐 | 182 | 0.98 | 52 | 284 | 難溶水,易溶苯 |
(4)儀器a的名稱為______________,和普通分液漏斗相比,使用滴液漏斗的優點是_________。
(5)洗滌操作中,水洗的目的是_____________;無水硫酸鎂的作用是______________。
(6)常壓蒸餾時,最低控制溫度是________________。
(7)該實驗的產率約為______________。(小數點后保留兩位有效數字)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各金屬的混合物2.5g和足量的鹽酸反應,放出的H2在標準狀況下體積為2.24L,其中可能的是
A. Zn和Fe B. Mg和Zn C. Al和Mg D. Cu和Fe
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下圖判斷,下列說法正確的是( )

A. 裝置Ⅰ和裝置Ⅱ中負極反應均是Fe-2e-Fe2+
B. 裝置Ⅰ和裝置Ⅱ中正極反應均是O2+2H2O+4e-4OH-
C. 裝置Ⅰ和裝置Ⅱ中鹽橋中的陽離子均向右側燒杯移動
D. 放電過程中,裝置Ⅰ左側燒杯和裝置Ⅱ右側燒杯中溶液的pH均增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知紅磷通常要比白磷穩定,下列兩個反應:
①P4(白磷,s)+5O2(g)=2P2O5(s) △H1
②4P(紅磷,s)+5O2(g)=2P2O5(s) △H2
則△H1和△H2的關系是
A.△H1=△H2 B.△H1>△H2 C.△H1<△H2 D.無法確定
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化學鍵的敘述,正確的一項是
A.離子化合物中一定含有離子鍵
B.單質分子中均不存在化學鍵
C.全部由非金屬元素形成的化合物中不可能含有離子鍵
D.含有共價鍵的化合物一定是共價化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會、生產、生活密切相關,下列說法正確的是
A.氫氧化鋁、氫氧化鈉都是常見的胃酸中和劑
B.海輪外殼鑲嵌鋅塊是利用犧牲陽極的陰極保護法
C.水泥、瑪瑙、分子篩都是硅酸鹽工業產品
D.明礬凈水時的作用是殺菌、消毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】烏洛托品在合成、醫藥、染料等工業中有廣泛用途,其結構式如圖所示。將甲醛水溶液與氨水混合蒸發可制得烏洛托品。若原料完全反應生成烏洛托品,則甲醛與氨的物質的量之比為( )
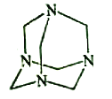
A.1:1 B.2:3 C.3:2 D.2:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com