
分析 (1)所含元素化合價升高的反應物是還原劑,反應中化合價升高的元素有Fe、O元素,計算生成氧氣物質的量,再根據Fe元素、O元素化合價變化計算轉移電子;
(2)①濕法制備高鐵酸鉀(K2FeO4),則FeO42-為產物,Fe(OH)3為反應物,化合價升高總共3價,由電子轉移守恒可知,ClO-為反應物,Cl-為生成物,化合價降低共2將,化合價升降最小公倍數為6,故Fe(OH)3的系數為2,FeO42-的系數為2,ClO-的系數為3,Cl-的系數為3,根據電荷守恒可知,OH-為反應物,系數為4,由元素守恒可知H2O為生成物,其系數為5;
②根據Fe元素化合價變化計算轉移電子,還原產物為Cl-,根據Cl元素化合價變化計算生成Cl-的物質的量;
③由溶解度大的轉化生成溶解度更小的物質.
解答 解:(1)所含元素化合價升高的反應物是還原劑,反應中化合價升高的元素有Fe、O元素,故還原劑為FeSO4、Na2O2,由方程式可知,每生成l mol Na2FeO4同時生成0.5mol氧氣,則轉移電子為1mol×(6-2)=0.5mol×2×[0-(-1)]=5mol,
故答案為:FeSO4、Na2O2;5;
(2)①濕法制備高鐵酸鉀(K2FeO4),則FeO42-為產物,Fe(OH)3為反應物,化合價升高總共3價,由電子轉移守恒可知,ClO-為反應物,Cl-為生成物,化合價降低共2將,化合價升降最小公倍數為6,故Fe(OH)3的系數為2,FeO42-的系數為2,ClO-的系數為3,Cl-的系數為3,根據電荷守恒可知,OH-為反應物,系數為4,由元素守恒可知H2O為生成物,其系數為5,離子方程式為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,
故答案為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;
②反應中Fe元素化合價變化由+3價升高為+6,故每生成1mol FeO42-轉移電子,1mol×(6-3)=3mol,還原產物為Cl-,若反應過程中轉移了0.3mol電子,則還原產物的物質的量為$\frac{0.3mol}{1-(-1)}$=0.15mol,
故答案為:3;0.15;
③該溫度下,K2FeO4的溶解度比Na2FeO4的溶解度更小,在高鐵酸鈉溶液中加入KOH至飽和可析出高鐵酸鉀(K2FeO4),
故答案為:該溫度下,K2FeO4的溶解度比Na2FeO4的溶解度更小.
點評 本題考查氧化還原反應計算與配平、物質的分離提純等,(1)為易錯點,注意根據元素化合價理解.


科目:高中化學 來源: 題型:解答題
 或
或 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 步驟(1)中每析出12.8g S沉淀共轉移0.4mol電子 | |
| B. | 步驟(1)中ZnS的還原性大于MnSO4的還原性 | |
| C. | 電解時MnO2在陽極處產生 | |
| D. | 硫酸在生產中可循環使用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有②③ | B. | 只有③④ | C. | 只有④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 氫氧化物開始沉淀時的pH | 氫氧化物沉淀完全時的pH | |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
 Cu(OH)2+2H+,加入硝酸可以抑制硝酸銅的水解.
Cu(OH)2+2H+,加入硝酸可以抑制硝酸銅的水解.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在化學反應過程中,發生物質變化的同時不一定發生能量變化 | |
| B. | 生成物全部化學鍵形成時所釋放的能量大于破壞反應物全部化學鍵所吸收的能量時,反應為吸熱反應 | |
| C. | 對一個可逆反應來說,吸熱反應一方的速率受溫度變化的影響總是大于放熱反應 | |
| D. | FeCl3+3KSCN?3KCl+Fe(SCN)3 體系中加入KCl固體,平衡向逆反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
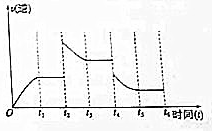 某溫度時,在2L密閉容器中有X、Y、Z三種氣態物質,實驗測得不同時刻各物質的量如下表所示,同時測得至3min時吸收熱量75kJ.
某溫度時,在2L密閉容器中有X、Y、Z三種氣態物質,實驗測得不同時刻各物質的量如下表所示,同時測得至3min時吸收熱量75kJ. | t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.60 | 0.20 | 0.80 |
| 14 | 0.60 | 0.20 | 0.80 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com