
苯乙烯是重要的基礎有機原料。工業中用乙苯(C6 H5- CH2 CH3)為原料,采用催化脫氫的方法制取苯乙烯(C6 H5- CH= CH2)的反應方程式為:
C6 H5- CH2 CH3 (g) C6 H5- CH=CH2 (g) +H2(g) ΔH1
C6 H5- CH=CH2 (g) +H2(g) ΔH1
(1)向體積為VL的密閉容器中充入a mol乙苯,反應達到平衡狀態時,平衡體系組成(物質的量分數)與溫度的關系如圖所示: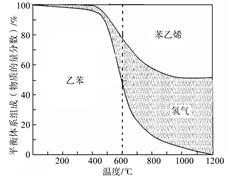
由圖可知:在600℃時,平衡體系中苯乙烯的物質的量分數為25%,則:
① 氫氣的物質的量分數為 ;乙苯的物質的量分數為 ;
② 乙苯的平衡轉化率為 ;
③ 計算此溫度下該反應的平衡常數(請寫出計算過程)。
(2) 分析上述平衡體系組成與溫度的關系圖可知:△H1 0(填“>、=或<” )。
(3)已知某溫度下,當壓強為101.3kPa時,該反應中乙苯的平衡轉化率為30%;在相同溫度下,若反應體系中加入稀釋劑水蒸氣并保持體系總壓為101.3kPa,則乙苯的平衡轉化率 30%(填“>、=、<” )。
(4)已知:
3C2 H2 (g)  C6 H6 (g) ΔH2
C6 H6 (g) ΔH2
C6 H6 (g) + C2H4 (g)  C6 H5- CH2CH3 (g) ΔH3
C6 H5- CH2CH3 (g) ΔH3
則反應3C2H2 (g)+ C2H4 (g)  C6 H5- CH=CH2 (g) +H2(g) 的ΔH= 。
C6 H5- CH=CH2 (g) +H2(g) 的ΔH= 。
(1)①25% ; 50% (共4分,各2分) ②33% (2分)
③(共4分) C6 H5- CH2 CH3 (g)  C6 H5- CH=CH2 (g) + H2(g)
C6 H5- CH=CH2 (g) + H2(g)
起始濃度/( mol?L-1) : a/V 0 0
變化濃度/( mol?L-1) : a/3V a/3V a/3V
平衡濃度/( mol?L-1) : 2a/3V a/3V a/3V(2分)
K =( a/3V? a/3V)/ (2a/3V) = a/6V (2分)
(2)> (2分) ;
(3)> (2分) ;
(4)ΔH1+ΔH2+ΔH3 (2分)
解析試題分析:(1)①從圖中可判斷乙苯的物質的量分數是50%,設消耗乙苯xmol,則生成苯乙烯和氫氣各xmol,所以余(a-x)mol乙苯,則(a-x)mol/(a-x)mol+2xmol=0.5,解得x=1/3amol,所以氫氣的物質的量分數是1/3a/(a+1/3a)×100%=25%;
②乙苯的平衡轉化率為1/3a÷a×100%=33%;
③平衡常數大等于平衡時生成物的濃度冪之積除以反應物的濃度冪之積,首先計算三種物質的平衡濃度,由①分析得平衡時乙苯的物質的量是a-1/3a=2/3a,苯乙烯、氫氣的物質的量都是1/3a,容器體積為VL,所以K=( a/3V? a/3V)/ (2a/3V) = a/6V,計算過程如下(三段式法)
C6 H5- CH2 CH3 (g)  C6 H5- CH=CH2 (g) + H2(g)
C6 H5- CH=CH2 (g) + H2(g)
起始濃度/( mol?L-1) : a/V 0 0
變化濃度/( mol?L-1) : a/3V a/3V a/3V
平衡濃度/( mol?L-1) : 2a/3V a/3V a/3V
K =( a/3V? a/3V)/ (2a/3V) = a/6V
(2)楊浦圖判斷,溫度升高乙苯的物質的量分數減小,說明升溫平衡正向移動,所以正向是吸熱反應△H1>0;
(3)溫度不變,加入稀釋劑水蒸氣并保持體系總壓為101.3kPa,則容器體積增大,相當于給反應體系降低壓強,平衡正向移動,所以再次平衡時乙苯的轉化率>30%;
(4)根據蓋斯定律,將已知三個熱化學方程式相加即得所求方程式,則所求熱效應也等于三式的熱效應相加,所以ΔH=ΔH1+ΔH2+ΔH3。
考點:考查對圖像的分析,混合體系中組分的物質的量分數的計算、轉化率的計算,平衡的移動的判斷,蓋斯定律的應用


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
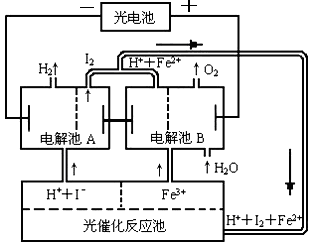
(10分)如右圖所示,常溫下電解5 min后,銅電極質量增加2.16g。
試回答: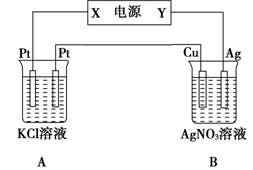
(1)電源電極X名稱為_______(填“正極”或“負極”)。
(2)電解池B中陰極的電極反應式是__________。
(3)若A中KCl溶液的體積是200mL,電解后溶液的
pH=_________(忽略電解前后溶液體積的變化)。
若要使電解后的溶液恢復到與電解完完全相同,應加入的物質是__________。
(4)已知在l0lkPa時,CO的燃燒熱為283 kJ/mol。相同條件下,若2 molCH4完全燃燒生成液態水,所放出的熱量為1 mol CO完全燃燒放出熱量的6.30倍,則CH4完全燃燒的熱化學方程式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)合成氨是人類研究的重要課題,目前工業合成氨的原理為:
合成氨是人類研究的重要課題,目前工業合成氨的原理為:
N2(g)+3H2(g) 2NH3(g)△H=-93.0kJ?mol-1,在3個2L的密閉容器中,使用相同的催化劑,按不同方式投入反應物,分別進行反應:
2NH3(g)△H=-93.0kJ?mol-1,在3個2L的密閉容器中,使用相同的催化劑,按不同方式投入反應物,分別進行反應:
相持恒溫、恒容,測的反應達到平衡時關系數據如下:
| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2mol NH3 |
| 達到平衡的時間/min | | 6 | 8 |
| 平衡時 N2的體積密度 | C1 | 1.5 | |
| 混合氣體密度/g·L-1 | 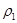 |  | |
| 平衡常數/ L2·mol-2 | K甲 | K乙 | K丙 |
 d.混合氣體的密度保持不變
d.混合氣體的密度保持不變 =
=  b.氮氣的轉化率:
b.氮氣的轉化率: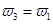 c.
c. 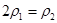 d.
d.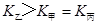
 的電解池,李勇能通過的氫離子的多孔陶瓷固體作電解質,氫氣和氮氣在電極上合成了氨,轉化率達到78%,在電解法合成氨的過程中,應將N2不斷地通入 極,該電極反應式為 。
的電解池,李勇能通過的氫離子的多孔陶瓷固體作電解質,氫氣和氮氣在電極上合成了氨,轉化率達到78%,在電解法合成氨的過程中,應將N2不斷地通入 極,該電極反應式為 。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.通常人們把拆開1 mol某化學鍵所吸收的能量看成該化學鍵的鍵能。下表為一些化學鍵的鍵能數據
| 化學鍵 | Si-Si | O=O | Si-O |
| 鍵能/kJ·mol-1 | a | b | c |
 2NH3(g);△H<0,反應達到平衡后,測得混合氣體為7體積。
2NH3(g);△H<0,反應達到平衡后,測得混合氣體為7體積。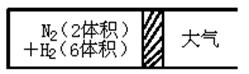
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
根據下列條件計算有關反應的焓變:
(1)已知:
Ti(s)+2Cl2(g)===TiCl4(l) ΔH=-804.2 kJ·mol-1
2Na(s)+Cl2(g)==="2NaCl(s)" ΔH=-882.0 kJ·mol-1
Na(s)===Na(l) ΔH=+2.6 kJ·mol-1
則反應TiCl4(l)+4Na(l)===Ti(s)+4NaCl(s)的ΔH= kJ·mol-1。
(2)已知下列反應數值:
| 序號 | 化學反應 | 反應熱 |
| ① | Fe2O3(s)+3CO(g)=== 2Fe(s)+3CO2(g) | ΔH1=-26.7 kJ·mol-1 |
| ② | 3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) | ΔH2=-50.8 kJ·mol-1 |
| ③ | Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) | ΔH3=-36.5 kJ·mol-1 |
| ④ | FeO(s)+CO(g)===Fe(s)+CO2(g) | ΔH4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
面對目前世界范圍內的能源危機,甲醇作為一種較好的可再生能源,具有廣泛的應用前景。
(1)已知在常溫常壓下反應的熱化學方程式:
①CO(g)+2H2(g)  CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)  CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
寫出由二氧化碳、氫氣制備甲醇的熱化學方程式:_______________________。
(2)在容積為V L的容器中充入a mol CO與2a mol H2,在催化劑作用下反應生成甲醇,平衡時的轉化率與溫度、壓強的關系如圖所示。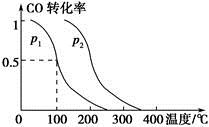
①p1________p2(填“大于”、“小于”或“等于”);
②在其他條件不變的情況下,再增加a mol CO與2a mol H2,達到新平衡時,CO的轉化率________(填“增大”、“減小”或“不變”,下同),平衡常數________。
(3)已知在T ℃時,CO(g)+H2O(g) CO2(g)+H2(g)的平衡常數K=0.32,在該溫度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某時刻經測定CO的轉化率為10%,則該反應________(填“已經”或“沒有”)達到平衡,原因是_________________________________________________
CO2(g)+H2(g)的平衡常數K=0.32,在該溫度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某時刻經測定CO的轉化率為10%,則該反應________(填“已經”或“沒有”)達到平衡,原因是_________________________________________________
此時刻v正________v逆(填“>”或“<”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
二甲醚(CH3OCH3)被稱為21世紀的新型能源,它清潔、高效、具有優良的環保性能。
Ⅰ.工業制備二甲醚的生產流程如下: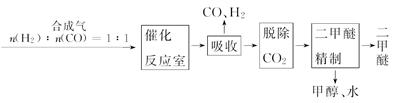
催化反應室中(壓強2.0~10.0 MPa,溫度230~280℃)進行下列反應:
CO(g)+2H2(g) 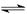 CH3OH(g)ΔH=-90.7 kJ/mol ①
CH3OH(g)ΔH=-90.7 kJ/mol ①
2CH3OH(g) 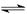 CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②
CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②
CO(g)+H2O(g) 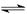 CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③
CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③
(1)甲烷氧化可制得合成氣,反應如下:CH4(g)+ O2(g)
O2(g) 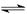 CO(g)+2H2(g) ΔH=-35.6 kJ/mol。該反應是 反應(填“自發”或“非自發”)。
CO(g)+2H2(g) ΔH=-35.6 kJ/mol。該反應是 反應(填“自發”或“非自發”)。
(2)催化反應室中總反應3CO(g)+3H2(g) 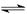 CH3OCH3(g)+CO2(g)的ΔH= 。830℃時反應③的K=1.0,則在催化反應室中反應③的K 1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的ΔH= 。830℃時反應③的K=1.0,則在催化反應室中反應③的K 1.0(填“>”、“<”或“=”)。
(3)上述反應中,可以循環使用的物質有 。
Ⅱ.如圖為綠色電源“二甲醚燃料電池”的工作原理示意圖。b電極是 極。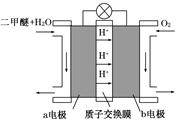
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)合成氨反應的熱化學方程式:N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
已知合成氨反應是一個反應物不能完全轉化為生成物的反應,在某一定條件下,N2的轉化率僅為10%,要想通過該反應得到92.2 kJ的熱量,至少在反應混合物中要投放N2的物質的量為________ mol。
(2)肼(N2H4)-空氣燃料電池是一種堿性燃料電池,電解質溶液是20%~30%的KOH溶液。肼-空氣燃料電池放電時:
正極的電極反應式:__________________________,
負極的電極反應式:__________________________。
(3)如圖是一個電解過程示意圖。
①鋅片上發生的電極反應式是:_______________________
②假設使用肼-空氣燃料電池作為該過程中的電源,銅片質量變化為128 g,則肼-空氣燃料電池理論上消耗標準狀況下的空氣________L(假設空氣中氧氣體積分數為20%)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
將煤轉化為水煤氣的主要化學反應為C(s)+H2O(g)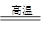 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃燒的熱化學方程式為:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃燒的熱化學方程式為:
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
請回答:
(1)根據以上數據,寫出C(s)與水蒸氣反應的熱化學方程式:________。
(2)比較反應熱數據可知,1 mol CO(g)和1 mol H2(g)完全燃燒放出的熱量之和比1 mol C(s)完全燃燒放出的熱量多。甲同學據此認為“煤轉化為水煤氣可以使煤燃燒放出更多的熱量”;乙同學根據蓋斯定律作出下列循環圖:
并據此認為“煤轉化為水煤氣再燃燒放出的熱量與煤直接燃燒放出的熱量相等”。
請分析:甲、乙兩同學觀點正確的是________(填“甲”或“乙”);判斷的理由是________。
(3)將煤轉化為水煤氣作為燃料和煤直接燃燒相比有很多優點,請列舉其中的兩個優點________。
(4)水煤氣不僅是優良的氣體燃料,也是重要的有機化工原料。CO和H2在一定條件下可以合成:①甲醇;②甲醛;③甲酸;④乙酸。試分析當CO和H2按1:1的體積比混合反應,合成上述________(填序號)物質時,可以滿足“綠色化學”的要求,完全利用原料中的原子,實現零排放。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com