
元素周期表是一座開放的“元素大廈”,元素大廈尚未客滿。若發現119號元素,請您在元素大廈中安排好它的“房間”
A.第七周期第0族 B.第六周期ⅡA族
C.第八周期第ⅠA族 D.第七周期第ⅦA族
科目:高中化學 來源:2016屆湖南省等四校高三聯考化學試卷(解析版) 題型:實驗題
為驗證MnO2在KC1O3受熱分解制O2的反應前后質量不變,某興趣小組利用如圖所示裝置進行了如下實驗:

(1)連接好裝置后,如何檢查裝置的氣密性? 。
(2)取2.45 g KClO3固體粉末與0.87g MnO2粉末充分混勻,置于如圖所示裝置的試管中,充分加熱后,停止加熱,移去酒精燈之前,應先 ;調節量筒內液面與水槽內液面高度相同,量筒內收集到的氣體體積 0.735L(填“>” “<”或“=”)。已知室溫下氣體摩爾體積為24.5 L•mol-1,不考慮氧氣在水中的溶解及水蒸氣的影響)。
(3)取充分加熱后試管中的殘余固體,溶于50 mL 1.0 mol • L-1稀硫酸中,加入50 mL 0.30 mol • L-1 Na2C2O4 溶液,待與Mn02作用完畢后,用 0.10 mol • L-1 KMn04標準溶液進行滴定,消耗KMn04標準溶液V mL(已知Mn2+對滴定反應有催化作用)[
A.寫出Mn02與Na2C204反應的離子方程式 ;
B.當消耗KMnO4標準溶液的體積V= mL時,表明MnO2在反應前后質量不變。
C.若盛裝標準液的滴定管沒有用標準液潤洗,所測Mn02質量會 (填“偏大”、“偏小”或“不變”,下同);若滴定終點時明顯出現黑色沉淀,所測質量會 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年天津市高一下期中化學試卷(解析版) 題型:選擇題
下列反應中屬于加成反應的是
A乙烯使酸性KMnO4溶液褪色
B.將苯滴入溴水中,振蕩后水層接近無色
C.乙烯使溴水褪色
D.甲烷與氯氣混合,黃綠色消失
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一下期中化學試卷(解析版) 題型:選擇題
下列有關化學反應速率的說法正確的是
A.用鐵片和稀硫酸反應制取氫氣時,改用98%的濃硫酸可以加快產生氫氣的速率
B.100mL2mol/L的鹽酸跟鋅片反應,加入適量的氯化鈉溶液,反應速率不變
C.SO2的催化氧化時一個放熱的反應,所以升高溫度,反應速率減慢
D.汽車尾氣中的NO和CO可以緩慢生成N2和CO2,減小壓強,反應速率減慢
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一下期中化學試卷(解析版) 題型:選擇題
下列說法合理的是
A.液態氟化氫中存在氫鍵,所以其分子比氯化氫更穩定
B.由水溶液的酸性:HCl>H2S,可推斷出元素的非金屬性:Cl>S
C.能形成+7價含氧酸及其鹽的元素一定屬于主族元素
D.原子最外層電子數等于6的元素一定屬于主族元素
查看答案和解析>>
科目:高中化學 來源:2015-2016學年寧夏育才中學高一下期中化學試卷(解析版) 題型:填空題
如圖所示,把試管放入盛有25℃飽和石灰水的燒杯中,試管開始放入幾小塊鎂片,再用滴管滴入5mL鹽酸于試管中。試回答下列問題:
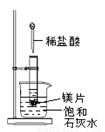
(1)實驗中觀察到的現象是____________________;
(2)產生上述現象的原因是____________________;
(3)寫出有關的離子方程式:________________ __。
(4)由實驗推知,反應中生成MgCl2和H2形成化學鍵時
所釋放的總能量____(填“大于”“小于”或“等于”)消耗鎂片和鹽酸時斷裂化學鍵所吸收的總能量。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年寧夏育才中學高一下期中化學試卷(解析版) 題型:選擇題
形成原電池的條件一般有:①電解質溶液;②兩個電極;③能自發地發生氧化還原反應;④形成閉合回路,請根據上述條件判斷下列裝置中屬于原電池的是( )
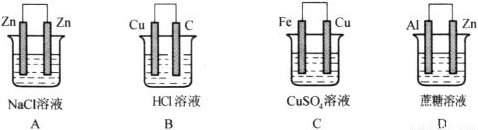
查看答案和解析>>
科目:高中化學 來源:2015-2016學年寧夏育才中學高一下期中化學試卷(解析版) 題型:選擇題
雷雨天閃電時空氣中有臭氧生成,下列說法正確的是( )
A.16O2和18O3互為同位素
B.O2和O3的相互轉化是物理變化
C.等物質的量的O2和O3含有相同的質子數
D.等質量的O2和O3含有相同的O原子數
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三第二次模擬理綜化學試卷(解析版) 題型:填空題
【化學—選修3:物質結構與性質】
I.80%左右的非金屬元素在現代技術包括能源、功能材料等領域占有極為重要的地位。
(1)氮及其化合物與人類生產、生活息息相關,基態N原子中電子在2p軌道上的排布遵循的原則是________,N2F2分子中N原子的雜化方式是____________,1mol N2F2含有______個σ鍵。
(2)高溫陶瓷材料Si3N4晶體中鍵角N—Si—N________Si—N—Si(填“>”“<”或“=”),原因是_________。
II.金屬元素在現代工業中也占據極其重要的地位,鈦被稱為“未來的鋼鐵”,具有質輕,抗腐蝕,硬度大特點,是理想化工設備材料。
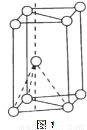
(3)基態鈦原子核外共有________種運動狀態不相同的電子。金屬鈦晶胞如下圖1所示,為_______
堆積(填堆積方式)。
4)納米TiO2是一種應用廣泛的催化劑,其催化的一個實例如下圖2。化合物乙的沸點明顯高于化合物甲,主要原因是_______。化合物乙中采取sp3雜化的原子的電負性由大到小的順序為__________。

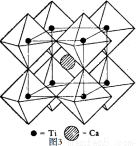
(5)鈣鈦礦晶體的結構如圖3所示。假設把氧離子看做硬球接觸模型,鈣離子和鈦離子填充氧離子的空隙,氧離子形成正八面體,鈦離子位于正八面體中心,則一個鈦離子被__________個氧離子包圍。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com