
| A. | Zn、FeCl2溶液、MgCl2溶液 | B. | Fe、Zn、MgCl2溶液 | ||
| C. | Mg、ZnCl2、FeSO4溶液 | D. | Fe、ZnSO4溶液、MgCl2溶液 |
分析 要驗證這三種金屬的活動性順序,可以利用金屬之間的置換反應來實現(xiàn),如果金屬和另外金屬的鹽溶液能發(fā)生金屬之間的置換反應,則能證明金屬的活動性順序,據(jù)此分析解答.
解答 解:要驗證這三種金屬的活動性順序,可以利用金屬之間的置換反應來實現(xiàn),如果金屬和另外金屬的鹽溶液能發(fā)生金屬之間的置換反應,則能證明金屬的活動性順序,這三種金屬中金屬性強弱順序是Mg>Zn>Fe,所以應該用Zn、可溶性鎂鹽及可溶性鐵鹽溶液來驗證即可,Zn和氯化鎂溶液不反應、能置換出氯化亞鐵中Fe,故選A.
點評 本題金屬性強弱順序判斷,為高頻考點,側(cè)重考查學生實驗設計能力,明確金屬性強弱判斷方法是解本題關鍵,熟練掌握金屬性強弱判斷方法及實驗現(xiàn)象、實驗結(jié)論,題目難度不大.


 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
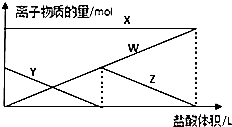 向aL1mol•L-1的Na2CO3的溶液中緩慢地滴加bL1mol•L-1的鹽酸,并不斷攪拌,隨著鹽酸的加入,溶液中離子物質(zhì)的量也相應地發(fā)生變化如圖所示(不考慮鹽類的水解及水的電離),下列說法正確的是( )
向aL1mol•L-1的Na2CO3的溶液中緩慢地滴加bL1mol•L-1的鹽酸,并不斷攪拌,隨著鹽酸的加入,溶液中離子物質(zhì)的量也相應地發(fā)生變化如圖所示(不考慮鹽類的水解及水的電離),下列說法正確的是( )| A. | 四條線與溶液中離子的對應關系是:X:Na+;Y:CO32-;Z:Cl-;W:HCO3- | |
| B. | 當a<b<2a時,發(fā)生的離子方程式為:CO32-+H+=CO2↑+H2O | |
| C. | 當3b=2a時,發(fā)生的離子方程式為:HCO3-+H+=CO2↑+H2O | |
| D. | 當$\frac{a}{2}$<b<a時,溶液中HCO32-與CO32-的物質(zhì)的量之比為b:(a-b) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下,當N2的生成速率與N2的分解速率相等時,該反應處于平衡狀態(tài) | |
| B. | 取1mol N2和3mol H2放在密閉容器內(nèi)反應達平衡時,生成2 mol NH3 | |
| C. | 一定條件下反應達到平衡,再充入N2,則正反應速率增大,逆反應速率減小 | |
| D. | 一定條件下反應達到平衡,若升高溫度,反應速率增大,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 陽極 | 陰極 | 溶液甲 | 物質(zhì)乙 |
| A.Pt | Pt | NaOH | NaOH固體 |
| B.銅 | 鐵 | CuSO4 | CuO |
| C.C | Pt | NaCl | 鹽酸 |
| D.Pt | Pt | H2SO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,其與過量的NaOH溶液反應的化學方程式是
,其與過量的NaOH溶液反應的化學方程式是 +2NaOH→
+2NaOH→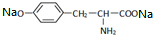 +2H2O.由酪氨酸生成聚酯的化學方程式是
+2H2O.由酪氨酸生成聚酯的化學方程式是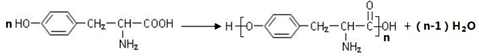 .
.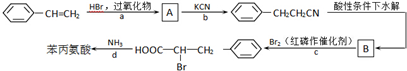
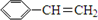 +HBr→
+HBr→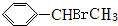 .
. +Br2$\stackrel{紅磷}{→}$
+Br2$\stackrel{紅磷}{→}$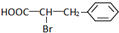 +HBr.
+HBr.查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com