
| A.溫度控制在500℃有利于合成氨反應 |
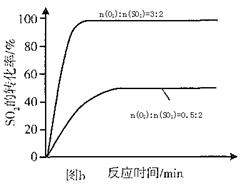
| B.用排飽和食鹽水法收集Cl2 |
| C.打開碳酸飲料會有大量氣泡冒出 |
| D.在硫酸工業生產中使用過量的氧氣 |
 名校名卷單元同步訓練測試題系列答案
名校名卷單元同步訓練測試題系列答案科目:高中化學 來源:不詳 題型:填空題
 2SO3(g) ΔH=-92.3KJ/mol,反應過程中,SO2、O2、SO3的物質的量(mol)的變化如下表(0~4min時,容器氣體壓強為0.1MPa):
2SO3(g) ΔH=-92.3KJ/mol,反應過程中,SO2、O2、SO3的物質的量(mol)的變化如下表(0~4min時,容器氣體壓強為0.1MPa):| 時間min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| n(SO2) | 2.00 | 1.92 | 1.84 | 1.76 | 1.76 | 1.64 | 1.52 | 1.40 | 1.40 | 1.40 |
| n(O2) | 1.00 | 0.96 | 0.92 | 0.88 | 0.88 | 0.82 | 0.76 | 0.70 | 0.70 | 0.70 |
| n(SO3) | 0 | 0.08 | 0.16 | 0.24 | 0.24 | 0.36 | 0.48 | 0.60 | 0.60 | 0.60 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);該反應達到平衡后,放出的熱量為Q1 kJ,物質X的轉化率為α;若平衡后再升高溫度,混合氣體的平均相對分子質量減小。
aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);該反應達到平衡后,放出的熱量為Q1 kJ,物質X的轉化率為α;若平衡后再升高溫度,混合氣體的平均相對分子質量減小。| 溫度/℃ | 200 | 250 | 300 | 350 |
| 平衡常數K | 9.94 | 5.2 | 1 | 0.5 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g) △H = –197kJ/mol達平衡后,各容器內放出熱量Q1、Q2、Q3和Q4的大小關系正確的是
2SO3(g) △H = –197kJ/mol達平衡后,各容器內放出熱量Q1、Q2、Q3和Q4的大小關系正確的是
| A.197>Q1>Q2 | B.Q1>2Q3 | C.Q1=Q4 | D.Q3<Q4 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.工業合成氨時使用催化劑 |
| B.配制FeCl3溶液時加入少量的鹽酸 |
| C.在Na2CO3溶液中,由水電離出的c(OH-) >1×10-7mol/L |
| D.AgCl在水中的溶解度大于在飽和NaCl溶液中的溶解度 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 nC(g)(正反應放熱),在相同溫度、不同壓強時,A的轉化率跟反應時間(t)的關系如圖所示,其中結論正確的是( )
nC(g)(正反應放熱),在相同溫度、不同壓強時,A的轉化率跟反應時間(t)的關系如圖所示,其中結論正確的是( )
| A.p1>p2,n>3 |
| B.p1<p2,n>3 |
| C.p1<p2,n<3 |
| D.p1>p2,n=3? |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g) △H<0,450℃時,n(SO3)和n(O2)隨時間的變化關系如圖所示,下列說法正確的是
2SO3(g) △H<0,450℃時,n(SO3)和n(O2)隨時間的變化關系如圖所示,下列說法正確的是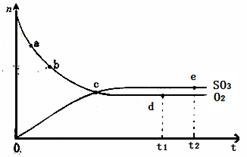
| A.點c處反應達到平衡 |
| B.點a的正反應速率比點b的大 |
| C.點d (t1時刻)和點e (t2時刻)處n(SO2)不一樣 |
| D.其他條件不變,600℃時反應至t1時刻,n(SO 3)比上圖中的d點值要大 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 PCl5(g)達到平衡時,PCl5為0.40mol,如果此時移走1.0molPCl3和0.50molCl2,在相同溫度下再達平衡時PCl5的物質的量是
PCl5(g)達到平衡時,PCl5為0.40mol,如果此時移走1.0molPCl3和0.50molCl2,在相同溫度下再達平衡時PCl5的物質的量是| A.0.40mol | B.小于0.20mol | C.0.20mol | D.大于0.20mol,小于0.40mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
A.2NO2(g)  N2O4(g)△H<0 N2O4(g)△H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2 H I(g)△H<0 2 H I(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g)△H>0 NH3(g)+H2O(g)+CO2(g)△H>0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com