
【題目】下列有關氯水的敘述中,不正確的是
A. 新制氯水呈黃綠色,且有刺激性氣味,說明有Cl2分子存在
B. 新制氯水只能使紫色石蕊試紙變紅
C. 新制氯水放置數(shù)天后酸性增強
D. 加入NaOH溶液,氯水黃綠色消失,說明有HClO分子存在
【答案】BD
【解析】
氯氣溶于水形成氯水,部分氯氣與水發(fā)生反應為Cl2+H2OHCl+HClO,HClO![]() H++ClO-,次氯酸因其自身的強氧化性而具有漂白作用,且不穩(wěn)定,光照下會分解,反應為2HClO
H++ClO-,次氯酸因其自身的強氧化性而具有漂白作用,且不穩(wěn)定,光照下會分解,反應為2HClO![]() 2HCl+O2↑,再結合離子、分子的性質來分析作答。
2HCl+O2↑,再結合離子、分子的性質來分析作答。
A. Cl2為黃綠色,有刺激性氣味,溶于水后部分氯氣與水發(fā)生反應為Cl2+H2OHCl+HClO,因此新制氯水呈黃綠色,且有刺激性氣味,說明有Cl2分子存在,故A項正確;
B.新制氯水中因含強氧化性的HClO而具有漂白性,因此新制氯水會使紫色石蕊試紙先變紅后褪色,故B項錯誤;
C.氯水中HClO為弱酸且不穩(wěn)定,見光易分解,反應為:2HClO![]() 2HCl+O2↑,因此新制氯水放置數(shù)天后酸性會增強,故C項正確;
2HCl+O2↑,因此新制氯水放置數(shù)天后酸性會增強,故C項正確;
D.因氯氣可以與NaOH溶液反應,2NaOH+Cl2=NaCl+NaClO+H2O,因此加入NaOH溶液,氯水黃綠色消失,故D項錯誤;
答案選BD。


科目:高中化學 來源: 題型:
【題目】向一容積不變的密閉容器中充入一定量A(g)和B,發(fā)生反應:xA(g)+2B(s) ![]() yC(g) △H<0.在一定條件下,容器中A、C的物質的量濃度隨時間變化的曲線如圖所示。
yC(g) △H<0.在一定條件下,容器中A、C的物質的量濃度隨時間變化的曲線如圖所示。
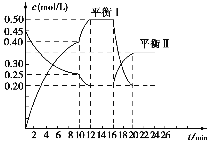
請回答下列問題
(1)根據(jù)圖示可確定x:y=________。
(2)0-10min容器內壓強______ (填“變大”、“ 不變”或“變小”)
(3)推測第10min引起曲線變化的反應條件可能是______(填編號,下同);第16min引起曲線變化的反應條件可能是________。
①減壓 ② 增大A的濃度 ③增大C的量 ④升溫 ⑤ 降溫⑥ 加催化劑
(4)若平衡1的平衡常數(shù)為K1,平衡II的平衡常數(shù)為K2,則K1______(填“>”“=”或“<”)K2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學反應中,屬于氧化還原反應的是
A. Na2CO3 + CaCl2=CaCO3 ↓ + 2NaCl B. Cl2 + 2KI=2KCl + I2
C. 2NaHCO3 ![]() Na2CO3 + CO2 ↑ + H2O D. CaO + H2O=Ca(OH)2
Na2CO3 + CO2 ↑ + H2O D. CaO + H2O=Ca(OH)2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四氧化三錳(Mn3O4)是電子工業(yè)的磁性材料,而氯化鉛(PbCl2)常用于焊料和助溶劑、制備其他鉛鹽等。用方鉛礦精礦(主要成分為PbS)和軟錳礦(主要成分是MnO2,還含有Fe2O3、Al2O3等雜質)制備PbCl2和Mn3O4的工藝流程如下:

已知:PbCl2(s) + 2Cl-(aq) ![]() PbCl42- ( aq) ΔH > 0
PbCl42- ( aq) ΔH > 0
(1)80℃時,為提高方鉛礦精礦、軟錳礦與鹽酸反應的速率,可采取的措施有________(寫出一條即可)。
(2)試劑X是___________。(填“化學式”)
(3)用鹽酸處理兩種礦石粉末,生成MnCl2、PbCl2和S的總反應化學方程式為___________。
(4)結合化學用語回答,向酸浸液中加入飽和食鹽水的目的是___________。
(5)向濾液b中通入NH3和O2發(fā)生反應后,總反應的離子方程式為___________。
(6)金屬錳可以用Mn3O4為原料,通過鋁熱反應來制備,當生成5.5 kg Mn 時,理論上消耗金屬鋁的質量最少為___________kg。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出下面的烴的名稱或結構簡式:
(1) _________________________________,
_________________________________,
(2)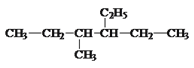 _______________________________,
_______________________________,
(3) __________________________________,
__________________________________,
(4)間甲基苯乙炔___________________________________,
(5)3-乙基-1-庚烯____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在0.1mol·L-1NH3·H2O 溶液中有如下電離平衡:NH3·H2O ![]() NH4++OH- 對于該平衡,下列敘述正確的是
NH4++OH- 對于該平衡,下列敘述正確的是
A.加入水時,平衡向逆反應方向移動
B.加入少量NaOH固體,平衡向逆反應方向移動
C.加入少量 0.1 mol·L-1鹽酸,溶液中c(H+)減小
D.加入少量NH4Cl固體,平衡向正反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列物質的電離方程式如下:
HClO4![]() H++ClO4-;
H++ClO4-;
Ba(OH)2![]() Ba2++2OH-;
Ba2++2OH-;
Fe2(SO4)3![]() 2Fe3++3SO42-;
2Fe3++3SO42-;
KHSO4![]() K++H++SO42-。
K++H++SO42-。
屬于酸的物質是______(寫化學式,下同);屬于堿的物質是______;屬于鹽的物質是___________。
(2)化工生產(chǎn)中常常用到“三酸兩堿”,“三酸”指硝酸、硫酸和鹽酸,“兩堿”指燒堿和純堿。
①從物質的分類角度看,不恰當?shù)囊环N物質是______。
②上述物質中既不是電解質也不是非電解質的是______。依據(jù)是__________。
③寫出純堿的電離方程式:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2的固定和利用對降低溫室氣體排放具有重要作用,CO2加氫合成甲醇不僅可以有效緩解減排壓力,而且還是CO2綜合利用的一條新途徑。CO2和H2在催化劑作用下能發(fā)生反應:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。測得甲醇的理論產(chǎn)率與反應溫度、壓強的關系如圖所示。
CH3OH(g)+H2O(g)。測得甲醇的理論產(chǎn)率與反應溫度、壓強的關系如圖所示。

(1)下列措施能使CO2的轉化率提高的是__。
A. 增大壓強 B.升高溫度 C.增大投料比 D.加入更高效的催化劑
(2)在220℃、5.0MPa時,CO2、H2的轉化率之比為______。
(3)將溫度從220℃降低至160℃,壓強從5.0MPa減小至3.0MPa,化學反應速率將___(填“增大”“減小”或“不變”,下同),CO2的轉化率將____。
(4)200℃時,將0.100 mol CO2和0.275 mol H2充入1 L密閉容器中,在催化劑作用下反應達到平衡。若CO2的轉化率為25%,則此溫度下該反應的平衡常數(shù)K=___ 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com