
(1)Na2SO3溶液蒸干得到的固體物質是___________,原因是______________.
(2)碳酸氫鋇溶液蒸干得到的固體物質是___________,原因是___________________.
(3)鹽酸與硫酸濃度各為1mol/L 的混合酸10mL,加熱濃縮至1mL,最后得到的溶液濃度
為_________,原因是_____________________________________________________。
(4)與c(H+)·c(OH-)=kw類似,FeS飽和溶液中存在:FeS(s) ![]() Fe
Fe![]()
![]() +S
+S![]()
![]() ,
,
c(Fe![]() )·c(s
)·c(s![]() )=ksp。常溫下ksp=8.1×10-17。(溶液密度為1.0g/cm3)。
)=ksp。常溫下ksp=8.1×10-17。(溶液密度為1.0g/cm3)。
理論上FeS的溶解度為___________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| △ |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
(1)濾液中除Na2S2O3和可能未反應完全的Na2SO3外,最可能的雜質是__________。它是由________________而產生的。如果濾液中該雜質的含量不是很低,其檢測方法是________________________________。
(2)設Na2SO3跟硫粉完全反應,將濾液蒸發濃縮后,冷卻至70 ℃,溶液的體積約為30 mL,該溶液是否達到飽和?試通過計算說明。(70 ℃時,Na2S2O3飽和溶液的密度為1.17 g·cm-3)
(3)若要計算在100 ℃下將溶液蒸發至體積為30.0 mL,再冷卻至10 ℃所能得到的Na2S2O3·5H2O的質量,你認為__________(填寫1個選項字母)。
A.前面提供的數據已經足夠
B.還需要提供100 ℃時溶液的密度(1.14 g·cm-3)
C.還需提供結晶后剩余溶液體積(10.0 mL)
(4)根據第(3)小題的選擇(如選A項則直接計算,如選B項或C項則可選用其數據計算),計算從10 ℃ 30.0 mL溶液中結晶析出的Na2S2O3·5H2O質量。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市楊浦區高三上學期學業質量調研化學試卷(解析版) 題型:計算題
硫有多種化合物,許多含硫化合物在工業上有重要的用途。
(1)工業上可用黃鐵礦、焦炭在有限的空氣中燃燒制備硫磺。
3FeS2 + 12C+ 8O2  Fe3O4 + nA↑+ 6S
Fe3O4 + nA↑+ 6S
A是 (寫化學式)。若得到192克的硫磺,則產生標準狀況下的A氣體 L。
(2)硫的氯化物常做橡膠工業的硫化劑。硫與氯氣在一定條件下反應,得到兩種硫的氯化物B和D。B物質中的含硫量為0.3107,D物質中的含氯量為0.5259,B的相對分子質量比D小32。計算確定這兩種氯化物的分子式分別為 。
(3)硫化氫有毒。在120℃、101kPa,將H2S和O2在密閉容器中點燃,充分反應后又恢復到了原來的溫度和壓強時,氣體體積減少30%,求原混合其氣體中H2S的體積分數。寫出推導過程。(不考慮硫化氫的分解)
(4)硫代硫酸鈉是重要的還原劑,可用亞硫酸鈉和硫粉在水溶液中加熱制得。取15.12g Na2SO3溶于80.0mL水中,加入5.00g硫粉,用小火加熱至微沸,反應約1小時后過濾,將濾液蒸發至體積為30.0mL,再冷卻到10℃,則理論上析出Na2S2O3∙5H2O多少克?寫出推導過程。(已知:Na2S2O3的溶解度,10℃時為60.0g/100g水,100℃時為207g/100g水。100℃時,Na2S2O3飽和溶液的密度為1.14g/mL)。
查看答案和解析>>
科目:高中化學 來源: 題型:
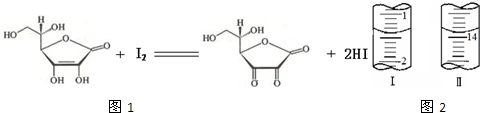
(10分)維生素C(C6H8O6,相對分子質量為176)可溶于水,具有強還原性,在堿性溶液中易被空氣氧化,在酸性介質中較為穩定。維生素C通常用標準I2溶液(I2在水中溶解度很小,易溶于KI溶液,I2+I–![]() I3–,故標準I2溶液應配成I2的KI溶液)進行滴定,原理如下:
I3–,故標準I2溶液應配成I2的KI溶液)進行滴定,原理如下:

(1)滴定過程中應選用 (填酸式或堿式)滴定管盛放標準I2溶液,滴定所用的指示劑為 ,出現 現象時即為滴定終點。
(2)待測維生素C溶液在配制過程中,可以加入下列試劑中的 (填字母)
 A.0.1 mol·L-1 CH3COOH B.0.1 mol·L-1 HNO3
A.0.1 mol·L-1 CH3COOH B.0.1 mol·L-1 HNO3
C.0.1 mol·L-1 NaOH D.0.1 mol·L-1 Na2SO3
(3)配制一定物質的量濃度的標準I2溶液所需玻璃儀器有 (填字母)
A.容量瓶 B.膠頭滴管 C.玻璃棒 D.燒杯 E.量筒
(4)將1.0 g 維生素樣品制成100 mL溶液,取25 mL用0.1 mol·L-1的I2溶液滴定,滴定前后滴定管中示數如圖,則樣品中維生素C的質量分數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com