
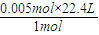 =0.112L=112mL,
=0.112L=112mL,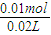 =0.5mol/L,
=0.5mol/L,

科目:高中化學 來源: 題型:
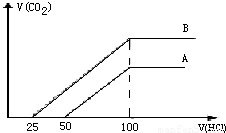
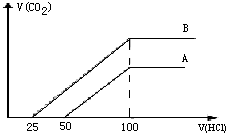 取等物質的濃度NaOH溶液兩份A和B,每份20ml,向其中各通入一定量的CO2,然后分別將其稀釋為100ml,分別向稀釋后的溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生CO2氣體體積與所加鹽酸的體積(單位為ml)的關系如圖所示.
取等物質的濃度NaOH溶液兩份A和B,每份20ml,向其中各通入一定量的CO2,然后分別將其稀釋為100ml,分別向稀釋后的溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生CO2氣體體積與所加鹽酸的體積(單位為ml)的關系如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:
 取等物質的量濃度的NaOH溶液兩份A和B,每份10mL,分別向A、B中通入不等量的CO2,再繼續向兩溶液中逐滴加入0.1 mol/L的鹽酸,標準狀況下產生的CO2的體積與所加鹽酸體積之間的關系如圖所示,試回答下列問題:
取等物質的量濃度的NaOH溶液兩份A和B,每份10mL,分別向A、B中通入不等量的CO2,再繼續向兩溶液中逐滴加入0.1 mol/L的鹽酸,標準狀況下產生的CO2的體積與所加鹽酸體積之間的關系如圖所示,試回答下列問題:查看答案和解析>>
科目:高中化學 來源:四川省華鎣中學2008屆高三第一次月考化學試題 題型:022
取等物質的濃度NaOH溶液兩份A和B,每份20 ml,向其中各通入一定量的CO2,然后分別將其稀釋為100 ml,分別向稀釋后的溶液中逐滴加入0.1 mol/L的鹽酸,標準狀況下產生CO2氣體體積與所加鹽酸的體積(單位為ml)的關系如下圖所示

(1)曲線A表明,原溶液中通入CO2后,所得溶液中的溶質為(寫化學式)________,加入鹽酸后產生CO2體積的最大值________ml,滴入鹽酸的過程中發生反應的離子方程式________、________.
(2)曲線B表明,原溶液中通入CO2后,所得溶液中的溶質為(寫化學式)________,兩溶質物質的量之比為________;加入鹽酸后產生CO2體積的最大值為________ml.
(3)求原NaOH溶液物質的量的濃度________mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
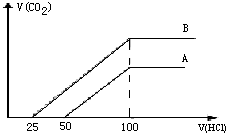 取等物質的濃度NaOH溶液兩份A和B,每份20ml,向其中各通入一定量的CO2,然后分別將其稀釋為100ml,分別向稀釋后的溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生CO2氣體體積與所加鹽酸的體積(單位為ml)的關系如圖所示.
取等物質的濃度NaOH溶液兩份A和B,每份20ml,向其中各通入一定量的CO2,然后分別將其稀釋為100ml,分別向稀釋后的溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生CO2氣體體積與所加鹽酸的體積(單位為ml)的關系如圖所示.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com