
| A. | 用pH試紙測得該消毒液的pH約為12 | |
| B. | 該消毒液中,Fe3+、K+、NO${\;}_{3}^{-}$、CH3CHO可以大量共存 | |
| C. | 向該消毒液中滴入少量Na2SO3溶液,反應的離子方程為:SO${\;}_{3}^{2-}$+ClO-=Cl-+SO${\;}_{4}^{2-}$ | |
| D. | 向該消毒液中加入濃鹽酸,每產生1mol Cl2,轉移電子數約為2×6.02×1023 |
分析 A.NaClO具有漂白性,不能用pH試紙測定pH;
B.CH3CHO能被NaClO氧化;
C.NaClO與Na2SO3發生氧化還原反應生成NaCl和硫酸鈉;
D.根據方程式ClO-+Cl-+2H+=Cl2↑+H2O計算.
解答 解:A.NaClO具有漂白性,能使pH褪色,所以不能用pH試紙測定pH,故A錯誤;
B.NaClO具有強氧化性,能與CH3CHO發生氧化還原反應,所以不能大量共存,故B錯誤;
C.NaClO與Na2SO3發生氧化還原反應生成NaCl和硫酸鈉,其反應的離子方程式為:SO32-+ClO-=Cl-+SO42-,故C正確;
D.向該消毒液中加入濃鹽酸,反應方程式為ClO-+Cl-+2H+=Cl2↑+H2O,反應中產生1mol Cl2轉移電子1mol,即轉移電子數約為6.02×1023,故D錯誤.
故選C.
點評 本題考查了氧化還原反應、離子共存、pH試紙的使用等,側重于考查氧化還原反應以及物質氧化性的應用,題目難度中等,注意把握NaClO的性質.


科目:高中化學 來源: 題型:多選題
| A. | 淀粉(氯化鈉)滲析 | |
| B. | 硬脂酸鈉(甘油溶液)鹽析、過濾 | |
| C. | 水(雞蛋清)蒸餾 | |
| D. | 蔗糖(葡萄糖)與銀氨溶液混合水浴加熱,過濾 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸性:H4SiO4<H3PO4<H2SO4<HClO4 | B. | 堿性:Ca(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 氫化物的穩定性:SiH4>H2S>H2O>HF | D. | 原子半徑:F<O<S<Na |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
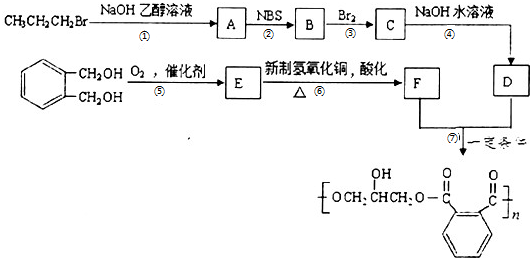
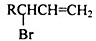
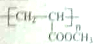 ,請設計合成路線(無機試劑及溶劑任選).注:合成路線的書寫格式參照如下示例流程圖:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
,請設計合成路線(無機試劑及溶劑任選).注:合成路線的書寫格式參照如下示例流程圖:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋼和鐵 | B. | 金剛石和石墨 | C. | 紅磷和白磷 | D. | 氧氣和臭氧 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | B |
| ①能使溴的四氯化碳溶液褪色 ②比例模型為:  ③能與水在一定條件下反應生成醇 | ①由C、H兩種元素組成 ②球棍模型為: 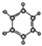 |
 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時,LiMn2O4發生氧化反應,電池內部Li+向正極移動 | |
| B. | 放電時,正極反應為:Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 醋酸可用作鋰離子電池的電解質 | |
| D. | 充電時,鋰的碳材料為陽極且反應為:Li++e-═Li |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com