
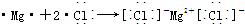 .
.分析 A、B、C、D、E為原子序數依次增大的短周期元素,A、C、F三原子最外層共有11個電子,且這三種元素的最高價氧化物對應的水化物之間兩兩皆能反應生成鹽和水,則B的最高價氧化物的水化物具有兩性,所以C為Al元素,A的最高價氧化物的水化物具有強堿性,則A是Na,根據三種元素最外層電子數知,F最外層有7個電子,則F為Cl元素,可知B為Mg,D元素的最外層電子數比次外層電子數少4,次外層有8個電子,則D元素最外層有4個電子,為Si元素,E元素原子次外層電子數比最外層電子數多3,則E元素最外層有5個電子,且E原子序數大于D,所以E為P元素,結合物質結構、性質分析解答.
解答 解:A、B、C、D、E為原子序數依次增大的短周期元素,A、C、F三原子最外層共有11個電子,且這三種元素的最高價氧化物對應的水化物之間兩兩皆能反應生成鹽和水,則B的最高價氧化物的水化物具有兩性,所以C為Al元素,A的最高價氧化物的水化物具有強堿性,則A是Na,根據三種元素最外層電子數知,F最外層有7個電子,則F為Cl元素,可知B為Mg,D元素的最外層電子數比次外層電子數少4,次外層有8個電子,則D元素最外層有4個電子,為Si元素,E元素原子次外層電子數比最外層電子數多3,則E元素最外層有5個電子,且E原子序數大于D,所以E為P元素,
(1)由以上分析可知A為Na,D為Si,E為P,故答案為:Na;Si;P;
(2)B為Mg,F為Cl,電子式表示B與F形成化合物的過程為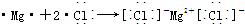 ,
,
故答案為: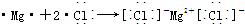 ;
;
(3)A、C兩元素的最高價氧化物對應水化物相互反應的離子方程式為Al(OH)3+OH-=AlO2-+2H2O,
故答案為:Al(OH)3+OH-=AlO2-+2H2O;
(4)D為Si,D的固態氧化物為SiO2,故答案為:SiO2.
點評 本題考查位置結構性質的相互關系及應用,為高考常見題型,正確推斷元素是解本題關鍵,熟練掌握原子結構、元素周期表結構及元素周期律內涵、元素化合物知識,注題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 綠色化學的核心是應用化學原理治理環境污染 | |
| B. | 可溶性銅鹽有毒,但在生命體中,銅是一種不可缺少的微量元素 | |
| C. | 化妝品中的“天然植物精華”在提取過程中可能用到化學中的萃取、蒸餾技術 | |
| D. | 苯是重要化工原料,被英國科學家法拉第首先發現,以煤和石油為原料通過化學變化均可得到苯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:r(D)>r(F)>r(A) | |
| B. | D與C也能形成D2C和D2C2化合物,兩種化合物中陽離子和陰離子個數比都為2:1 | |
| C. | 把2mol D的單質投入足量的水中,產生的氣體體積為22.4L | |
| D. | 由A、B、C三種元素組成的18電子微粒能發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe與稀HNO3 | B. | Na2O2與CO2 | ||
| C. | NaOH溶液與CO2 | D. | AlCl3溶液與NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
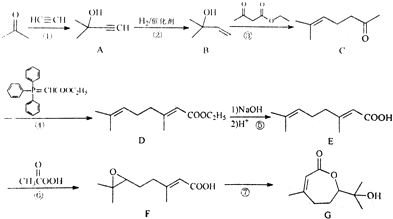
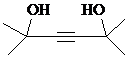 .
.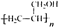 ,寫出合成流程圖(無機試劑任用).合成流程圖示例如下:
,寫出合成流程圖(無機試劑任用).合成流程圖示例如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該合金中銅與鎂的物質的量之比是2:1 | |
| B. | 可得到2.54 g沉淀 | |
| C. | 如果是銅鋁合金,則產生的NO2 的體積不會是1344mL | |
| D. | 恰好全部沉淀時,加入NaOH溶液的體積是600 mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將純水加熱到950C時,Kw變大,pH不變,水仍呈中性 | |
| B. | 向純水中加入稀氨水,平衡逆向移動,c(OH-)增大,Kw變小 | |
| C. | 向水中加入少量固體硫酸氫鈉,c(H+)增大,平衡逆向移動,KW不變 | |
| D. | 向水中通入HCl氣體,平衡逆向移動,溶液導電能力減弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18.6g | B. | 20g | C. | 19.4g | D. | 24g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com