
【題目】瓦斯中甲烷與氧氣的質量比為1∶4時極易爆炸,此時甲烷與氧氣的體積比為( )
A. 1∶4 B. 2∶1 C. 1∶1 D. 1∶2
科目:高中化學 來源: 題型:
【題目】汽車劇烈碰撞時,安全氣囊中發生反應10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化產物比還原產物多1.75 mol,則下列判斷正確的是( )
A.生成42.0 L N2(標準狀況) B.轉移電子的物質的量為1.25 mol
C.有0.250 mol KNO3被氧化 D.被氧化的N原子的物質的量為3.75 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無土栽培用的營養液,要求KCl、K2SO4和NH4Cl三種固體原料的物質的量之比為1:4:8。若配置該營養液,取428 g NH4Cl,則需KCl和K2SO4的質量分別為( )
A.53.5 g和214 g B.74.5 g和348 g
C.74.5 g和696 g D.149 g和696 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2NO(g) +O2(g)![]() 2NO2(g),其他條件相同時,分別測得NO的平衡轉化率在不同壓強(p1、p2)下隨溫度變化的曲線(如圖),下列說法不正確的是( )
2NO2(g),其他條件相同時,分別測得NO的平衡轉化率在不同壓強(p1、p2)下隨溫度變化的曲線(如圖),下列說法不正確的是( )
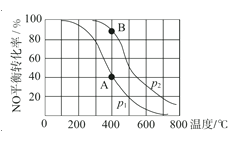
A.p1<p2
B.該反應的△H<0
C.A、B兩點的平衡常數:K(A)<K(B)
D.A、B兩點的化學反應速率:v(A)<v(B)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在體積均為1.0 L的恒容兩個密閉容器中分別 加入足量的相同的碳粉,再分別加入0.1 mol CO2和0.2 mol CO2,在不同溫度下反應CO2(g)+C(s)![]() 2CO(g)達到平衡,平衡時CO2的物質的量濃度c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上)。下列說法正確的是( )
2CO(g)達到平衡,平衡時CO2的物質的量濃度c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上)。下列說法正確的是( )
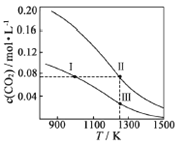
A.化學平衡常數K:K(狀態I) < K(狀態II) <K(狀態III)
B.CO2的平衡轉化率α:α(狀態I) <α(狀態Ⅱ)=α(狀態III)
C.體系中c(CO):c (CO,狀態Ⅱ) < 2c (CO,狀態Ⅲ)
D.逆反應速率v逆:v逆(狀態Ⅰ)> v逆(狀態Ⅲ)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在25 ℃的水溶液中,AgX、AgY、AgZ均難溶于水,但存在溶解平衡。當達到平衡時,溶液中離子濃度的乘積是一個常數(此常數用Ksp表示,Ksp和水的KW相似)。
如:AgX(s)![]() Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
AgY(s)![]() Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
AgZ(s)![]() Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
(1)根據以上信息,判斷AgX、AgY、AgZ三者的溶解度(用已被溶解的溶質的物質的量的濃度表示)S(AgX)、S(AgY)、S(AgZ)的大小順序為____________________________。
(2)若向AgY的飽和溶液中加入少量的AgX固體,則c(Y-)________(填“增大“減小”或“不變”)。
(3)在25 ℃時,若取0.188 g的AgY(相對分子質量為188)固體放入100 mL水中(忽略溶液體積的變化),則溶液中Y-的物質的量濃度為________。
(4)①由上述Ksp判斷,在上述(3)的體系中,能否實現AgY向AgZ的轉化,并簡述理由:________________。
②在上述(3)體系中,能否實現AgY向AgX的轉化?根據你的觀點選答一項。
若不能,請簡述理由:____________________________________。
若能,則實現轉化的必要條件是:__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各物質中,按熔點由高到低的順序排列正確的是( )
A. CH4>SiH4>GeH4>SnH4
B. KCl>NaCl>MgCl2>MgO
C. Rb>K>Na>Li
D. 石墨>金剛石>SiO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若NA表示阿伏加德羅常數,下列說法正確的是( )
A.16g氧氣和臭氧的混合物中含有的氧原子數為NA
B.標準狀況下,22.4 L水中含有的氧原子數為NA
C.0.5mol·L-1的H2SO4溶液中所含硫酸分子數目為0.5NA
D.0.1 mol 氦氣所含有的原子數為0.2NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com