
| 溫度/℃ 溶解度/g 鹽 |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | - | 88.0 |
| FeSO4?7H2O | 15.7 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | - |
| (NH4)SO4FeSO4?6H2O | 12.5 | 17.2 | 21.6 | 28.1 | 33.0 | 40.0 | - |
| 起始鐵的質量m1/g | 反應后鐵的質量m2/g | 莫爾鹽的質量 | 產率 | |
| 理論產量/g | 實際產量m3/g | |||
| 5.0 | 2.2 | c | 14.7 | d |
| m1-m2 |
| 56 |
| m1-m2 |
| 56 |
| m1-m2 |
| 56 |
| 5.0-2.2 |
| 56 |


科目:高中化學 來源: 題型:閱讀理解
| 溫度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
| 1 |
| V |
| 1 |
| V |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 溫度/℃ | 10 | 20 | 30 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 |
| FeSO4?7H2O | 20.0 | 26.5 | 32.9 |
| (NH4)2SO4?FeSO4 | 17.2 | 21.6 | 28.1 |

| 1 |
| V |
| 1 |
| V |
查看答案和解析>>
科目:高中化學 來源: 題型:
 【實驗化學】
【實驗化學】查看答案和解析>>
科目:高中化學 來源:2012年人教版高中化學選修6 3.2 物質含量的測定練習卷(解析版) 題型:填空題
硫酸亞鐵銨的化學式為(NH4)2SO4·FeSO4·6H2O,又名莫爾鹽,是分析化學中常見的還原劑。某化學研究小組設計如下實驗來制備莫爾鹽并測定硫酸亞鐵銨的純度。
步驟一:鐵屑的處理與稱量。在盛有適量鐵屑的錐形瓶中加入Na2CO3溶液,加熱、過濾、洗滌、干燥、稱量,質量記為m1。
步驟二:FeSO4的制備。將上述鐵屑加入到一定量的稀硫酸中,充分反應后過濾并用少量熱水洗滌錐形瓶和濾紙。濾液及洗滌液完全轉移至蒸發皿中。濾渣干燥后稱重,質量記為m2。
步驟三:硫酸亞鐵銨的制備。準確稱取所需質量的(NH4)2SO4加入“步驟二”中的蒸發皿中,緩緩加熱一段時間后停止,冷卻,待硫酸亞鐵銨結晶后過濾。晶體用無水乙醇洗滌并自然干燥,稱量所得晶體質量。
步驟四:用比色法測定硫酸亞鐵銨的純度。
回答下列問題:
(1)步驟三中稱取的(NH4)2SO4質量為________。
(2)①鐵屑用Na2CO3溶液處理的目的是_______________________________。
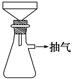
制備FeSO4溶液時,用右圖裝置趁熱過濾,原因是
_______________________________________________________________。
②將(NH4)2SO4與FeSO4混合后加熱、濃縮,停止加熱的時機是
________________________________________________________________________。
③比色法測定硫酸亞鐵銨純度的實驗步驟為:Fe3+標準色階的配制、待測硫酸亞鐵銨溶液的配制、比色測定。標準色階和待測液配制時除均需加入少量稀鹽酸外,還應注意的問題是________________________________________________________________________。
④該實驗最終通過____________________確定硫酸亞鐵銨產品等級。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com