
(12分)為研究溫度對Cl2與KOH反應的影響,設計實驗如下:
在蒸餾燒瓶中裝入足量MnO2,分液漏斗中裝足量濃鹽酸,大試管A中裝4mol/LKOH溶液15mL,并置于75℃水浴中,大試管B中裝02mol/LKOH溶液,并置于冰水中,C中裝NaOH溶液。
試回答下列問題:
(1)水浴加熱有什么優點?
(2)如何判斷A中已經反應完全?
(3)分離A中生成的兩種鹽,檢測發現其中KCl為005mol(不考慮HCl揮發),寫出A中發生的化學方程式
(4)分離B中生成的兩種鹽,其物質的量之比為1:1,寫出離子方程式。
(5)試管B要置于冰水中降溫的主要原因是:
A.從試管A中出來的氣體溫度較高,易使試管B中的溶液溫度升高
B.防止生成的鹽分解C.催化劑在冷水中活性最強
D.該反應是放熱反應,為防止溫度過高,采用降溫
(6)圖一中,分液漏斗下端連接玻璃管并伸入液面下,其作用是什么?可以用圖二代替嗎?。

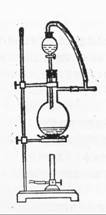
圖一 圖二
 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:
(12分)為研究溫度對Cl2與KOH反應的影響,設計實驗如下:
在蒸餾燒瓶中裝入足量MnO2,分液漏斗中裝足量濃鹽酸,大試管A中裝4mol/LKOH溶液15mL,并置于75℃水浴中,大試管B中裝02mol/LKOH溶液,并置于冰水中,C中裝NaOH溶液。
試回答下列問題:
(1)水浴加熱有什么優點?
(2)如何判斷A中已經反應完全?
(3)分離A中生成的兩種鹽,檢測發現其中KCl為005mol(不考慮HCl揮發),寫出A中發生的化學方程式
(4)分離B中生成的兩種鹽,其物質的量之比為1:1,寫出離子方程式。
(5)試管B要置于冰水中降溫的主要原因是:
A.從試管A中出來的氣體溫度較高,易使試管B中的溶液溫度升高
B.防止生成的鹽分解C.催化劑在冷水中活性最強
D.該反應是放熱反應,為防止溫度過高,采用降溫
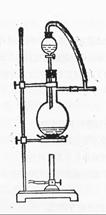
(6)圖一中,分液漏斗下端連接玻璃管并伸入液面下,其作用是什么?可以用圖二代替嗎?。
圖一 圖二
查看答案和解析>>
科目:高中化學 來源:江西省上高二中2011屆高三第二次月考化學試題 題型:實驗題
(12分)為研究溫度對Cl2與KOH反應的影響,設計實驗如下:
在蒸餾燒瓶中裝入足量MnO2,分液漏斗中裝足量濃鹽酸,大試管A中裝4mol/LKOH溶液15mL,并置于75℃水浴中,大試管B中裝02mol/LKOH溶液,并置于冰水中,C中裝NaOH溶液。
試回答下列問題:
(1)水浴加熱有什么優點?
(2)如何判斷A中已經反應完全?
(3)分離A中生成的兩種鹽,檢測發現其中KCl為005mol(不考慮HCl揮發),寫出A中發生的化學方程式
(4)分離B中生成的兩種鹽, 其物質的量之比為1:1,寫出離子方程式。
其物質的量之比為1:1,寫出離子方程式。
(5)試管B要置于冰水中降溫的主要原因是:
| A.從試管A中出來的氣體溫度較高,易使試管B中的溶液溫度升高 | |
| B.防止生成的鹽分解 | C.催化劑在冷水中活性最強 |
| D.該反應是放熱反應,為防止溫度過高,采用降溫 |
 可以用圖二代替嗎?。
可以用圖二代替嗎?。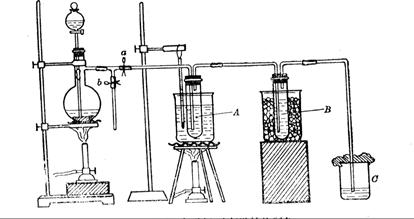
查看答案和解析>>
科目:高中化學 來源:2013屆浙江省高二下學期期中考試化學試卷(解析版) 題型:填空題
(8分)在溫度T1和T2下,X2(g)和 H2反應生成HX的平衡常數如下表:
|
化學方程式 |
K (T1 ) |
K (T2) |
|
F2+H2 |
1.8 ×1036 |
1.9 ×1032 |
|
Cl2+H2 |
9.7 ×1012 |
4.2 ×1011 |
|
Br2+H2 |
5.6 ×107 |
9.3 ×106 |
|
I2+H2 |
43 |
34 |
(1)僅依據K的變化,可以推斷出:隨著鹵素原子核電荷數的增加,_______(選填字母)
a.在相同條件下,X2的平衡轉化率逐漸降低 b. X2與H2反應的劇烈程度逐漸減弱
c. HX的穩定性逐漸減弱 d. HX的還原性逐漸減弱
(2)在容積為3L的密閉容器中,由I2(g)和H2(g)合成HI(g),在其他條件不變的情況下,研究溫度對反應的影響,HI的物質的量的變化情況如下圖所示。

①溫度為T1時,在0~tAmin內,H2的消耗速率v (H2)=__________
②分析右圖所示圖像,下列說法正確的是________(填序號)
a.溫度為T2,容器內氣體密度不變時,反應到達B點所示狀態
b.平衡狀態從A點移動到B點,n(HI)/n(H2)增大
c.該反應為放熱反應
(3)加水稀釋0.1mol·L-1的HF溶液,下列各量中增大的是________(填序號)
a.c(H+) b. Ka(HF) c. c(F-)/c(H+) d. c(H+) / c(HF)
查看答案和解析>>
科目:高中化學 來源: 題型:
為研究溫度對Cl2與KOH反應的影響,設計實驗如下:
在蒸餾燒瓶中裝入足量MnO2,分液漏斗中裝足量濃鹽酸,大試管A中裝4mol/LKOH溶液15mL,并置于75℃水浴中,大試管B中裝02mol/LKOH溶液,并置于冰水中,C中裝NaOH溶液。
試回答下列問題:
(1)水浴加熱有什么優點?![]()
(2)如何判斷A中已經反應完全?
(3)分離A中生成的兩種鹽,檢測發現其中KCl為005mol(不考慮HCl揮發),寫出A中發生的化學方程式
(4)分離B中生成的兩種鹽,![]() 其物質的量之比為1:1,寫出離子方程式。
其物質的量之比為1:1,寫出離子方程式。
(5)試管B要置于冰水中降溫的主要原因是:
A.從試管A中出來的氣體溫度較高,易使試管B中的溶液溫度升高
B.防止生成的鹽分解C.催化劑在冷水中活性最強
D.該反應是放熱反應,為防止溫度過高,采用降溫
(6)圖一中,分液漏斗下端連接玻璃管并伸入液面下,其作用是什么?![]() 可以用圖二代替嗎?。
可以用圖二代替嗎?。
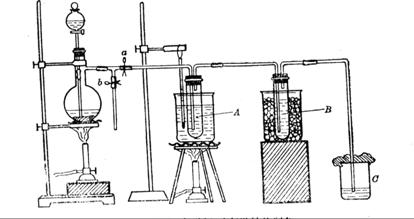
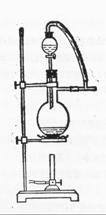
圖一 圖二
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com