
【題目】以芳香烴A為原料合成有機物F和I的合成路線如下:

(1)A的分子式為__________,C中的官能團名稱為________________。
(2)D分子中最多有______個原子共平面。
(3)E生成F的反應類型為___________,G的結構簡式為__________。
(4)由H生成I的化學方程式為______________。
(5)符合下列條件的B的同分異構體有_______種(不考慮立體異構),其中核磁共振氫譜為4組峰,且面積比為6:2:1:1的是________(寫出其中一種的結構簡式)。
①屬于芳香化合物; ②能發生銀鏡反應。
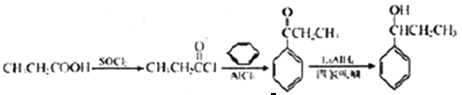
(6)已知![]() ,參照上述合成路線,以苯和丙酸為原料(無機試劑任選),設計制備
,參照上述合成路線,以苯和丙酸為原料(無機試劑任選),設計制備![]() 的合成路線________________。
的合成路線________________。
【答案】 C7H8 羥基 17 消去反應 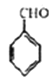
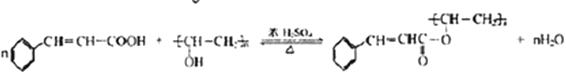 14
14 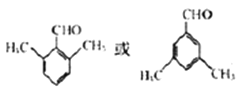
【解析】試題以甲苯的兩種重要工業應用流程為基礎,考查官能團、有機分子的空間結構、有機反應類型、有機反應原理、有機物結構的測定方法、同分異構體、有機合成路徑的設計等知識,考查考生對有機流程的分析能力和對有機化合物知識的綜合應用能力。
解析:首先對已知流程進行分析。芳香烴A與![]() 反應生成
反應生成![]() ,則A為甲苯(
,則A為甲苯(![]() ),B分子中羰基一定條件下被還原生成C,通過C轉變成D的條件可以知道,C在此過程中發生的是消去反應,所以生成的D為
),B分子中羰基一定條件下被還原生成C,通過C轉變成D的條件可以知道,C在此過程中發生的是消去反應,所以生成的D為![]() ,E為
,E為![]() ,“KOH/乙醇/△”是鹵代烴消去反應的條件,所以E→F是消去反應。下方流程中,甲苯生成G是氧化反應,產物G是
,“KOH/乙醇/△”是鹵代烴消去反應的條件,所以E→F是消去反應。下方流程中,甲苯生成G是氧化反應,產物G是![]() 。從H生成I已有結構可知H為
。從H生成I已有結構可知H為![]() 。 (1)A是甲苯,C分子中的官能團是羥基。答案:C7H8、羥基。(2)D是
。 (1)A是甲苯,C分子中的官能團是羥基。答案:C7H8、羥基。(2)D是![]() ,分子中“苯結構”(有2個H原子被C替換)中的12個原子共面,右側“乙烯結構”(有1個H原子被苯環的C替換)中的6個原子共面,這兩個平面共用兩個C原子但不一定是同一個平面,左側的甲基4個原子呈三角錐形不共面,但是最多可能有1個H原子恰好存在于苯環平面,所以該分子中共面的原子最多1+12+6-2=17。答案:17。(3)根據反應條件判斷E→F是消去反應,G是苯甲醛。答案:消去反應、
,分子中“苯結構”(有2個H原子被C替換)中的12個原子共面,右側“乙烯結構”(有1個H原子被苯環的C替換)中的6個原子共面,這兩個平面共用兩個C原子但不一定是同一個平面,左側的甲基4個原子呈三角錐形不共面,但是最多可能有1個H原子恰好存在于苯環平面,所以該分子中共面的原子最多1+12+6-2=17。答案:17。(3)根據反應條件判斷E→F是消去反應,G是苯甲醛。答案:消去反應、![]() 。(4)H是
。(4)H是![]() ,通過酯化反應生成I。答案:
,通過酯化反應生成I。答案: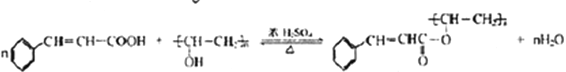 。(5)B分子式為C9H10O,不飽和度為5,由條件①可知同分異構體結構中含有苯環,條件②說明同分異構體結構中含有—CHO,除此之外,還有2個C原子且通過單鍵連接在分子中,這2個C原子可能全部或部分與醛基連接后連接在苯環上,也可能組合或單獨連接在苯環上。根據這2個C原子上述不同方式的連接,部分同分異構體羅列如下:
。(5)B分子式為C9H10O,不飽和度為5,由條件①可知同分異構體結構中含有苯環,條件②說明同分異構體結構中含有—CHO,除此之外,還有2個C原子且通過單鍵連接在分子中,這2個C原子可能全部或部分與醛基連接后連接在苯環上,也可能組合或單獨連接在苯環上。根據這2個C原子上述不同方式的連接,部分同分異構體羅列如下: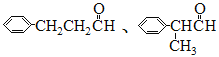 、
、![]() (存在苯環上鄰、間、對共3種異構)、
(存在苯環上鄰、間、對共3種異構)、![]() (存在苯環上鄰、間、對共3種異構)、
(存在苯環上鄰、間、對共3種異構)、![]() (存在苯環上位置不同的6種異構),共計14種。核磁共振氫譜是研究化學環境不同H原子的譜圖,其面積比表示不同化學環境H原子數目比值,例如
(存在苯環上位置不同的6種異構),共計14種。核磁共振氫譜是研究化學環境不同H原子的譜圖,其面積比表示不同化學環境H原子數目比值,例如![]() 存在5種化學環境不同的H原子,數目比(譜圖中面積比)為3:2:2:2:1,結合上述14種同分異構體分子結構,滿足條件的是
存在5種化學環境不同的H原子,數目比(譜圖中面積比)為3:2:2:2:1,結合上述14種同分異構體分子結構,滿足條件的是![]() 或
或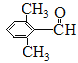 。答案:14、
。答案:14、![]() 或
或 。
。
(6)兩個有機分子通過碳碳鍵連接形成一個分子的方案只能參照已知中A→B完成,因此先要得到![]() ,已知中提供了由—COOH得到—COCl的方法。參照已知中A→B,
,已知中提供了由—COOH得到—COCl的方法。參照已知中A→B,![]() 與苯發生取代反應生成
與苯發生取代反應生成![]() ,再用已知中B→C的方法還原
,再用已知中B→C的方法還原![]() 既可得到需要的產物。
既可得到需要的產物。
答案: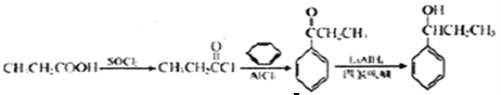 。
。


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
【題目】某原電池,兩電極一為碳棒,一為鐵片,若電流表的指針發生偏轉,且a極上有大量氣泡生成,則以下敘述正確的是

A.a為負極,是鐵片,燒杯中的溶液為硫酸
B.a為負極,是鐵片,燒杯中的溶液為硫酸銅溶液
C.a為正極,是碳棒,燒杯中的溶液為硫酸
D.b為正極,是碳棒,燒杯中的溶液為硫酸銅溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】奧運五環代表著全世界五大洲的人民團結在一起。下列各項中的物質,能滿足如圖中陰影部分關系的是( )

① | ② | ③ | ④ | |
A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
B | Na2SO4 | K2SO4 | KCl | NH4Cl |
C | NaCl | K2SO4 | KCl | NH4Cl |
D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯氧布洛芬鈣G是評價較好的解熱、鎮痛、消炎藥,下面是它的一種合成路線(具體反應條件和部分試劑略)

已知:
①氯化亞砜(SOCl2)可與醇發生反應,醇的羥基被氯原子取代而生成氯代烴。
② (X表示鹵素原子)
(X表示鹵素原子)
回答下列問題:
(1)寫出D的結構簡式:________________。F 中所含的官能團名稱是___________。
(2)B→C的反應類型是_______________;D→E的反應類型是_______________。
(3)寫出F和C在濃硫酸條件下反應的化學方程式__________________________。
(4)寫出A的符合以下條件同分異構體的所有結構簡式______________________。
①屬于苯的二取代物;
②苯環上核磁共振氫譜圖中共有2個吸收峰
③與FeCl3溶液發生顯色反應。
(5)結合上述推斷及所學知識,參照上述合成路線任選無機試劑設計合理的方案,以苯甲醇(![]() )為原料合成苯乙酸苯甲酯(
)為原料合成苯乙酸苯甲酯(![]() )寫出合成路線,并注明反應條件_________________。
)寫出合成路線,并注明反應條件_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(化學:選修5:有機化學基礎)以有機物A制備高分子化合物F( )的流程如下:
)的流程如下:

請回答下列問題。
(1)A的官能團名稱是_______;C的系統命名是____________。
(2)①的反應類型是_______,⑤的反應類型是___________。
(3)寫出反應③的化學方程式:______________________。
(4)滿足下列條件的B同分異構體有____種。
Ⅰ.能與Na反應產生氣體 Ⅱ.能與NaOH 反應 Ⅲ.不能與Na2CO3反應。
若與NaOH溶液反應的有機物中的碳原子數目為2,則其結構簡式是__________。
(5)已知:
Ⅰ. ![]()
Ⅱ. 
寫出以CH2=CHCH=CH2為原料制備C的合成路線流程圖(無機試劑可以任選):__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,通過下列反應可以制備特種陶瓷的原料MgO: MgSO4(s)+CO(g) ![]() MgO(s)+CO2(g)+SO2(g) △H >0,該反應在某密閉容器中達到平衡。下列分析正確的是
MgO(s)+CO2(g)+SO2(g) △H >0,該反應在某密閉容器中達到平衡。下列分析正確的是
A. 恒溫恒容時,充入CO氣體,達到新平衡時![]() 增大
增大
B. 容積不變時,升高溫度,混合氣體的平均相對分子質量減小
C. 恒溫恒容時,分離出部分SO2氣體可提高MgSO4的轉化率
D. 恒溫時,增大壓強平衡逆向移動,平衡常數減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H、N、O、Na、S、Cl都是中學化學中的常見元素,根據題意回答與這些元素有關的問題:
(1)畫出Na原子結構示意圖_______,Na2O2可用作供氧劑,其電子式為_______。
(2)Cl2是一種大氣污染物,裝有液氯的鋼瓶上應貼的標簽是_______(填編號)。

氯氣泄漏可用NaHSO3溶液來處理,寫出相關的離子反應方程式_____________。
(3)25C時,利用pH試紙測得0.1mol/L氨水的pH約為11,則可以估算出氨水的電離常數約為_____;向10mL此溶液中通入少量氨氣,忽略溶解過程中溶液溫度和體積的微小變化,溶液中![]() 將_______(填“增大” “減小”或“無法確定”)。
將_______(填“增大” “減小”或“無法確定”)。
(4)有兩種化合物同時含有上述六元素中的四種元素。將這兩種化合物的溶液混合后,恰好完全反應,生成物之一M仍含有這四種元素,該反應的離子方程式為______________。若M溶液的pH =5,則由水電離出的c(H+)=_______mol/L,該溶液離子濃度由大到小的順序為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1 L某混合溶液中,溶質X、Y濃度都為0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物質的量如圖所示,則X、Y、Z分別是

A. 氯化鋁、氯化鎂、氫氧化鈉B. 偏鋁酸鈉、氫氧化鋇、硫酸
C. 氯化鋁、氯化鐵、氫氧化鈉D. 偏鋁酸鈉、氯化鋇、硫酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某廢渣中含有Al 2O3和Cr2O3(三氧化二鉻),再次回收利用工藝流程如下。

回答下列問題:
(1)濾液1中陰離子為CrO42-和AlO2-,X的電子式是_______。寫出濾液1與過量氣體X反應生成Al(OH) 3的離子方程式:_____________________。
(2)“熔燒”中反應之一是4Na2CO3+ 2Cr2O3+ 3O2 =4Na2CrO4+ 4X,該反應中被氧化的物質是______(填化學式);若該反應轉移6mol電子,則生成_____mol Na2CrO4。
(3)“還原””中加入適量稀硫酸,調節pH=5,氧化產物為SO42-。寫出離子方程式____________。
(4)已知該廢料中含鉻元素質量分數為a%,wt這樣廢料經上述流程提取mkgCr2O3。則該廢料中鉻元素回收率為_______(用代數式表示)。(已知回收率等于實際回收質量與理論質量之比)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com