
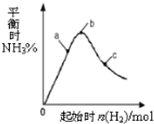
 在300℃時,改變起始反應物中n(H2)對反應N2(g)+3H2(g)?2NH3(g)+Q(Q>0)的影響如圖所示.下列說法正確的是( )
在300℃時,改變起始反應物中n(H2)對反應N2(g)+3H2(g)?2NH3(g)+Q(Q>0)的影響如圖所示.下列說法正確的是( )

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:閱讀理解
| 時間/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
化學在能源開發與利用中起著十分關鍵的作用。
(1)蘊藏在海底的“可燃冰”是高壓下形成的外觀像冰的甲烷水合物固體。甲烷氣體燃燒的熱化學方程式為:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol。
356g“可燃冰”(分子式為CH4·9H2O)釋放的甲烷氣體完全燃燒生成液態水.放出的熱量為 _______ 。
(2)某種燃料電池,一個電極通入空氣,另一電極通入液化石油氣(以C4H10表示),電池的電解質是摻入了Y2O3的ZrO2晶體,它在高溫下傳導O2-。
已知該電池負極的電極反應為:C4H10+2O2--4e-=CO2+H2O,則該電池正極的電極反應式為 _______ ,電池工作時,固體電解質里的O2-向 _______ 極移動。
![]() (3)已知一氧化碳與水蒸氣的反應為:CO(g)+H2O(g) CO2(g)+H2(g)
(3)已知一氧化碳與水蒸氣的反應為:CO(g)+H2O(g) CO2(g)+H2(g)
①T℃時,在一定體積的容器中,通入一定量的CO(g)和H2O(g),發生反應并保持溫度不變,各物質濃度隨時間變化如下表: T℃時物質的濃度(mol/L)變化
| 時間 / min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
第5、6min時的數據是保持溫度和體積不變時,改變某一條件后測得的。第4~5min之間,改變的條件是 _______ ,第5~6min之間,改變的條件是 _______ 。T℃時該化 學反應的平衡常數是 _______ 。
②已知420℃時,該化學反應的平衡常數為9。如果反應開始時,CO和H2O(g)的濃度都是0.01 mol/L,則CO在此條件下的轉化率為 _______ 。
③397℃時該反應的平衡常數為12,請判斷該反應的△H _______ 0(填“>”、“=”、“<”).
查看答案和解析>>
科目:高中化學 來源:2010-2011學年江蘇省海門市高二下學期期末教學質量調研化學試題 題型:實驗題
二氯化二硫(S2Cl2)是一種重要的化工原料,常用作橡膠硫化劑,改變生橡膠受熱發粘、遇冷變硬的性質。查閱資料可知S2Cl2具有下列性質:
| 物理性質 | 色態 | 揮發性 | 熔點 | 沸點 |
| 金黃色液體 | 易揮發 | -76℃ | 138℃ | |
| 化學性質 | 300 ℃以上完全分解 | |||
S2Cl2+Cl2 2SCl2 2SCl2 | ||||
| 遇水反應生成SO2、S等產物 | ||||
查看答案和解析>>
科目:高中化學 來源:2012-2013學年云南省昆明三中、滇池中學高二下學期期末考試化學卷(帶解析) 題型:填空題
(1)O3在水中易分解,一定條件下,O3的濃度減少一半所需的時間(t)如下表所示。
①pH增大能加速O3分解,表明對O3分解起催化作用的是_________________。
②據表中的遞變規律,推測O3在下列條件下分解速率依次增大的順序為________(填代號)
a. 40°C、pH=3.0 b. 10°C、pH=4.0 c. 30°C、pH=7.0
(2)向一容積為2升的密閉容器中充入2molA、0.6molC和一定量的B三種氣體,一定條件下發生某種反應。現有兩個圖像分別對該反應的情況進行描述:
圖1表示各物質的濃度隨時間的變化情況,其中t0~t1階段c(B)未畫出;
圖2為反應體系中反應速率隨時間變化的情況,且t2、t3、t4各改變一種不同的條件(其中t2改變的條件是加入某種催化劑);(說明:圖1中實線表示反應進程)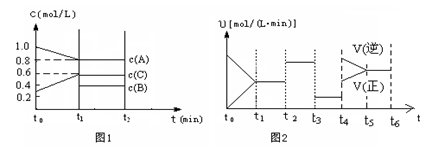
①你認為t3時改變的條件是 (填寫“加壓”或“減壓”),B的起始物質的量為 mol;
②各階段平衡時對應的平衡常數如下表所示:
| 時間段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常數 | K1 | K2 | K3 | K4 |
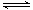 CH3OH(g)反應合成甲醇。
CH3OH(g)反應合成甲醇。| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
科目:高中化學 來源:2012屆江蘇省海門市高二下學期期末教學質量調研化學試題 題型:實驗題
二氯化二硫(S2Cl2)是一種重要的化工原料,常用作橡膠硫化劑,改變生橡膠受熱發粘、遇冷變硬的性質。查閱資料可知S2Cl2具有下列性質:
|
物理性質 |
色態 |
揮發性 |
熔點 |
沸點 |
|
金黃色液體 |
易揮發 |
-76℃ |
138℃ |
|
|
化學性質 |
300 ℃以上完全分解 |
|||
|
S2Cl2+Cl2 |
||||
|
遇水反應生成SO2、S等產物 |
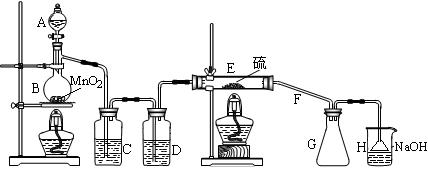
向熔融的硫中通以干燥、純凈的C12即可生成S2C12。下圖是實驗室制備S2Cl2的裝置。

(1)儀器A的名稱是 ,導管F除導氣外還起的作用是 ;
(2)B中反應的離子方程式為 ;
(3)開始實驗,打開分液漏斗的活塞,發現濃鹽酸流出少量后即難以下滴,經檢查分
液漏斗活塞沒有堵塞,你認為應采取的措施是 ;
(4)裝置C中的試劑是 ;如果缺少D裝置,則對實驗的影響是(用化學方程式表示) ;
(5)如果在加熱E時溫度過高,對實驗結果的影響是 ;為了提高S2C12的純度,關鍵的操作是控制好溫度和 。
(6)設計裝置H的目的是 ;燒杯中發生反應的離子方程式
是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com