
【題目】(1)一杯咖啡中含有0.194g咖啡因(分子式C8H10N4O2,M=194g/mol),你知道其中有_______個咖啡因分子;這些咖啡因分子中的N原子的物質的量為_________.
(2)經檢測一瓶泉水樣品,1.0L樣品中含4.8×10﹣2g Mg2+,那么該泉水中Mg2+的物質的量濃度為____________.含1.0mol Mg的這種泉水的體積是_________L.
(3)0.2mol H2S,在標準狀況下的體積約為_______L;相同質量的CH4和H2S中分子個數比為____________.
【答案】0.001NA 0.004mol 0.002mol/L 500L 4.48L 17:8
【解析】
根據物質的量與質量、氣體體積、物質的量濃度等物理量的關系分析解答。
(1)0.194g咖啡因的物質的量為:![]() ,含有咖啡因分子的數目為0.001NA;咖啡因的分子式為C8H10N4O2,每個咖啡因分子中含有4個N反應中,則該咖啡因分子中含有N的物質的量為:0.001mol×4=0.004mol,故答案為:0.001NA;0.004mol;
,含有咖啡因分子的數目為0.001NA;咖啡因的分子式為C8H10N4O2,每個咖啡因分子中含有4個N反應中,則該咖啡因分子中含有N的物質的量為:0.001mol×4=0.004mol,故答案為:0.001NA;0.004mol;
(2)4.8×10-2g![]() ,Mg2+的物質的量為:
,Mg2+的物質的量為:![]() ;含1.0mol Mg2+的這種泉水的體積為:
;含1.0mol Mg2+的這種泉水的體積為:![]() ;故答案為:0.002mol/L;500L;
;故答案為:0.002mol/L;500L;
(3)標準狀況下0.2molH2S的體積為:22.4L/mol×0.2mol=4.48L;相同質量的CH4和H2S的物質的量與摩爾質量成反比,則其分子個數比=物質的量之比=34g/mol:16g/mol=17:8;故答案為:4.48L;17:8。


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:
【題目】金屬鉬(![]() )在工業和國防建設中有重要的作用。鉬的常見化合價為
)在工業和國防建設中有重要的作用。鉬的常見化合價為![]() 。由鉬精礦(主要成分是
。由鉬精礦(主要成分是![]() )制備單質鉬和鉬酸鈉晶體(
)制備單質鉬和鉬酸鈉晶體(![]() ),部分流程如下圖所示:
),部分流程如下圖所示:
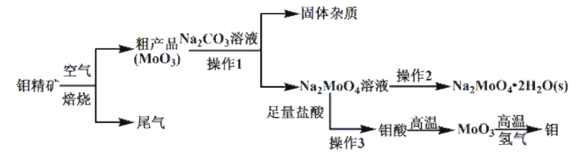
已知:鉬酸微溶于水,可溶于堿溶液。
回答下列問題:
(1)鉬精礦在空氣中焙燒時,發生的主要方程式為_______________________。
(2)鉬精礦焙燒時排放的尾氣對環境會產生危害,請你提出一種實驗室除去該尾氣的方法________________________。
(3)操作2的名稱為_________________________________。
(4)實驗室由鉬酸經高溫制![]() ,所用到的硅酸鹽材料儀器的名稱是____________________________。
,所用到的硅酸鹽材料儀器的名稱是____________________________。
(5)操作1中,加入碳酸鈉溶液充分反應后,堿浸液中![]() 、
、![]() ,在結晶前需加入
,在結晶前需加入![]() 固體以除去溶液中的
固體以除去溶液中的![]() 。當
。當![]() 開始沉淀時,
開始沉淀時,![]() 的去除率是_________。[
的去除率是_________。[![]() 、
、![]() ,溶液體積變化可忽略不計]
,溶液體積變化可忽略不計]
(6)焙燒鉬精礦所用的裝置是多層焙燒爐,圖2為各爐層固體物料的物質的量的百分數(![]() )。
)。
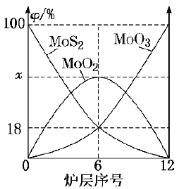
①![]() ___________。
___________。
②焙燒爐中也會發生![]() 與
與![]() 反應生成
反應生成![]() 和
和![]() ,還原劑為_________。若反應中轉移
,還原劑為_________。若反應中轉移![]() ,則消耗的還原劑的物質的量為______________。
,則消耗的還原劑的物質的量為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高氯酸銨是一種常見的強氧化劑,常用作火箭發射的推進劑。根據下列信息回答問題:
已知:①高氯酸銨受熱分解為N2、Cl2、O2和H2O;②Mg3N2易水解;③Cu與N2在酒精燈加熱條件下不反應。
(1)寫出高氯酸銨受熱分解的化學反應方程式: _____________,Mg3N2的電子式為________。
(2)現有23.5g NH4ClO4分解,用下列裝置設計實驗,驗證其分解產物并計算分解率。(注:①裝置中空氣已除盡;②裝置可重復使用;③B~F裝置中的試劑均過量且能與相應物質反應完全。)
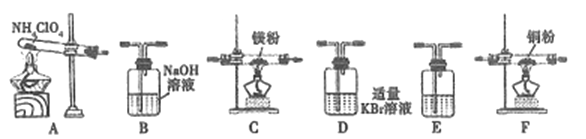
①用E裝置質量的增加來驗證生成的氣體產物之一,則E中盛放的試劑是:_______。
②請按氣流由左至右的方向連接裝置:A →E→D →B→______→_____→_______→E (選擇B~F裝置,并用B~F字母填空)。
③證明產物中有Cl2的實驗現象:________。
④反應結束后,若C裝置質量增加了2.38g,則NH4ClO4的分解率是:________%。
(3)樣品中NH4ClO4的含量(雜質中不含NH4+)還可用蒸餾法測定(如圖所示,加熱和夾持裝置已略去),實驗步驟如下:

步驟1:組裝儀器,檢查氣密性;準確稱取樣品a g(不超過0.5g)于蒸餾燒瓶中,加入約150mL水溶解。
步驟2:準確量取40.00mL 約0.1mol/L H2SO4于錐形瓶中。
步驟3:向蒸餾燒瓶中加入20mL 3mol/L NaOH溶液;加熱蒸餾使NH3全部揮發。
步驟4:用新煮沸過的水沖洗冷凝裝置2~3次,洗滌液并入錐形瓶中。
步驟5:向錐形瓶中加2~3滴甲基橙,用c mol/L NaOH標準溶液滴定至終點,消耗NaOH標準溶液V1 mL。
步驟6:重復實驗2~3次。
回答下列問題:
①步驟2中,準確量取40.00ml H2SO4 溶液的玻璃儀器是: __________。
②為獲得樣品中NH4ClO4的含量,還需補充的實驗是:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋇在氧氣中燃燒時得到一種鋇的氧化物晶體,其晶胞的結構如圖所示,下列有關說法中正確的是
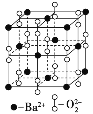
A. 該晶體屬于離子晶體
B. 晶體的化學式為Ba2O2
C. 該晶體的晶胞結構與CsCl相似
D. 與每個Ba2+距離相等且最近的Ba2+共有12個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列鹵代烴在KOH醇溶液中加熱不發生消去反應的是( )
①![]() ②
②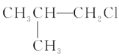 ③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤
③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A.①③⑥B.②③⑤C.全部D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為流動電池,其電解質溶液可在電池外部流動,調節電解質,可維持電池內部電解質溶液濃度穩定。下列關于該電池的說法錯誤的是
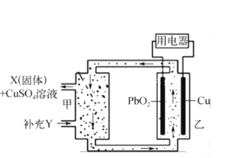
A.Cu為該電池的負極
B.X為PbSO4,Y為H2SO4
C.當消耗1 mol PbO2,需分離出320 g CuSO4
D.PbO2電極反應式為PbO2+4H+ + SO42- +2e-=PbSO4+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞甲基藍(Methylnene Blue)在堿性條件下與葡萄糖作用生成亞甲基白(Methylene White),亞甲基藍的結構簡式:
著名的藍瓶子實驗操作步驟如下:
①如圖示在250mL錐形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,攪拌溶解后,再加入3滴~5滴0.2%的亞甲基藍溶液,振蕩混合液呈現藍色;
②塞緊橡皮塞(活塞a、b關閉),將溶液靜置,溶液變為無色;
③再打開瓶塞,振蕩,溶液又變為藍色;
④再塞緊橡皮塞,將溶液靜置,溶液又變為無色,以上③、④可重復多次。
試回答下列問題:

(1)某學生將起初配得的藍色溶液分裝在A,B兩支試管中(如上圖,A試管充滿溶液,B中有少量溶液),塞上橡皮塞靜置片刻,兩溶液均顯無色,若再同時振蕩A,B試管,能顯藍色的是_________(填“A”或“B”);
(2)若塞緊錐形瓶塞并打開活塞a、b,通入足量氫氣后,再關閉活塞a、b并振蕩,溶液能否由無色變為藍色_________(填“能”或“不能”);若塞緊錐形瓶塞并打開a、b通入足量氧氣,溶液能否由無色變為藍色_________(填“能”或“不能”);
(3)上述轉化過程中,葡萄糖的作用是_________,亞甲基藍的作用是_________;
(4)上述實驗中葡萄糖也可用鮮橙汁(其中含豐富維生素C)代替,這是因為維生素C具有_____;
(5)該實驗中③、④操作能否無限次重復進行_________(填“能”或“不能”),理由是 _____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將等物質的量的A、B混合于2 L的密閉容器中,發生下列反應2A(g) + B(g) ![]() xC(g) + 2D(g),經4min后達平衡,測得D的濃度為1.0 mol·L-1,c(A) : c(B)=2 : 3,以C表示的平均速率υ(C)=0.125 mol·L-1·min-1,下列說法不正確的是
xC(g) + 2D(g),經4min后達平衡,測得D的濃度為1.0 mol·L-1,c(A) : c(B)=2 : 3,以C表示的平均速率υ(C)=0.125 mol·L-1·min-1,下列說法不正確的是
A. 反應速率υ(A)=0.25 mol·L-1·min-1
B. 該反應方程式中,x=1
C. 4 min時,B的物質的量為2 mol
D. 該反應的平衡常數K=1/3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】O3是一種常見的綠色氧化劑,可由臭氧發生器(原理如圖)電解稀硫酸制得。下列說法錯誤的是( )
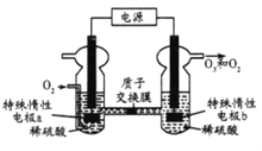
A.電極a為陰極
B.a極的電極反應為O2+4H++4e-═2H2O
C.電解一段時間后b極周圍的pH上升
D.標準狀況下,當有5.6LO2反應時,收集到O2和O3混合氣體4.48L,O3的體積分數為80%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com