
分析 根據原子半徑D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相對位置為: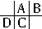 ,C的原子核內的質子數等于A、B原子核內的質子數之和,C質子數等于A+8,故B為8號元素氧;因A、C為主族元素,且C最外層電子數為D的4倍,則D最外層電子數只能為1,故D為鈉、C為硅、A為碳,據此進行解答.
,C的原子核內的質子數等于A、B原子核內的質子數之和,C質子數等于A+8,故B為8號元素氧;因A、C為主族元素,且C最外層電子數為D的4倍,則D最外層電子數只能為1,故D為鈉、C為硅、A為碳,據此進行解答.
解答 解:根據原子半徑D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相對位置為: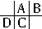 ,C的原子核內的質子數等于A、B原子核內的質子數之和,C質子數等于A+8,故B為8號元素氧.因A、C為主族元素,且C最外層電子數為D的4倍,則D最外層電子數只能為1,故D為鈉,C為硅,A為碳,
,C的原子核內的質子數等于A、B原子核內的質子數之和,C質子數等于A+8,故B為8號元素氧.因A、C為主族元素,且C最外層電子數為D的4倍,則D最外層電子數只能為1,故D為鈉,C為硅,A為碳,
(1)由上述分析可知,A、B、C、D的元素符號分別是C、O、Si、Na,
故答案為:C;O;Si;Na;
(2)D單質為金屬鈉,B單質為氧氣,鈉在氧氣中燃燒生成過氧化鈉,反應的化學方程式為:2Na+O2$\frac{\underline{\;點燃\;}}{\;}$Na2O2,
故答案為:2Na+O2$\frac{\underline{\;點燃\;}}{\;}$Na2O2;
(3)A為C、C為Si元素,非金屬性:C>Si,則最高價氧化物對應水合物的酸性強弱為:H2CO3>H2SiO3,
故答案為:H2CO3>H2SiO3.
點評 本題考查元素位置結構性質的關系應用,題目難度中等,推斷元素種類為解答關鍵,注意熟練掌握原子結構與元素周期律、元素周期表的關系,試題培養了學生的分析能力及靈活應用基礎知識的能力.


 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:推斷題
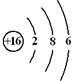 ,電子式表示化合物 C2D 的形成過程
,電子式表示化合物 C2D 的形成過程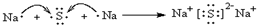 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 (1)分別取等物質的量的金屬鈉、鐵、鋁與足量的鹽酸反應,在相同條件下產生氫氣的體積比是1:2:3.
(1)分別取等物質的量的金屬鈉、鐵、鋁與足量的鹽酸反應,在相同條件下產生氫氣的體積比是1:2:3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①中有機物均可以發生還原反應 | |
| B. | ②中有機物可用飽和Na2CO3溶液鑒別 | |
| C. | ③中有機物均可以發生水解反應 | |
| D. | ③中有機物均屬于高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
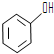 和
和 ,應選用a(填字母).
,應選用a(填字母).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若混合溶液的pH=7,則 c1V1>c2V2 | |
| B. | 若V1=V2、c1=c2,則混合溶液中 c(Na+)=c(Ac-) | |
| C. | 若V1=V2,且混合溶液的pH>7,則一定有 c1>c2 | |
| D. | 若混合溶液的pH=7,則混合溶液中 c(Na+)=c(Ac-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com