
分析 (1)首先計算氧氣的物質的量,根據方程式計算CaO2的物質的量;
(2)根據CaCO3沉淀的質量可得樣品中Ca元素的質量,根據Ca元素質量守恒計算CaO的質量,總質量減去CaO2和CaO的質量即得水的質量,進而計算H2O和CaO2的物質的量比值,即可得到x的值.
解答 解:(1)n(O2)=$\frac{0.0672L}{22.4L/mol}$=0.003mol,
2(CaO2•xH2O)$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑+2xH2O
2mol 1mol
n(CaO2•xH2O) 0.003mol
n(CaO2•xH2O)=0.006mol,
則n(CaO2)=n(CaO2•xH2O)=0.006mol,
故答案為:0.006mol;
(2)n(CaCO3)=$\frac{0.70g}{100g/mol}$=0.007mol,
①樣品中水的質量為:m(H2O)=0.542g-m(CaO2)-m(CaO)=0.542g-0.006mol×72g/mol-0.056g=0.054g,n(H2O)=$\frac{0.054g}{18g/mol}$=0.003mol,
x=$\frac{n({H}_{2}O)}{n(Ca{O}_{2})}$=$\frac{0.003mol}{0.006mol}$=0.5,
n(H2O)=$\frac{0.054g}{18g/mol}$=0.003mol,
x=$\frac{n({H}_{2}O)}{n(Ca{O}_{2})}$=$\frac{0.003mol}{0.006mol}$=0.5,
答:樣品中CaO2•xH2O的x值為0.5;
②根據Ca元素守恒,可知:n(CaO)=0.007mol-0.006mol=0.001mol,
所以樣品的組成為:CaO•6CaO2•3H2O,
故答案為:CaO•6CaO2•3H2O.
點評 本題考查混合物的計算,題目難度中等,注意根據反應的化學方程式,從質量守恒的角度計算.


科目:高中化學 來源: 題型:填空題
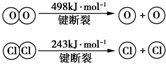 用Cl2生產某些含氯有機物時會產生副產物HCl.利用反應A,可實現氯的循環利用.反應A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反應A中,4mol HCl被氧化,放出115.6kJ的熱量.
用Cl2生產某些含氯有機物時會產生副產物HCl.利用反應A,可實現氯的循環利用.反應A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反應A中,4mol HCl被氧化,放出115.6kJ的熱量.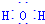 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | PH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | 由水電離出的C(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 無色溶液中:Cu2+、Al3+、NH4+、Cl- | |
| D. | 0.1 mol•L-1FeCl3溶液中:Fe2+、NH4+、AlO2-、S2- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗編號 | 溫度/℃ | H2O2濃度/% | 其它試劑 | 實驗目的 |
| ① | 20 | 5 | 無 | (Ⅰ)實驗①和②探究催化劑對H2O2分解速率的影響; (Ⅱ)實驗②和③探究溫度對該反應速率的影響; (Ⅲ)實驗②和④探究H2O2濃度對該反應速率的影響. |
| ② | 20 | 5 | FeCl3 溶液 | |
| ③ | ||||
| ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
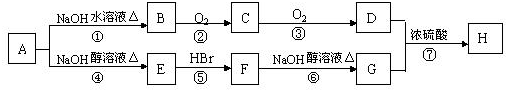
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+ | B. | SO42- | C. | S 2- | D. | NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2的電子式: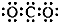 | |
| B. | 質量數為37的氯原子:${\;}_{37}^{17}$Cl | |
| C. | NH4Cl的電子式: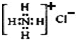 | |
| D. | 原子核內有10個中子的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用96%的工業酒精制取無水乙醇,可采用的方法是加生石灰,再蒸餾 | |
| B. | 在組裝蒸餾裝置時,溫度計的水銀球應伸入液面下 | |
| C. | 在苯甲酸重結晶實驗中,粗苯甲酸加熱溶解后還要加少量蒸餾水 | |
| D. | 在苯甲酸重結晶實驗中,待粗苯甲酸完全溶解后要冷卻到常溫才過濾 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
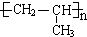 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com