
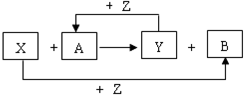
 X、Y、Z為常見的三種單質,Z是綠色植物光合作用的產物之一,A、B為常見化合物.它們在一定條件下可發生如圖所示的反應(均是在非溶液中進行的反應):
X、Y、Z為常見的三種單質,Z是綠色植物光合作用的產物之一,A、B為常見化合物.它們在一定條件下可發生如圖所示的反應(均是在非溶液中進行的反應):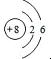 ;
; 或
或 ;
;分析 X、Y、Z為常見的三種單質,Z是綠色植物光合作用的產物之一,故Z為O2,由Y+Z→A可知A為氧化物,X+Z→B可知B為氧化物,由轉化關系X+A→Y+B為:單質(X)+氧化物(A)→單質(Y)+氧化物(B),符合置換反應,單質X具有還原性,結合常見單質解答,
(1)Z是綠色植物光合作用的產物之一為氧氣,氧原子的核內質子數為8,核外有2個電子層,第一層上有2個電子,第二層上有6個電子
(2)當X為金屬,Y為非金屬時,當X為金屬,Y為非金屬時,X為Mg或Fe,A為CO2或H2O,Y為C或H2,B為MgO或Fe3O4,符合轉化關系;
(3)當X為非金屬,Y為金屬時,X為H2或C,Y為CuO等,符合轉化關系;
(4)當X與Y均為金屬時,考慮鋁熱反應,A為Al,B為Fe3O4(或Fe2O3),符合轉化關系;
(5)當X與Y均為非金屬時,若X與Y同主族,X為C單質,B為SiO2,符合轉化關系;
若X與Y不在同一主族,X為C單質,B為H2O,符合轉化關系.
解答 解:X、Y、Z為常見的三種單質,Z是綠色植物光合作用的產物之一,故Z為O2,由Y+Z→A可知A為氧化物,X+Z→B可知B為氧化物,由轉化關系X+A→Y+B為:單質(X)+氧化物(A)→單質(Y)+氧化物(B),符合置換反應,單質X具有還原性,
(1)Z是綠色植物光合作用的產物之一為氧氣,氧原子的核內質子數為8,核外有2個電子層,第一層上有2個電子,第二層上有6個電子,其原子結構示意圖為:
故答案為: ;
;
(2)當X為金屬,Y為非金屬時,X為Mg或Fe,A為CO2或H2O,Y為C或H2,B為MgO或Fe3O4,符合轉化關系,發生反應為2Mg+CO2,$\frac{\underline{\;點燃\;}}{\;}$C+2MgO,3Fe+4H2O$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2,A的電子式為:二氧化碳為直線型結構,分子中存在兩個碳氧雙鍵,二氧化碳的電子式為: ,水中存在兩個氧氫鍵,氧原子最外層達到8電子穩定結構,水的電子式為:
,水中存在兩個氧氫鍵,氧原子最外層達到8電子穩定結構,水的電子式為: ;
;
故答案為: 或
或 ;
;
(3)當X為非金屬,Y為金屬時,X為H2或C,Y為CuO等,符合轉化關系,
發生反應為H2+CuO$\frac{\underline{\;高溫\;}}{\;}$Cu+H2O(或C+2CuO$\frac{\underline{\;高溫\;}}{\;}$2Cu+CO2↑等);
故答案為:H2或C;
(4)當X與Y均為金屬時,考慮鋁熱反應,A為Al,B為Fe3O4(或Fe2O3),符合轉化關系,
反應方程式為:8Al+3Fe3O4 $\frac{\underline{\;高溫\;}}{\;}$9Fe+4Al2O3(或2Al+Fe2O3 2Fe+Al2O3);
故答案為:8Al+3Fe3O4 $\frac{\underline{\;高溫\;}}{\;}$9Fe+4Al2O3(或2Al+Fe2O3 $\frac{\underline{\;高溫\;}}{\;}$2Fe+Al2O3);
(5)當X與Y均為非金屬時,若X與Y同主族,X為C單質,B為SiO2,符合轉化關系,
反應方程式為:2C+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+2CO↑;若X與Y不在同一主族,X為C單質,B為H2O,符合轉化關系,反應方程式為:C+H2O$\frac{\underline{\;高溫\;}}{\;}$H2+CO;
故答案為:2C+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+2CO↑;C+H2O$\frac{\underline{\;高溫\;}}{\;}$H2+CO.
點評 本題以無機框圖題的形式考查中學置換反應、元素單質及其化合物之間的相互轉化關系,根據要求選擇適合的反應,難度較大,以考查學生的對基礎知識的熟練掌握程度為主.


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:解答題
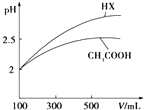 已知25℃時部分弱電解質的電離平衡常數數據如表所示:
已知25℃時部分弱電解質的電離平衡常數數據如表所示:| 化學式 | CH3COOH | H2CO3 | HClO | |
| 電離平衡常數 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
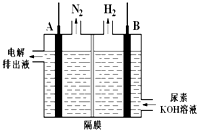
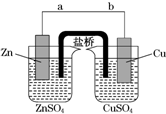 某學生利用如圖實驗裝置探究鹽橋式原電池的工作原理(Cu元素的相對原子質量為64).按照實驗步驟依次回答下列問題:
某學生利用如圖實驗裝置探究鹽橋式原電池的工作原理(Cu元素的相對原子質量為64).按照實驗步驟依次回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分餾石油時,溫度計的水銀球必須插入液面下 | |
| B. | 用濃氨水洗滌做過銀鏡反應的試管 | |
| C. | 配制銀氨溶液時,將稀氨水慢慢滴加到稀硝酸銀溶液中,產生白色沉淀后繼續滴加直至沉淀剛好溶解為止 | |
| D. | 蔗糖水解后,直接滴加新制氫氧化銅懸濁液并加熱檢驗水解產物中的葡萄糖 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 位于同一主族的元素的價電子數相同,則各元素的常見化合價也一定相同 | |
| B. | 堿金屬族元素同鹵族元素一樣,其單質的熔沸點隨元素原子序數的增大而逐漸升高 | |
| C. | 若x是ⅡB族中元素的原子序數,那么原子序數為x+1的元素是ⅢA族 | |
| D. | 在周期表中金屬和非金屬元素的分界線附近的元素是過渡元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com