

| A. | 用右圖所示方法可保護鋼閘門不被腐蝕 | |
| B. | SiO2(s)+2C(s)═Si(s)+2CO(g)在常溫下不能自發進行,則該反應的△H>0 | |
| C. | 常溫下,NH4Cl溶液加水稀釋,$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$增大 | |
| D. | C(s)+H2O(g)?CO(g)+H2(g)(△H>0),其它條件不變時,升高溫度,正反應速率增大、逆反應速率減小,平衡正向移動 |
分析 A、保護鋼閘門不被腐蝕,應讓鋼閘門做原電池的正極或電解池的陰極;
B、△H-T△S>0反應非自發進行,反應△S>0,△H>0;
C、鹽的水解平衡常數Kh只受溫度的影響;
D、升高溫度,正、逆反應速率都增大;
解答 解:A、保護鋼閘門不被腐蝕,應讓鋼閘門做原電池的正極或電解池的陰極,而此圖中鋼閘門做了原電池的負極,腐蝕速率會加快,故A錯誤;
B、△H-T△S>0,反應非自發進行,反應△S>0,滿足△H-T△S>0,則△H>0,故B正確;
C、銨根離子的水解平衡常數Kh=$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$只受溫度的影響,與其他任何因素無關,故常溫加水稀釋,Kh值不變,故C錯誤;
D、升高溫度,正、逆反應速率都增大,正反應速率增大更多,平衡向正反應方向移動,故D錯誤;
故選B.
點評 本題考查金屬的腐蝕與防護、水解平衡常數的影響因素,題目難度不大,本題把握外界條件對平衡常數的影響.


科目:高中化學 來源: 題型:選擇題
| A. | PM2.5表示每立方米空氣中直徑小于或等于2.5μm的顆粒物的含量,PM2.5值越高,大氣污染越嚴重,因此由PM2.5引起的霧霾一定屬于膠體 | |
| B. | 分光光度計可用于分析溶液顏色與反應物(或生成物)濃度的關系,從而確定化學反應速率 | |
| C. | 對“地溝油”加工處理可以達到變廢為寶的目的,比如對“地溝油”進行分餾可以制得汽油、煤油 | |
| D. | 次氯酸和臭氧都是強氧化劑,都能殺死水中的細菌.自來水常用氯氣來殺菌消毒,是因為氯氣殺菌消毒效果要比臭氧好,且不會殘留有毒、有害物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖是檢驗氣體性質的實驗裝置.向裝置中緩慢通入氣體X,若關閉活塞K,品紅溶液無變化、澄清石灰水變渾濁;若打開活塞K,品紅溶液褪色.據此判斷,氣體X和液體Y可能是( )
如圖是檢驗氣體性質的實驗裝置.向裝置中緩慢通入氣體X,若關閉活塞K,品紅溶液無變化、澄清石灰水變渾濁;若打開活塞K,品紅溶液褪色.據此判斷,氣體X和液體Y可能是( )| 選項 物質 | A | B | C | D |
| X | H2S | SO2 | CO2 | Cl2 |
| Y | 濃硫酸 | NaHCO3飽和溶液 | Na2SO3 溶液 | NaHSO3 溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使酚酞變紅色的溶液:NH4+、Ca2+、NO3-、SO42- | |
| B. | c(OH-)=1×10-13 mol•L-1的溶液:Na+、K+、ClO-、SO42- | |
| C. | 0.1 mol•L-1 FeCl2溶液:K+、Na+、SO42-、NO3- | |
| D. | 0.1 mol•L-1 KMnO4溶液:Na+、Mg2+、NO3-、SO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
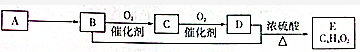
| A. | B中含有的官能團為羥基 | B. | 可用碳酸鈉溶液區別B、D | ||
| C. | D中含有C═O鍵,E的名稱為乙酸乙酯 | D. | B+D→E反應的裝置如圖 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 亞氯酸鈉(NaClO2)是一種重要的含氯消毒劑,主要用于水的消毒以及砂糖、油脂的漂白與殺菌.如圖是過氧化氫法生產亞氯酸鈉的工藝流程圖:
亞氯酸鈉(NaClO2)是一種重要的含氯消毒劑,主要用于水的消毒以及砂糖、油脂的漂白與殺菌.如圖是過氧化氫法生產亞氯酸鈉的工藝流程圖:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com