
【題目】鐵氮化合物(FexNy)在磁記錄材料領域有著廣泛的應用前景。某FexNy的制備需鐵、氮氣、丙酮和乙醇參與。
(1)Fe3+基態核外電子排布式為___未成對電子數為___個。
(2)丙酮(![]() )分子中碳原子軌道的雜化類型是___,丙酮分子中含有σ鍵的數目為____個。
)分子中碳原子軌道的雜化類型是___,丙酮分子中含有σ鍵的數目為____個。
(3)C、H、O三種元素的電負性由小到大的順序為___。
(4)乙醇的沸點高于丙酮,這是因為___。
(5)利用價層電子對互斥理論判斷PCl3的立體構型是___。
(6)某FexNy的晶胞如圖-1所示,Cu可以完全替代該晶體中a位置Fe或者b位置Fe,形成Cu替代型產物Fe(x-n) CunNy。FexNy轉化為兩種Cu替代型產物的能量變化如圖-2 所示,其中更活潑的Cu替代型產物的化學式為___。

【答案】[Ar]3d5或1s22s22p63s23p63d5 5 sp2和sp3 9 H<C<O 乙醇分子間存在氫鍵 三角錐形 FeCu3N
【解析】
(1)Fe的原子序數為26,根據核外電子的排布規則書寫電子排布式;
(2)![]() 中單鍵均為σ鍵,雙鍵中含1個σ鍵,甲基上C形成4個σ鍵,C=O中C形成3個σ鍵,據此分析解答;
中單鍵均為σ鍵,雙鍵中含1個σ鍵,甲基上C形成4個σ鍵,C=O中C形成3個σ鍵,據此分析解答;
(3)根據非金屬性越強,電負性越大分析判斷;
(4)乙醇分子之間形成氫鍵,導致沸點較高;
(5)根據價層電子對個數=σ鍵個數+孤電子對個數=σ鍵個數+![]() (a-xb)分析判斷;
(a-xb)分析判斷;
(6)由圖2可知,Cu替代b位置的Fe時能量較高,不穩定,結合分攤法分析解答。
(1)Fe的原子序數為26,Fe3+基態核外電子數為23,3d為半滿穩定結構,Fe3+基態核外電子排布式為[Ar]3d5或1s22s22p63s23p63d5,未成對電子數為5個,故答案為:[Ar]3d5或1s22s22p63s23p63d5;5;
(2)![]() 中單鍵均為σ鍵,雙鍵中含1個σ鍵,1個π鍵,丙酮分子共有9個σ鍵;甲基上C形成4個σ鍵,C=O中C形成3個σ鍵,含有1個孤電子對,則羰基上C為sp2雜化,甲基上C為sp3雜化,故答案為:sp2和sp3;9;
中單鍵均為σ鍵,雙鍵中含1個σ鍵,1個π鍵,丙酮分子共有9個σ鍵;甲基上C形成4個σ鍵,C=O中C形成3個σ鍵,含有1個孤電子對,則羰基上C為sp2雜化,甲基上C為sp3雜化,故答案為:sp2和sp3;9;
(3)非金屬性越強,電負性越大,則C、H、O三種元素的電負性由小到大的順序為H<C<O,故答案為:H<C<O;
(4)乙醇分子間存在氫鍵,而丙酮中不存在氫鍵,導致乙醇的沸點高于丙酮,故答案為:乙醇分子間存在氫鍵;
(5)PCl3中P原子的價層電子對數=3+![]() =4,P原子采用sp3雜化,含有1個孤電子對,PCl3的立體構型是三角錐形,故答案為:三角錐形;
=4,P原子采用sp3雜化,含有1個孤電子對,PCl3的立體構型是三角錐形,故答案為:三角錐形;
(6)由圖2可知,Cu替代a位置的Fe時能量較低,更穩定,替代b位置的Fe時能量較高,不穩定,因此更活潑的Cu替代型產物是替代b位置的Fe,則Cu位于面心,N(Cu)=6×![]() =3,Fe位于頂點,N(Fe)=8×
=3,Fe位于頂點,N(Fe)=8×![]() =1,N位于體心,則只有1個N,其化學式為FeCu3N,故答案為:FeCu3N。
=1,N位于體心,則只有1個N,其化學式為FeCu3N,故答案為:FeCu3N。


科目:高中化學 來源: 題型:
【題目】在10L密閉容器中,1molA和3molB在一定條件下反應:A(g)+xB(g)![]() 2C(g),2min后反應達到平衡時,測得混合氣體共3.4mol,生成0.4molC,則下列計算結果不正確的是( )
2C(g),2min后反應達到平衡時,測得混合氣體共3.4mol,生成0.4molC,則下列計算結果不正確的是( )
A.平衡時,物質的量比A:B:C=2:11:4
B.x值等于4
C.A的轉化率20%
D.B的平均反應速率為0.04mol·L-1·min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值。下列敘述中不正確的是( )
A.分子總數為NA的NO2和CO2混合氣體中含有的氧原子數為2NA
B.28g乙烯和丙烯(C3H6)的混合氣體中含有的碳原子數為2NA
C.常溫常壓下,92g的NO2和N2O4混合氣體含有的原子數為6NA
D.常溫常壓下,22.4L氯氣與足量H2充分反應 ,生成HCl的分子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,用元素符號或化學式填空回答以下問題:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
⑴在這些元素中,最活潑的非金屬元素是___________,化學性質最不活潑的元素是______________。
⑵表中金屬性最強的元素是_______________,其原子結構示意圖為 _______________________ 。
⑶表中元素的最高價氧化物對應的水化物中酸性最強的是__________,呈兩性的氫氧化物是______。
⑷元素⑩的元素符號為 ____________ ,元素⑦的原序數為_________。
⑸在①~③元素中,原子半徑最大的是_____________,原子半徑最小的是_____________。
⑹十種元素中有一種元素的氫化物水溶液呈堿性,該氫化物的電子式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著社會經濟的發展,汽車已進入千家萬戶,它給人們出行帶來方便的同時汽車尾氣污染問題也日益突顯,汽車尾氣中含![]() 和固體懸浮顆粒等。用活性炭還原處理氮氧化物是一種實用的氮氧化物轉化方法:
和固體懸浮顆粒等。用活性炭還原處理氮氧化物是一種實用的氮氧化物轉化方法:![]() ,可實現氮氧化物無害轉化。下列環境問題與汽車尾氣的大量排放無關的是( )
,可實現氮氧化物無害轉化。下列環境問題與汽車尾氣的大量排放無關的是( )
A.酸雨B.溫室效應C.PM 2.5超標D.白色污染
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋中有豐富的食品、礦產、能源、藥物和水產資源,下圖為海水利用的部分過程。
下列有關說法正確的是
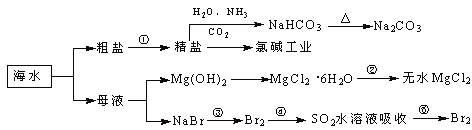
A. 過程①中除去粗鹽中的SO42-、Ca2+、Mg2+、Fe3+等雜質,加入的藥品順序為:Na2CO3溶液→NaOH溶液→BaCl2溶液→過濾后加鹽酸
B. 用澄清的石灰水可鑒別NaHCO3和Na2CO3
C. 過程②中結晶出的MgCl2·6H2O要在HCl氛圍中加熱脫水制得無水MgCl2
D. 工業上通過電解飽和MgCl2溶液制取金屬鎂
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于Fe3+、Fe2+性質實驗的說法錯誤的是

A. 用上圖裝置可以制備沉淀Fe(OH)2
B. 配制FeCl3溶液時,先將氯化鐵晶體溶于較濃的鹽酸中,再加水稀釋到所需要的濃度
C. FeCl3溶液中滴加KSCN溶液會生成紅色沉淀
D. 向FeCl2溶液中加入少量鐵粉是為了防止Fe2+被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列各組物質中:A.O2和O3 B.12C和13C C.H2O和D2O
___組兩物質互為同位素;___組兩物質互為同素異形體。
(2)工業上用![]() 做原料制取硝酸,要經過三步主要反應,請寫出第二步和第三步反應的化學方程式。
做原料制取硝酸,要經過三步主要反應,請寫出第二步和第三步反應的化學方程式。
第一步反應:4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
第二步反應:___;
第三步反應:___。
(3)把下列現象中硫酸所表現出來的性質填寫在空白處。
用稀硫酸清洗鐵銹___;
放置在敞口燒杯中的濃硫酸質量增加__;
濃硫酸滴在紙上時,紙變黑。__;
把銅片放入熱的濃硫酸中時,有氣體放出。___。
(4)用序號填空,下列物質中:①PH3 ②H2O2 ③Na2O2 ④KOH ⑤(NH4)2SO4 ⑥F2
只含共價鍵的是___;既含離子鍵又含極性鍵的是___;既含離子鍵又含非極性鍵的是___。
(5)下列反應中,屬于放熱反應的有___(填序號)。
①煅燒石灰石(主要成分是CaCO3)制生石灰(CaO)
②Ba(OH)2·8H2O和NH4Cl晶體的反應
③炸藥爆炸
④酸與堿的中和反應
⑤生石灰與水作用制熟石灰
⑥食物因氧化而腐敗
⑦乙醇燃燒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中科院某課題組將二氧化錳和生物質置于一個由濾紙制成的折紙通道內形成電池(如圖所示),該電池可將可樂(pH=2.5)中的葡萄糖作為燃料獲得能量。下列說法中正確的是( )
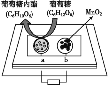
A. a極為正極
B. 隨著反應不斷進行,負極區的pH不斷增大
C. b極電極反應式為MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,電路中轉移0.02mol電子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com