
����ұ����һ�N�¹�ˇ�����ܺ��١��p�٭h(hu��n)����Ⱦ���Q�顰�Gɫұ�𡱡���ԭ��������������U���;���U���ܰѵVʯ�е������������ᣬ����(y��ng)ʽ��2S+3O2+2H2O
2H2SO4�����������F��U��������a(ch��n)�����������ܰ����၆�F�����������F�ۼ����õ�������Ҫ�����������ɵ������F�ɰ�FeS2���S�F�V����Cu2S���x�~�V�����D(zhu��n)׃?y��u)�����Ի�������ĵVʯ���ܽ�������仯�W(xu��)�^���ǣ�
Fe2S2���S�F�V��+7Fe2(SO4)3+8H2O
15FeSO4+ 8H2SO4
Cu2S���x�~�V��+2Fe2(SO4)2
2CuSO4+4FeSO4+S
��1�������ڷ���(y��ng)�Ļ��W(xu��)����ʽ�� ��
��2��ij���С�M�����������~�����၆�F�����Ի��Һ���x�����၆�F��Һ����(j��ng)����Y�ϵ�֪������Һ��ͨ�^�{(di��o)��(ji��)��Һ����A�Զ�ʹCu2+��Fe2+��Fe3+�քe���ɳ�����pH���2
|
���|(zh��) |
Cu��OH��2 |
Fe��OH��2 |
Fe��OH��3 |
|
�_ʼ����pH |
6.0 |
7.5 |
1.4 |
|
������ȫpH |
13 |
14 |
3.7 |
�����������ԇ���ɹ��x��A�� H2O2 B��CaO C��CuO D��ϡH2SO4 E���F��;
��(j��ng)�^�V��߀���O(sh��)Ӌ�Č��������E��Ŀ���ǣ�
|
���E |
������ |
��������Ŀ�� |
|
���E1 |
|
|
|
���E2 |
|
|
|
���E3] |
|
|
|
���E4 |
ϴ�� |
|
|
���E5 |
|
�õ�FeSO4��Һ |
��3������CuSO4��FeSO4���Һ�м����m���AҺ������Һ���ɡ��Ɵ��õ��tɫ��ĩ��Fe2O3��Cu2O�������y��ԓ�������Cu2O���|(zh��)���֔�(sh��)��ԓ���С�M�ķ�������m g������м���������ϡ���ᣬ��(j��ng)�^�V��ϴ�졢����Q�����w���|(zh��)����n g����֪Cu2O����ϡ��������Cu��CuSO4��ij�W(xu��)����(j��)��Ӌ���ԓ�����Cu2O���|(zh��)���֔�(sh��)��Ӌ��ʽ ��ԓ�W(xu��)����Ӌ���Ƿ����_��
��Ո�f������
��
��ԓ�W(xu��)����Ӌ���Ƿ����_��
��Ո�f������
��
��14�֣�1��4FeSO4+2H2SO4+O2=2Fe2��SO4��3+2H2O��2�֣�
��2��
|
���E |
������ |
��������Ŀ�� |
|
���E1 |
����H2O2 |
�Ѷ��r�F���������r |
|
���E2 |
�����m�������~���{(di��o)��(ji��)pH��3.7 |
���C���r�F��ȫ���� |
|
���E3 |
�^�V |
�V���������F |
|
���E4 |
ϴ����� |
��ȥ�s�|(zh��) |
|
���E5 |
������м����m��ϡ������m���F�� |
�õ�FeSO4��Һ |
��3�������_��2�֣������ԓӋ��]�п��]Cu�cFe3+�ķ���(y��ng)��2�֣�
��������(1)����(j��)����(y��ng)����������֪��ԓ����(y��ng)�ķ���ʽ��4FeSO4+2H2SO4+O2 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
��2��pH>3.7�r��F(xi��n)e(OH)3�ѳ�����ȫ����pH=6.0�rCu(OH)2���_ʼ�������t����ͨ�^�{(di��o)��(ji��)��Һ��pHʹ�FԪ�ء��~Ԫ�ط��x�����x�r�����Ȍ�Fe2+������Fe3+���������x��H2O2�^�ã��]���s�|(zh��)���룻���{(di��o)��(ji��)��Һ��pH���x���ԇ����Ҫ����H+�ֲ������s�|(zh��)���x��CuO����m������茢Fe(OH)3�����D(zhu��n)����FeSO4��Һ���x��ϡ������F�ۼ��ɡ�
��3��Fe2O3��Cu2O��������ϡ����l(f��)���ķ���(y��ng)�У�Fe2O3+3H2SO4��Fe2(SO4)3+3H2O,Cu2O+H2SO4 Cu+CuSO4+H2O��Cu+Fe2(SO4)3��2FeSO4+CuSO4��


 ��x��܇ϵ�д�
��x��܇ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
| ||
| ||
| ���|(zh��) | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �_ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
| ���E | ������ | ��������Ŀ�� |
| ���E1 | ����H2O2 ����H2O2 |
�Ѷ��r�F���������r �Ѷ��r�F���������r |
| ���E2 | �����m�������~���{(di��o)��(ji��)pH��3.7 �����m�������~���{(di��o)��(ji��)pH��3.7 |
���C���r�F��ȫ���� ���C���r�F��ȫ���� |
| ���E3 | �^�V �^�V |
�V���������F �V���������F |
| ���E4 | ϴ�� | ��ȥ�s�|(zh��) ��ȥ�s�|(zh��) |
| ���E5 | ������м����m��ϡ������m���F�� ������м����m��ϡ������m���F�� |
�õ�FeSO4��Һ |
| 144n |
| 64m |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2013���|��ʡ�|�������p�Z�W(xu��)У������һ��ģ�M��ԇ���W(xu��)ԇ������������ �}�ͣ�����}
����ұ����һ�N�¹�ˇ�����ܺ��١��p�٭h(hu��n)����Ⱦ���Q�顰�Gɫұ�𡱡���ԭ��������������U���;���U���ܰѵVʯ�е������������ᣬ����(y��ng)ʽ��2S+3O2+2H2O 2H2SO4�����������F��U��������a(ch��n)�����������ܰ����၆�F�����������F�ۼ����õ�������Ҫ�����������ɵ������F�ɰ�FeS2���S�F�V����Cu2S���x�~�V�����D(zhu��n)׃?y��u)�����Ի�������ĵVʯ���ܽ�������仯�W(xu��)�^���ǣ�
Fe2S2���S�F�V��+7Fe2(SO4)3+8H2O 15FeSO4+ 8H2SO4
Cu2S���x�~�V��+2Fe2(SO4)2 2CuSO4+4FeSO4+S
��1�������ڷ���(y��ng)�Ļ��W(xu��)����ʽ�� ��
��2��ij���С�M�����������~�����၆�F�����Ի��Һ���x�����၆�F��Һ����(j��ng)����Y�ϵ�֪������Һ��ͨ�^�{(di��o)��(ji��)��Һ����A�Զ�ʹCu2+��Fe2+��Fe3+�քe���ɳ�����pH���2
| ���|(zh��) | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �_ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
| ���E | ������ | ��������Ŀ�� |
| ���E1 | | |
| ���E2 | | |
| ���E3] | | |
| ���E4 | ϴ�� | |
| ���E5 | | �õ�FeSO4��Һ |
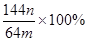 ��ԓ�W(xu��)����Ӌ���Ƿ����_�� ��Ո�f������ ��
��ԓ�W(xu��)����Ӌ���Ƿ����_�� ��Ո�f������ ���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
| ���|(zh��) | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �_ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
| ���E | ������ | ��������Ŀ�� |
| ���E1 | ______ | ______ |
| ���E2 | ______ | ______ |
| ���E3 | ______ | ______ |
| ���E4 | ϴ�� | ______ |
| ���E5 | ______ | �õ�FeSO4��Һ |
| 144n |
| 64m |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2013���|��ʡ�|�������p�Z�W(xu��)У�߿����W(xu��)һģԇ���������棩 �}�ͣ�����}
| ���|(zh��) | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �_ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
| ���E | ������ | ��������Ŀ�� |
| ���E1 | ||
| ���E2 | ||
| ���E3 | ||
| ���E4 | ϴ�� | |
| ���E5 | �õ�FeSO4��Һ |
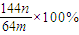 ��ԓ�W(xu��)����Ӌ���Ƿ����_�� ��Ո�f������ ��
��ԓ�W(xu��)����Ӌ���Ƿ����_�� ��Ո�f������ ���鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com