
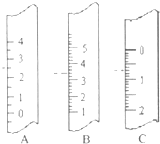
 (1)如圖分別是溫度計、量筒、滴定管的一部分,則:
(1)如圖分別是溫度計、量筒、滴定管的一部分,則:| c(標準)×V(標準) |
| V(待測) |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:
| 空 |
| 燃 |
| 空 |
| 燃 |
| 光合作用 |
| ||
| △ |
| ||
| △ |
| ||
| △ |
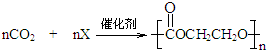 ,則X的結構簡式為
,則X的結構簡式為

查看答案和解析>>
科目:高中化學 來源: 題型:
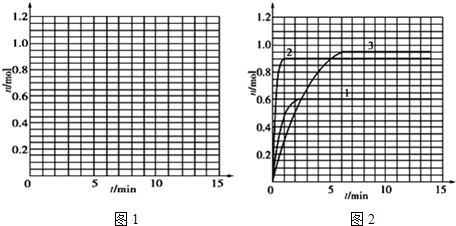
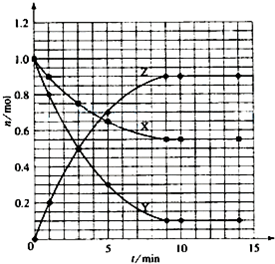
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

查看答案和解析>>
科目:高中化學 來源: 題型:

 、
、 、
、 分別表示N2、H2、NH3.圖⑤表示生成的NH3離開催化劑表面,圖②和圖③的含義分別是
分別表示N2、H2、NH3.圖⑤表示生成的NH3離開催化劑表面,圖②和圖③的含義分別是| c2(NH3) |
| c(N2).c3(H2) |
| c2(NH3) |
| c(N2).c3(H2) |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| 時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4mol?L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(NO)(×10-3mol?L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

查看答案和解析>>
科目:高中化學 來源: 題型:
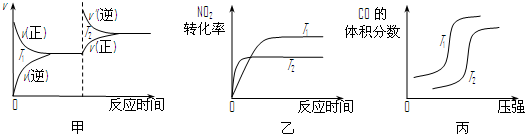
 的物質計量數;X1、X2表示不同溫度或壓強),某物理量Y隨時間(t)變化的情況如圖所示,
的物質計量數;X1、X2表示不同溫度或壓強),某物理量Y隨時間(t)變化的情況如圖所示,查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com