
【題目】某溫度下,H2(g)+CO2(g)![]() H2O(g)+CO2(g)的平衡常數
H2O(g)+CO2(g)的平衡常數![]() 。該溫度下在甲、乙、丙三個恒容密閉容器中,
。該溫度下在甲、乙、丙三個恒容密閉容器中,
起始濃度 | 甲 | 乙 | 丙 |
c(H2)/mol | 0.010 | 0.020 | 0.020 |
c(CO2)/mol | 0.010 | 0.010 | 0.020 |
投入H2(g)和CO2(g),其起始濃度如表所示。下列判斷不正確的是( )
A.平衡時,乙中CO2的轉化率大于60%
B.平衡時,甲中和丙中H2的轉化率均是60%
C.平衡時,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反應開始時,丙中的反應速率最快,甲中的反應速率最慢
【答案】C
【解析】
A.設甲容器中平衡時反應掉的二氧化碳的濃度為xmol/L,根據K=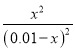 =2.25,得x=0.006,所以CO2的轉化率為60%,H2的轉化率也是60%,在乙容器中相當于是甲容器中增加了H2,CO2的轉化率增大,故A不選;
=2.25,得x=0.006,所以CO2的轉化率為60%,H2的轉化率也是60%,在乙容器中相當于是甲容器中增加了H2,CO2的轉化率增大,故A不選;
B.設甲容器中平衡時反應掉的氫氣的濃度為xmol/L,根據K=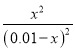 =2.25,得x=0.006,所以H2的轉化率是60%,又甲和丙為等效平衡,所以甲中和丙中H2的轉化率均是60%,故B不選;
=2.25,得x=0.006,所以H2的轉化率是60%,又甲和丙為等效平衡,所以甲中和丙中H2的轉化率均是60%,故B不選;
C.由A的分析可知,平衡時甲容器中c(CO2)是0.004mol/L,而甲和丙為等效平衡,但丙的起始濃度為甲的兩倍,所以平衡時,丙中c(CO2)是0.008mol/L,故C選;
D.根據濃度越大反應速率越快可知,反應開始時,丙中的反應物濃度最大,所以反應速率最快,甲中的反應物濃度最小,所以反應速率最慢,故D不選;
綜上所述,故選C。


 黃岡小狀元同步計算天天練系列答案
黃岡小狀元同步計算天天練系列答案科目:高中化學 來源: 題型:
【題目】下列各離子①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO3- ⑧NH4+中,不影響水的電離平衡的是( )
A.①③⑤⑦⑧B.②④⑦C.①⑥D.②④⑥⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a~n10中元素在周期表中的位置如圖所示,請回答下列問題:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的陰離子的結構示意圖為___。
(2)b的最高價氧化物的化學式為___;用化學方程式表示f、d的單質形成f2d2的過程___。
(3)d、g、n形成的簡單離子的半徑由大到小的順序為___(用離子符號表示)。
(4)以上元素組成的物質有下列框圖中的轉化關系,其中甲為10電子微粒。
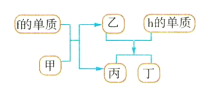
請寫出h的單質與乙反應的化學方程式:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D四種元素的核電荷數依次增大,它們的簡單離子的電子層數相同且最外層電子數均為8。A原子的L層電子數與K、M層電子數之和相等,D原子的K、L層電子數之和等于其電子總數的一半。
請回答下列問題:
(1)四種元素的元素符號依次是A________B________C________D________。它們的原子半徑由大到小的順序是________________(用元素符號表示)。
(2)試寫出四種元素的簡單離子結構示意圖A________B________C________D________。它們的離子半徑由大到小的順序是________________(用元素符號表示)
(3)A、B、C、D的最高價氧化物對應水化物的化學式分別是________________,分別比較其最高價氧化物對應水化物酸性和堿性的強弱________________。
(4)寫出其中非金屬元素形成的氣態氫化物的化學式:________,其穩定性強弱是_________,理由是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能達到實驗目的的是( )
序號 | 實驗操作 | 實驗目的 |
A | Cl2、Br2分別與H2反應 | 比較氯、溴的非金屬性強弱 |
B | MgCl2、AlCl3溶液中分別通入NH3 | 比較鎂、鋁的金屬性強弱 |
C | 測定等物質的量濃度的H2CO3、H2SO4溶液的pH | 比較碳、硫的非金屬性強弱 |
D | Fe、Cu分別放入相同濃度的鹽酸中 | 比較鐵、銅的金屬性強弱 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】解釋下列過程的離子方程式不正確的是
A.K2Cr2O7 溶液中加入濃 NaOH 溶液后變黃:![]() +H2O
+H2O![]() 2
2![]() +2H+
+2H+
B.明礬溶于水產生Al(OH)3 膠體:Al3++3H2O![]() Al(OH)3(膠體)+3H+
Al(OH)3(膠體)+3H+
C.用碳酸鈉溶液處理鍋爐水垢中的硫酸鈣:CaSO4+![]() ==CaCO3+
==CaCO3+![]()
D.向Ca(HCO3)2 溶液中滴加少量 NaOH 溶液生成白色沉淀:Ca2++2![]() +2OH-=CaCO3↓+
+2OH-=CaCO3↓+![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】油脂是重要的營養物質.某天然油脂A可發生下列反應:

已知:A的分子式為C57H106O6.1mol該天然油脂A經反應①可得到1molD、1mol不飽和脂肪酸B和2mol直鏈飽和脂肪酸C.經測定B的相對分子質量為280,原子個數比為C:H:O=9:16:1;
(1)寫出B的分子式:________________________;
(2)寫出反應①的反應類型:____________;C的名稱(或俗稱)是_________;
(3)近日,電視媒體關于“氫化油危害堪比殺蟲劑”的報道引發軒然大波,反應②為天然油脂的氫化過程.下列有關說法不正確的是_______________;
a.氫化油又稱人造奶油,通常又叫硬化油.
b.植物油經過氫化處理后會產生副產品反式脂肪酸甘油酯,攝入過多的氫化油,容易堵塞血管而導致心腦血管疾病.
c.氫化油的制備原理是在加熱植物油時,加入金屬催化劑,通入氫氣,使液態油脂變為半固態或固態油脂.
d.油脂的氫化與油脂的皂化都屬于加成反應
(4)D和足量金屬鈉反應的化學方程式_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】表是元素周期表的一部分,請用元素符號、離子符號或相關化學式回答有關問題:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中能形成兩性氫氧化物的元素在周期表中的位置是________;
(2)寫出②的氣態氫化物的結構式________;
(3)元素④⑤⑥⑦離子半徑由大到小的順序________;
(4)①、⑥、⑦三種元素的最高價氧化物的水化物中酸性最強的是________;④、⑤、⑨三種元素的最高價氧化物的水化物中堿性最強的是
(5)⑦和⑩氧化性較強的是________用一個置換反應證實這一結論(寫化學方程式)___________________________。
(6)④⑤兩元素相比較,金屬性較強的是________,可以驗證該結論的實驗是________;
(a)將在空氣中放置已久的這兩種元素的塊狀單質分別放入熱水中
(b)將形狀、大小相同的這兩種元素的單質用砂紙打磨后分別和同濃度的鹽酸反應
(c)將形狀、大小相同兩種元素的單質用砂紙打磨后分別和熱水作用,并滴入酚酞
(d)比較這兩種元素的氣態氫化物的穩定性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦和鈦的合金已被廣泛應用于制造電訊器材、人造骨骼、化工設備、飛機等航天航空材料,被譽為“未來世界的金屬”。試回答下列問題:
(1)鈦有![]() Ti和
Ti和![]() Ti兩種原子,它們互稱為________。Ti元素在元素周期表中的位置是第________周期,第________族;基態原子的電子排布式為________,按外圍電子排布特征Ti元素在元素周期表分區中屬于___________區元素。
Ti兩種原子,它們互稱為________。Ti元素在元素周期表中的位置是第________周期,第________族;基態原子的電子排布式為________,按外圍電子排布特征Ti元素在元素周期表分區中屬于___________區元素。
(2)偏鈦酸鋇在小型變壓器、話筒和擴音器中都有應用。偏鈦酸鋇晶體中晶胞的結構如圖所示,它的化學式是_____________。
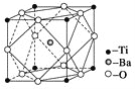
(3)現有含Ti3+的配合物,化學式為[TiCl(H2O)5]Cl2·H2O。配離子[TiCl(H2O)5]2+中含有的化學鍵類型是________,該配合物的配位體是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com