
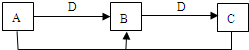
分析 I.A、B、C三種物質都由短周期元素組成,A連續與D反應生成C,D是空氣的主要成分之一,判斷D為O2.
(1)若A是非金屬單質,常溫下為固態,且A與C在一定條件下能發生反應,則A為碳,B為CO,C為CO2;
(2)若A短周期是金屬單質,則A為Na,B為Na2O,C為Na2O2;
(3)若常溫時C為紅棕色氣體,則C為NO2,A為N2或NH3,B為NO;
Ⅱ.(1)①若D為生活中常見的金屬單質,A與D連續發生氧化反應,則D為變價金屬,A具有強氧化性,由轉化關系可知,A為Cl2,D為Fe,B為FeCl3,C為FeCl2;
(2)若D為強堿,A為常見的正鹽,A、B、C中共同含有的元素是日常生活中常見的合金元素,則A為鋁鹽、B為氫氧化鋁、C為偏鋁酸鹽.
解答 I.A、B、C三種物質都由短周期元素組成,A連續與D反應生成C,D是空氣的主要成分之一,判斷D為O2.
(1)若A是非金屬單質,常溫下為固態,且A與C在一定條件下能發生反應,則A為碳,B為CO,C為CO2,
故答案為:CO2;
(2)若A短周期是金屬單質,則A為Na,B為Na2O,C為Na2O2,Na再周期表中位置為:第三周期IA族,
故答案為:第三周期IA族;
(3)若常溫時C為紅棕色氣體,則C為NO2,A為N2或NH3,B為NO,工業上用A與D反應制取B的反應是氨氣的催化氧化反應生成一氧化氮和水,反應的化學方程式為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O,
故答案為:N2或NH3;4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O;
Ⅱ.(1)①若D為生活中常見的金屬單質,A與D連續發生氧化反應,則D為變價金屬,A具有強氧化性,由轉化關系可知,A為Cl2,D為Fe,B為FeCl3,C為FeCl2,
A與C反應生成B的離子方程式為:2Fe2++Cl2=2Fe3++2Cl-,
檢驗FeCl3中陽離子的方案:取少量B溶液,往其中滴加少量硫氰化鉀溶液,若溶液變紅,則含有Fe3+,
故答案為:2Fe2++Cl2=2Fe3++2Cl-;取少量B溶液,往其中滴加少量硫氰化鉀溶液,若溶液變紅,則含有Fe3+;
(2)若D為強堿,A為常見的正鹽,A、B、C中共同含有的元素是日常生活中常見的合金元素,則A為鋁鹽、B為氫氧化鋁、C為偏鋁酸鹽,A與C反應生成B的離子方程式為:3AlO2-+Al3++6H2O=4Al(OH)3↓,
故答案為:3AlO2-+Al3++6H2O=4Al(OH)3↓.
點評 本題考查無機物的推斷,基本屬于開放性題目,需要學生熟練掌握元素化合物性質,熟練掌握中學常見連續反應,題目難度中等.


 快樂小博士鞏固與提高系列答案
快樂小博士鞏固與提高系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度,溶液中c(OH-)降低 | B. | 加入少量NaOH固體,c(CO32-)增大 | ||
| C. | c(Na+)═2c(CO32-)+c(HCO3-)+c(H2CO3) | D. | c(Na+)+c(H+)═2c(CO32-)+2c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
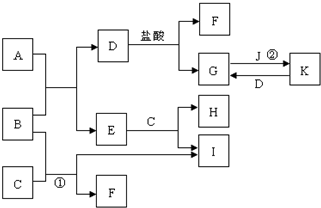 如圖所示的是一些常見的單質、化合物之間的轉化關系圖,有些反應中的部分物質和反應條件被略去. A俗稱“鐵紅”,B、D都是日常生活中常見的金屬,且B元素是地殼中含量最多的金屬元素,常溫下,J為黃綠色氣體,H為無色氣體;C是一種堿,且其焰色反應時,透過藍色鈷玻璃可觀察到紫色火焰.
如圖所示的是一些常見的單質、化合物之間的轉化關系圖,有些反應中的部分物質和反應條件被略去. A俗稱“鐵紅”,B、D都是日常生活中常見的金屬,且B元素是地殼中含量最多的金屬元素,常溫下,J為黃綠色氣體,H為無色氣體;C是一種堿,且其焰色反應時,透過藍色鈷玻璃可觀察到紫色火焰. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子數 | B. | 分子數 | C. | 質量 | D. | 密度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
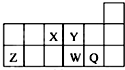
| A. | 元素Y的單質比元素X的單質更容易與氫氣反應 | |
| B. | 原子半徑的大小順序為:rX>rY>rZ>rW>rQ | |
| C. | 離子Y2-和Z3+的核外電子數和電子層數都不相同 | |
| D. | 元素W的最高價氧化物對應的水化物的酸性比Q的強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com