
【題目】二茂鐵[(C5H5)2Fe](橙黃色粉末,不溶于水,易溶于乙醚等有機溶劑)及其衍生物在工業、農業、醫藥、航天、節能、環保等行業具有廣泛地應用。某校課外小組依據反應2KOH+2C5H6+FeCl2=(C5H5)2Fe+2KCl+2H2O在絕對無水、無氧的條件下制備二茂鐵。
回答下列問題:
(1)甲組同學擬制備無水FeCl2,主要實驗流程為:

步驟I用飽和Na2CO3溶液浸泡的目的是_______;步驟II 中鐵屑是過量的,其目的是_____;步驟IV脫水的方法是____________。
(2)乙組用環戊二烯二聚體(沸點為174℃)制備環戊二烯(沸點為419℃),已知:(C5H6)2(環戊二烯二聚體)![]() 2C5H6(環戊二烯)。分離得到環戊二烯的操作方法為________。
2C5H6(環戊二烯)。分離得到環戊二烯的操作方法為________。
(3)丙組同學制備二茂鐵的裝置如圖所示(夾持裝置已略去)。

已知:二甲基亞砜的結構式為 ,熱穩定性好,能溶解大多數有機物。
,熱穩定性好,能溶解大多數有機物。
①圖中冷卻水從接口______進入(填“a”或“b”)。
②裝藥品前及整個過程需通入干燥的A,裝藥品前通入N2的目的是_________。
③反應后分離出上層橙黃色乙醚清液,先用鹽酸洗滌,其目的是_______;再用水洗,水洗時能說明已洗滌干凈的依據是_________;洗滌后得到的二茂鐵乙醚溶液獲得二茂鐵固體可采用的操作方法是_____________。
【答案】 除去鐵屑表而的油污 確保反應后的液體中不含Fe3+ 在HCl氣流中加熱脫水 蒸餾 a 排盡裝置內空氣 除去產品中溶解的KOH 取最后一次洗滌液水層中液體少許于試管中,滴入硝酸酸化的AgNO3溶液,無白色沉淀產生 蒸發結晶
【解析】(1)鐵屑表面有油污,用飽和Na2CO3溶液浸泡可除去;Fe2+易被氧化為Fe3+,為防止溶液中含有Fe3+,步驟II中應使鐵屑過量還原Fe3+;為防止氯化亞鐵晶體在加熱時發生水解,步驟IV脫水的方法是在HCl氣流中加熱脫水;綜上,本題正確答案是: 除去鐵屑表而的油污; 確保反應后的液體中不含Fe3+ ; 在HCl氣流中加熱脫水。
(2)已知:(C5H6)2(環戊二烯二聚體)![]() 2C5H6(環戊二烯),結合信息:環戊二烯二聚體(沸點為174℃)和環戊二烯(沸點為419℃),分離沸點不同的液體混合物的方法為蒸餾,因此,本題正確答案為:蒸餾。
2C5H6(環戊二烯),結合信息:環戊二烯二聚體(沸點為174℃)和環戊二烯(沸點為419℃),分離沸點不同的液體混合物的方法為蒸餾,因此,本題正確答案為:蒸餾。
(3)①在蒸餾裝置中,冷凝管的冷凝水要從下口進上口出,故選a;
②由信息知:制備二茂鐵需要在絕對無水、無氧的條件下,因此裝藥品前通入N2以排盡裝置內空氣;
③上層橙黃色乙醚清液,先用鹽酸洗滌,可除去產品中溶解的KOH;再用水洗,可除去過量的鹽酸,檢驗是否洗滌干凈,可檢查濾液中是否含有Cl-,采用的方法是:取最后一次洗滌液水層中液體少許于試管中,滴入硝酸酸化的AgNO3溶液,無白色沉淀產生,則說明洗滌干凈;由于二茂鐵易溶于乙醚,乙醚易揮發,故可采用蒸發結晶的操作方法;綜合以上分析:本題正確答案為: 除去產品中溶解的KOH ;取最后一次洗滌液水層中液體少許于試管中,滴入硝酸酸化的AgNO3溶液,無白色沉淀產生; 蒸發結晶


科目:高中化學 來源: 題型:
【題目】已知有以下物質相互轉化。試回答:
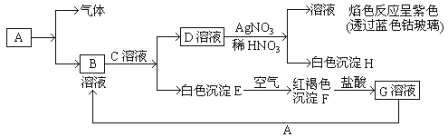
(1)寫出B的化學式_____________________D的化學式________________。
(2)寫出由E轉變成F的化學方程式_____________________________________。
(3)寫出用KSCN鑒別G溶液的離子方程式____________________________;向G溶液加入A的有關離子反應方程式________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于氧化還原反應的說法,正確的是( )
A.物質失去的電子數越多,其還原性越強
B.物質所含元素化合價升高的反應叫還原反應
C.某元素由化合態變為游離態,則它一定被還原
D.置換反應一定屬于氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用化學平衡移動原理解釋的是
A. 光照新制的氯水時,溶液的pH逐漸減小
B. 紅棕色的NO2,加壓后顏色先變深后變淺,但比原來要深
C. 500℃時比室溫更利于合成氨
D. 用排飽和食鹽水法收集Cl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹽酸廣泛應用在稀有金屬的濕法冶金、漂染工業、金屬加工、無機藥品及有機藥物的生產等領域中。HCl 極易溶于水,工業上用 HCl 氣體溶于水的方法制取鹽酸。
(1)用 12.0mol/L 濃鹽酸配置 230mL 0.3mol/L 的稀鹽酸,需要量取濃鹽酸的體積為___mL;
(2)溶液稀釋過程中需要的玻璃儀器有燒杯、玻璃棒、量筒、____________、___________;
(3)溶液稀釋過程中有以下操作:
a.量取濃鹽酸和一定體積的水,在燒杯中稀釋
b.計算所需濃鹽酸的體積
c.上下顛倒搖勻
d.加蒸餾水至刻度線 1-2cm 地方,改用膠頭滴管加蒸餾水至凹液面與刻度線相切
e.將稀釋液轉移入容量瓶,洗滌燒杯和玻璃棒,并將洗滌液轉移入容量瓶,振蕩
以上正確的操作順序為____________________________________________(填序號);
(4)實驗過程中的以下操作會導致最終所配溶液濃度(填“偏大”、“偏小”或“不變”)
a.量取濃鹽酸時俯視:______________________;
b.量取濃鹽酸后,清洗了量筒并將洗滌液轉移入容量瓶:______________________;
c.實驗前,容量瓶中有少量殘留蒸餾水:______________________;
(5)標準狀況,1L 水中通入 aL HCl 氣體,忽略鹽酸溶液中 HCl 的揮發,得到的鹽酸溶液密度為 b g/mL,物質的量濃度為 ______________________mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若在加入鋁粉能放出氫氣的溶液中,分別加入下列各組離子,一定能大量共存的是
A. NH![]() 、SO
、SO![]() 、CO
、CO![]() 、K+ B. Na+、Ba2+、Ca2+、HCO
、K+ B. Na+、Ba2+、Ca2+、HCO![]()
C. Mg2+、SO![]() 、K+、Cl- D. K+、Cl-、Na+、SO
、K+、Cl- D. K+、Cl-、Na+、SO![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】控制變量是科學研究重要方法。由下列實驗現象一定能得出相應結論的是
選項 | A | B |
裝 置 圖 |
|
|
現象 | 右邊試管產生氣泡較快 | 左邊棉球變棕黃色,右邊棉球變藍色 |
結論 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 |
選項 | C | D |
裝 置 圖 |
|
|
現象 | 試管中先出現淡黃色固體,后出現黃色固體 | 試管中液體變渾濁 |
結論 | Ksp:AgCl>AgBr>AgI | 非金屬性:C>Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na2O2可用作漂白劑和呼吸面具中的供氧劑
(1)某學習小組發現:在盛有Na2O2的試管中加入足量水,固體完全溶解,并立即產生大量氣泡,當氣泡消失后,向其中滴入1~2滴酚酞溶液,溶液變紅;將試管輕輕振蕩,紅色很快褪去;此時再向試管中加入少量MnO2粉末,又有氣泡產生。
①寫出Na2O2作供氧劑的化學反應方程式____________;
②使酚酞溶液變紅是因為________,紅色褪去的可能原因是___________;
③加入MnO2反應的化學方程式為____________;
(2)Na2O2有強氧化性,H2具有還原性,有同學猜想Na2O2與H2能反應。為了驗證此猜想,該小組同學進行加下實驗,實驗步驟和現象如下:
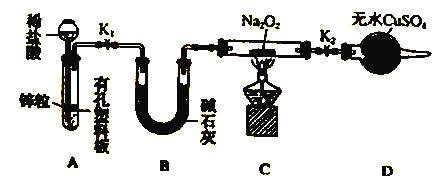
步驟1:按上圖組裝儀器(圖中夾持儀器省略),檢查氣密性,裝入藥品。
步驟2:打開K1、K2,產生的氫氣流經裝有Na2O2的硬質玻璃管,一段時間后沒有任何現象。
步驟3: ,開始加熱,觀察到硬質玻璃管內Na2O2開始熔化,淡黃色的粉末變成了白色固體,干燥管內硫酸銅未變藍色。
步驟4:反應后撤去酒精燈,待硬質玻璃管冷卻后關閉K1。
①添加稀鹽酸的儀器名稱是______,B裝置的作用_________。
②步驟3在點燃C處酒精燈前必須進行的操作是______________;
③裝置D的目的是_________;
④你得到的結論是________(若能反應請用化學方程式表示);
⑤該實驗設計中存在著明顯不足之處,應該如何改進:___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A. 離子晶體中每個離子的周圍均吸引著6個帶相反電荷的離子
B. 金屬導電的原因是在外加電場的作用下金屬產生自由電子,電子定向運動
C. 分子晶體的熔沸點低,常溫下均呈液態或氣態
D. 原子晶體中的各相鄰原子都以共價鍵相結合
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com