
(14分)丙烷在燃燒時能放出大量的熱,它也是液化石油氣的主要成分,作為能源應用于人們的日常生產和生活。
已知:

(1)反應
(2)現(xiàn)有1mol C3H8在不足量的氧氣里燃燒,生成1mol CO和2mol CO2以及氣態(tài)水,將所有的產物通入一個固定體積為1L的密閉容器中,在一定條件下發(fā)生如下可逆反應:

①下列事實能說明該反應達到平衡的是
a.體系中的壓強不發(fā)生變化
b.
c.混合氣體的平均相對分子質.量不發(fā)生變化
d.CO2的濃度不再反生變化
②5min后體系達到平衡,經測定,H2為0.8mol,則v(H2)= 。
③向平衡體系中充入少量CO則平衡常數___ _(填“增大”、“減小”或“不變”)。
(3)依據(1)中的反應可以設計一種新型燃料電池,一極通入空氣,另一極通入丙烷氣體;燃料電池內部是熔融的摻雜著氧化釔(Y2O3)的氧化鋯(ZrO2)晶體,在其內部可以傳導O2—。在電池內部O2—由__ __極移向___ _極(填“正”或“負”);電池的正極電極反應式為 。
(4)用上述燃料電池用惰性電極電解足量Mg(NO3)2和NaCl的混合溶液。電解開始后陰極的現(xiàn)象為____ 。
(1) -2219.9kJ/mol(2分)
(2)①bd(2分) ②0.16 mol/(L·min) (2分) ③不變(2分)
(3)正、負(2分) O2+ 4e- ="2" O2- (2分)
(4)有大量無色氣泡(或氣體)產生,并且有白色沉淀產生 (2分)
【解析】
試題分析:(1)根據蓋斯定律,此反應的反應熱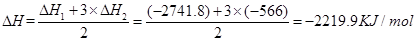 。
。
(2)①判斷反應是否達到平衡狀態(tài),主要看正逆反應速率是否相等。因此答案為bd。
②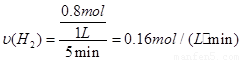
③平衡常數只受溫度的影響,加入CO,會影響平衡的移動,但不改變平衡常數,故平衡常數不變。
(3)電池的正極反應式為O2+4e- =2O2-,故在電池內部O2—由正極移向負極。
(4)用惰性電極電解足量Mg(NO3)2和NaCl的混合溶液時,陰極上放電的離子為氯離子,因此可觀察到的現(xiàn)象為產生氣泡,并有白色沉淀生成。
考點:電化學基礎;熱化學方程式
點評:本題是對電化學及熱化學的綜合考查,屬于能力提升題。也是高考中常考的綜合題。復習備考過程中,學生應特別注意加強對這類題型的訓練。解題的關鍵在于知識的綜合應用。


 中考解讀考點精練系列答案
中考解讀考點精練系列答案 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案科目:高中化學 來源:2013-2014學年湖北省孝感市高三第二次統(tǒng)考理綜化學試卷(解析版) 題型:填空題
丙烷在燃燒時能放出大量的熱,它也是液化石油氣的主要成分,作為能源應用于人們的日常生產和生活。已知:
①2C3H8(g) +7O2(g) = 6CO(g)+8H2O(g)?? △H = -2389.8 kJ/mol
②2CO(g) + O2(g) = 2CO2(g)????????????? △H = -566 kJ/mol
③H2O(l) = H2O(g)???? △H = + 44.0 kJ/mol
(1)寫出C3H8燃燒時燃燒熱的熱化學方程式???????????????????????????????????????????? 。
(2)C3H8在不足量的氧氣里燃燒,生成CO、CO2、H2O(g),將所有的產物通入一個體積固定的密閉
容器中,在一定條件下發(fā)生如下可逆反應: CO(g) +? H2O(g) CO2(g) +? H2(g)
CO2(g) +? H2(g)
該反應的平衡常數與溫度的關系如下表:
溫度/℃ | 400 | 500 | 800 |
平衡常數K | 9.94 | 9 | 1 |
保持溫度為800℃,在甲、乙兩個恒容密閉容器中,起始時按照下表數據進行投料,充分反應直至達到平衡。
| H2O | CO | CO2 | H2 |
甲 (質量/g) | 1.8 | 8.4 | a | 1 |
乙 (質量/g) | 1.8 | 2.8 | 0 | 0 |
①起始時,要使甲容器中反應向正反應方向進行,則a的取值范圍是????????????????? ;達到平衡
時,乙容器中CO的轉化率為???????? 。
②如圖表示上述甲容器中反應在t1時刻達到平衡,在t2時刻因改變某一個條件而發(fā)生變化的情況。則t2時刻改變的條件可能是???????????????????????????? 、??????????????????? (答兩個要點即可)。

(3)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3。
① Na2CO3溶液中離子濃度由大到小的順序為 ?????????? ??? ;
② 已知25℃時,H2CO3的電離平衡常數K1 = 4.4×10-7 mol/L、K2 = 4.7×10-11 mol/L,當Na2CO3溶液的pH為11時, 溶液中c(HCO3-)∶c(CO32-) = ?????????? 。
③ 0.1 mol/L Na2CO3溶液中c(OH-) - c(H+ ) = ?????????????????????? [用含c(HCO3-)、c(H2CO3)的符號表示]。
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com