
碘化鈉是常用的分析試劑,還用于醫療、照相業。工業上用鐵屑還原法制備NaI,其主要流程如下,請回答問題:

已知:NaI易被空氣氧化;反應②為:3Fe + IO3-+ 3H2O → 3Fe (OH)2 ↓ +I-
40.實驗室灼燒Fe(OH)2主要在 進行(填儀器名稱);灼燒后的副產品是 __________(寫化學式)。
41.判斷①中碘單質是否完全反應的實驗方法是 ;
42.實驗室配制一定量10%NaOH溶液,其操作步驟是 。
43.測定產品中NaI含量的方法是:
a.稱取3.000 g樣品、溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待測溶液于錐形瓶中;
c.用0.1000 mol·L-1AgNO3溶液滴定至終點,消耗AgNO3溶液體積的平均值為19.00 mL。
①測定過程所需儀器在使用前需要檢查是否漏液的有 。
② 該樣品中NaI的質量分數為 。
③ 若測定結果偏低,試分析可能的原因(任寫兩條):
、 。
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:閱讀理解
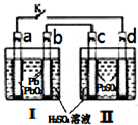 飛機、汽車、拖拉機、坦克,都是用蓄電池作為照明光源是典型的可充型電池,總反應式為:
飛機、汽車、拖拉機、坦克,都是用蓄電池作為照明光源是典型的可充型電池,總反應式為:
| ||
| 充電 |
| 實驗內容 | 實驗方法 | 實驗現象及原因分析 |
| ①碘離子濃度增大對平衡的影響 | 取PbI2飽和溶液少量于一支試管中,再加入少量NaI飽和溶液, 取PbI2飽和溶液少量于一支試管中,再加入少量NaI飽和溶液, |
溶液中出現黃色渾濁. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp 溶液中出現黃色渾濁. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp |
| ②鉛離子濃度減小對平衡的影響 | 取PbI2懸濁液少量于一支試管中,再加入少量NaCl飽和溶液 取PbI2懸濁液少量于一支試管中,再加入少量NaCl飽和溶液 |
黃色渾濁消失 原因是形成PbCl42-,導致溶液中c(Pb2+)減小,使Qc小于了pbI2的Ksp 黃色渾濁消失 原因是形成PbCl42-,導致溶液中c(Pb2+)減小,使Qc小于了pbI2的Ksp |
| ③ 鉛離子和碘離子濃度都減小對平衡的影響 鉛離子和碘離子濃度都減小對平衡的影響 |
在PbI2懸濁液中加入少量FeCl3飽和溶液 | PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
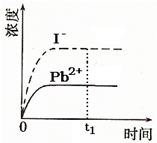 ④已知室溫下PbI2的Ksp=8.0×10-9,將適量PbI2固體溶于 100mL水中至剛好飽和,該過程中Pb2+和I-濃度隨時間變化關系如圖(飽和PbI2溶液中c(I-)=0.0025mol?L-1).若t1時刻在上述體系中加入100mL.、0.020mol?L-1 NaI 溶液,畫出t1時刻后Pb2+和I-濃度隨時間變化關系圖.
④已知室溫下PbI2的Ksp=8.0×10-9,將適量PbI2固體溶于 100mL水中至剛好飽和,該過程中Pb2+和I-濃度隨時間變化關系如圖(飽和PbI2溶液中c(I-)=0.0025mol?L-1).若t1時刻在上述體系中加入100mL.、0.020mol?L-1 NaI 溶液,畫出t1時刻后Pb2+和I-濃度隨時間變化關系圖.查看答案和解析>>
科目:高中化學 來源:2011年浙江省杭州市新理想高復學校高考化學模擬試卷(解析版) 題型:解答題
 2PbSO4+2H2O
2PbSO4+2H2O| 實驗內容 | 實驗方法 | 實驗現象及原因分析 |
| ①碘離子濃度增大對平衡的影響 | ______ | ______ |
| ②鉛離子濃度減小對平衡的影響 | ______ | ______ |
| ③______ | 在PbI2懸濁液中加入少量FeCl3飽和溶液 | ______ |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com