
在80℃時,0.40 mol的N2O4氣體充入2 L已經抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:
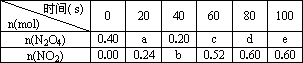
(1)計算20 s-40 s內用N2O4表示的平均反應速率為________.
(2)計算在80℃時該反應的平衡常數K________.
(3)能判斷該反應是否已達化學平衡狀態的依據是________.
a.容器中壓強不變
b.混合氣體中c(N2O4)不變
c.v正(NO2)=v逆(N2O4)
d.混合氣體密度不變
e.混合氣體的平均摩爾質量不變
f.c(N2O4)=c(NO2)
(4)反應進行至100 s后將反應混合物的溫度降低,混合氣體的顏色________(填“變淺”、“變深”或“不變”).
(5)要增大該反應的K值,可采取的措施有(填序號)________,若要重新達到平衡時,使[NO2]/[N2O4]值變小,可采取的措施有(填序號)________.
A.增大N2O4的起始濃度
B.向混合氣體中通入NO2
C.使用高效催化劑
D.升高溫度
(6)如下圖是80℃時容器中N2O4物質的量的變化曲線,請在該圖中補畫出該反應在60℃時N2O4物質的量的變化曲線.
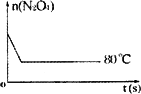
科目:高中化學 來源: 題型:
 在80℃時,0.40mol的N2O4氣體充入2L固定容積的密閉容器中發生如下反應:N2O4(g)?2NO2(g)△H>0,隔一段時間對該容器內的物質進行分析得到如下數據:
在80℃時,0.40mol的N2O4氣體充入2L固定容積的密閉容器中發生如下反應:N2O4(g)?2NO2(g)△H>0,隔一段時間對該容器內的物質進行分析得到如下數據:| n(mol) 時間(s) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化學 來源: 題型:
在80℃時,0.40mol的N2O4氣體充入 2L已經抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:
| 時間(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)計算20s—40s內用N2O4表示的平均反應速率為 。
(2)計算在 80℃時該反應的平衡常數K 。
(3)能判斷該反應是否已達化學平衡狀態的依據是________________。
a.容器中壓強不變
b.混合氣體中c(N2O4)不變
c.v正(NO2)=v逆(N2O4)
d.混合氣體密度不變
e.混合氣體的平均摩爾質量不變
f.c(N2O4)= c(NO2)
(4)反應進行至100s后將反應混合物的溫度降低,混合氣體的顏色 (填“變淺”、“變深”或“不變”)。
(5)要增大該反應的K值,可采取的措施有(填序號) ,若要重新達到平衡時,使[NO2]/[N2O4]值變小,可采取的措施有(填序號) 。
A.增大N2O4的起始濃度 B.向混合氣體中通入NO2
C.使用高效催化劑 D.升高溫度
(6)如右圖是 80℃時容器中N2O4物質的量的變化曲線,請在該圖中補畫出該反應在 60℃時N2O4物質的量的變化曲線。
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)在80℃時,0.40mol的N2O4氣體充入2L固定容積的密閉容器中發生如下反應:N2O4(g) 2 NO2(g) ΔH>0 ,隔一段時間對該容器內的物質進行分析得到如下數據:
|
| 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)求b、e的值:b= ,e=
(2)計算20s—40s內用N2O4表示的平均反應速率為 ;80℃該反應的化學平衡常數K為
(3)改變條件并達到新平衡,要使NO2在平衡體系中的含量變小,可采取的措施有(填序號) 。
A.向混合氣體中再通入N2O4 B.保持容積不變,通入He
C.使用高效催化劑 D.降低溫度
(4)如果在80℃、將0.40mol的N2O4氣體放入一個起始體積為2L、且壓強維持不變的容器中發生上述反應。則達到平衡時n(NO2) 0.60mol(填“ 大于 ” “等于” 或“ 小于”)
(5)如圖是80℃時容器中N2O4物質的量的變化曲線,請在該圖中補畫出該反應在60℃時N2O4物質的量的變化曲線。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年廣東汕頭市畢業班教學質量監測理綜化學部分 題型:填空題
在80℃時,0.40mol的N2O4氣體充入2L已經抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:
|
時間(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)計算20s~40s內用N2O4表示的平均反應速率為 。
(2)計算在80℃時該反應的平衡常數K 。
(3)反應進行至100s后將反應混合物的溫度降低,混合氣體的顏色 (填“變淺”、“變深”或“不變”)。
(4)要增大該反應的K值,可采取的措施有(填序號) ,若要重新達到平衡時,使[NO2]/[N2O4]值變小,可采取的措施有(填序號) 。
A.增大N2O4的起始濃度 B.向混合氣體中通入NO2
C.使用高效催化劑 D.升高溫度
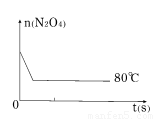
(5)如右圖是80℃時容器中N2O4物質的量的變化曲線,請在該圖中補畫出該反應在60℃時N2O4物質的量的變化曲線。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com