
LiPF6是鋰離子電池中廣泛應用的電解質。某工廠用LiF、PCl5為原料,低溫反應制備LiPF6,其流程如下:
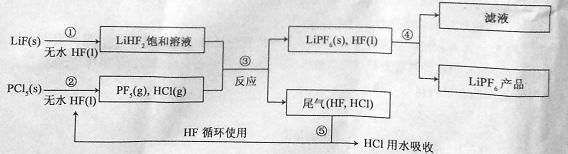
已知:HCl的沸點是-85.0 ℃,HF的沸點是19.5 ℃。
(1)第①步反應中無水HF的作用是 、 。反應設備不能用玻璃材質的原因是 (用化學方程式表示)。無水HF有腐蝕性和毒性,工廠安全手冊提示:如果不小心將HF沾到皮膚上,可立即用2%的 溶液沖洗。
(2)該流程需在無水條件下進行,第③步反應中PCl5極易水解,其產物為兩種酸,寫出PCl5水解的化學方程式: 。
(3)第④步分離采用的方法是 ;第⑤步分離尾氣中HF、HCl采用的方法是 。
(4)LiPF6產品中通常混有少量LiF。取樣品wg。測得Li的物質的量為nmol,則該樣品中LiPF6的物質的量為 mol(用含有w、n的代數式表示)。
 開心練習課課練與單元檢測系列答案
開心練習課課練與單元檢測系列答案 開心試卷期末沖刺100分系列答案
開心試卷期末沖刺100分系列答案科目:高中化學 來源: 題型:
化學式為C8H10O的化合物A具有如下性質:
 |
①A+Na—→慢慢產生氣泡 ②A+RCOOH 有香味的產物
 ④其催化脫氫產物不能發生銀鏡反應
④其催化脫氫產物不能發生銀鏡反應
⑤脫水反應的產物,經聚合反應可制得一種塑料品(它是目前造成“白色污染”的主要
污染源之一)
(1)根據上述信息,對該化合物的結構可做出的判斷是 。
A.苯環上直接連有羥基 B.苯環側鏈末端有甲基 C.肯定有醇羥基 D.肯定是芳香烴
(2)化合物A的結構簡式為 ;
(3)A和金屬鈉反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
室溫下,下列溶液中粒子濃度大小關系正確的是
A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
B.Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-)
D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
查看答案和解析>>
科目:高中化學 來源: 題型:
茶葉中鐵元素的檢驗可經過以下四個步驟完成,各步驟中選用的實驗用品不能都用到的是( )


A.將茶葉灼燒灰化,選用①、②和⑨
B.用濃硝酸溶解茶葉灰并加蒸餾水稀釋,選用④、⑥和⑦
C.過濾得到的濾液,選用④、⑤和⑦
D.檢驗濾液中的Fe3+,選用③、⑧和⑩
查看答案和解析>>
科目:高中化學 來源: 題型:
氫能是最重要的新能源。儲氫作為氫能利用的關鍵技術,是當前關注的熱點之一。
⑴氫氣是清潔能源,其燃燒產物為 。
⑵NaBH4是一種重要的儲氫載體,能與水反應生成NaBO3,且反應前后B的化合價不變,該反應的化學方程式為,反應消耗1molNaBH4時轉移的電子數目為。
⑶儲氫還可借助有機物,如利用環已烷和苯之間的可逆反應來實現脫氫和加氫。

 (g)
(g)


 (g)+3H2(g)
(g)+3H2(g)
在某溫度下,向恒容容器中加入環已烷,其起始濃度為amol·L-1,平衡時苯的濃度為bmol·L-1,該反應的平衡常數K=
⑷一定條件下,題11圖所示裝置可實現有機物的電化學儲氫(忽略其它有機物)。


①導線中電子轉移方向為 。(用A、D表示)
②生成目標產物的電極反應式為 。
③該儲氫裝置的電流效率η= 。(η=生成目標產物消耗的電子數/轉移的電子總數×100%,計算結果保留小數點后1位。)
查看答案和解析>>
科目:高中化學 來源: 題型:
氯在飲用水處理中常用作殺菌劑,且HClO的殺菌能力比ClO-強。25℃時氯氣-氯水體系中存在以下平衡關系:
Cl2(g)  Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O  HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO  H+ + ClO- Ka=?
H+ + ClO- Ka=?
 其中Cl2(aq)、HClO和ClO-分別在三者中所占分數(α)隨pH變化的關系如圖所示。下列表述正確的是
其中Cl2(aq)、HClO和ClO-分別在三者中所占分數(α)隨pH變化的關系如圖所示。下列表述正確的是
A.Cl2(g)+ H2O  2H+ + ClO- + Cl- K=10-10.9
2H+ + ClO- + Cl- K=10-10.9
B.在氯處理水體系中,c(HClO) + c(ClO-) =c(H+)-c(OH-)
C.用氯處理飲用水時,pH=7.5時殺菌效果比pH=6.5時差
D.氯處理飲用水時,在夏季的殺菌效果比在冬季好
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com