
電化學原理在工業生產中有著重要的作用,請利用所學知識回答有關問題。
(1)用電解的方法將硫化鈉溶液氧化為多硫化物的研究具有重要的實際意義,將硫化物轉變為多硫化物是電解法處理硫化氫廢氣的一個重要內容。如圖,是電解產生多硫化物的實驗裝置:
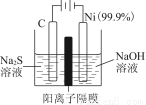
①已知陽極的反應為(x+1)S2-=Sx+S2-+2xe-,則陰極的電極反應式是________________________________________________________________________。
當反應轉移x mol電子時,產生的氣體體積為____________(標準狀況下)。
②將Na2S·9H2O溶于水中配制硫化物溶液時,通常是在氮氣氣氛下溶解。其原因是(用離子反應方程式表示):___________________________________________________。
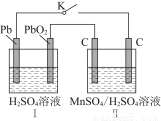
(2)MnO2是一種重要的無機功能材料,制備MnO2的方法之一是以石墨為電極,電解酸化的MnSO4溶液,陽極的電極反應式為______________________。現以鉛蓄電池為電源電解酸化的MnSO4溶液,如圖所示,鉛蓄電池的總反應方程式為_______________________________________________,當蓄電池中有4 mol H+被消耗時,則電路中通過的電子的物質的量為________,MnO2的理論產量為________g。
(3)用圖電解裝置可制得具有凈水作用的FeO42-。實驗過程中,兩極均有氣體產生,Y極區溶液逐漸生成FeO42-。

①電解過程中,X極區溶液的pH________(填“增大”“減小”或“不變”)。
②電解過程中,Y極發生的電極反應為Fe-6e-+8OH-=FeO42-+4H2O和________________________________________________________________________,
若在X極收集到672 mL氣體,在Y極收集到168 mL氣體(均已折算為標準狀況時氣體體積),則Y電極(鐵電極)質量減少________g。
(1)①2H2O+2e-=2OH-+H2↑(或2H++2e-=H2↑) 11.2x L
②2S2-+O2+2H2O=2S↓+4OH-
(2)Mn2+-2e-+2H2O=MnO2+4H+
Pb+PbO2+2H2SO4=2PbSO4+2H2O
2 mol 87
(3)增大 4OH--4e-=2H2O+O2↑ 0.28
【解析】(1)電解時,水電離的H+在陰極發生得電子還原反應,生成H2。根據電子守恒可知有x mol電子轉移,產生H2 0.5x mol。S2-具有較強還原性,易被空氣中的氧氣氧化,故配制溶液時需要氮氣作保護氣。
(2)根據題意Mn2+失電子生成MnO2,產物中的氧元素來源于水,生成H+,再將電極方程式配平即可。
(3)圖中X極的電極反應為2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-),所以X極區的pH增大,由生成氫氣672 mL,可知得電子數為0.06 mol,Y極生成氧氣為168 mL,失電子數0.03 mol,由得失電子守恒可知鐵失電子數為0.03 mol,由電極反應可知鐵溶解為0.005 mol,即0.28 g。


科目:高中化學 來源:2014高考化學名師知識點精編 專題15富集在海水的元素-氯溴碘練習卷(解析版) 題型:選擇題
下列反應的離子方程式書寫正確的是( )
A.在澄清石灰水中加入少量小蘇打:Ca2++OH-+HC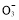
 CaCO3↓+H2O
CaCO3↓+H2O
B.苯酚鈉溶液中通入少量CO2:2C6H5O-+CO2+H2O 2C6H5OH+C
2C6H5OH+C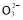
C.將少量SO2氣體通入NaClO溶液中:SO2+2ClO-+H2O S
S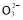 +2HClO
+2HClO
D.將標準狀況下112 mL氯氣通入10 mL濃度為1 mol·L-1的溴化亞鐵溶液中:2Fe2++4Br-+3Cl2 2Fe3++6Cl-+2Br2
2Fe3++6Cl-+2Br2
查看答案和解析>>
科目:高中化學 來源:2014高考化學名師知識點精編 專題11電化學練習卷(解析版) 題型:選擇題
用a、b兩個質量相等的Pt電極電解AlCl3和CuSO4的混合溶液[n(AlCl3)∶n(CuSO4)=1∶9]。t1時刻a電極得到混合氣體,其中Cl2在標準狀況下為224 mL(忽略氣體的溶解);t2時刻Cu全部在電極上析出。下列判斷正確的是( )
A.a電極與電源的負極相連
B.t2時,兩電極的質量相差3.84 g
C.電解過程中,溶液的pH不斷增大
D.t2時,b的電極反應是4OH--4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化學 來源:2014高考化學名師知識點精編 專題10鹽類水解與沉淀溶解平衡練習卷(解析版) 題型:選擇題
25 ℃時,濃度為0.2 mol/L的NaHCO3溶液中,下列判斷不正確的是( )
A.存在電離平衡HC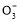
 H++C
H++C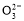
B.存在水解平衡HC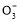 +H2O
+H2O H2CO3+OH-
H2CO3+OH-
C.將溶液加熱蒸干、灼燒得Na2O2固體
D.加入NaOH固體,恢復到原溫度,c(OH-)、c(C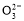 )均增大
)均增大
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題9電化學原理練習卷B(解析版) 題型:選擇題
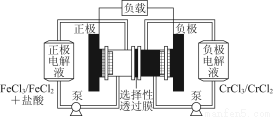
鐵鉻氧化還原液流電池是一種低成本的儲能電池,電池結構如圖所示,工作原理為Fe3++Cr2+ Fe2++Cr3+。下列說法一定正確的是( )
Fe2++Cr3+。下列說法一定正確的是( )
A.充電時,陰極的電極反應式為Cr3++e-=Cr2+
B.電池放電時,負極的電極反應式為Fe2+-e-=Fe3+
C.電池放電時,Cl-從負極室穿過選擇性透過膜移向正極室
D.放電時,電路中每流過0.1 mol電子,Fe3+濃度降低0.1 mol·L-1
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題9電化學原理練習卷A(解析版) 題型:選擇題
有一種鋰電池,用金屬鋰和石墨作電極材料,電解質溶液是由四氯化鋁鋰(LiAlCl4)溶解在亞硫酰氯(SOClCl)中形成的,其電池總反應方程式為8Li+3SOCl2=6LiCl+Li2SO3+2S。下列敘述中正確的是( )
A.電解質溶液可以用水,也可以用飽和食鹽水
B.電池工作過程中,亞硫酰氯(SOCl2)被還原成Li2SO3
C.電池工作時,鋰電極為正極,石墨電極為負極
D.電池工作過程中,金屬鋰提供的電子與正極區析出的硫的物質的量之比為4∶1
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題8電解質溶液練習卷B(解析版) 題型:實驗題
人體血液里Ca2+離子的濃度一般采用mg/mL來表示。加適量的草酸銨[(NH4)2C2O4]溶液,可析出草酸鈣(CaC2O4)沉淀,將此草酸鈣沉淀洗滌后溶于強酸可得草酸(H2C2O4),再用KMnO4溶液滴定,使草酸轉化成CO2逸出。
試回答:
(1)現需要80 mL 0.02 mol·L-1標準KMnO4溶液來進行滴定,則配制溶液時需要的玻璃儀器有燒杯、玻璃棒和______________________;配制時, KMnO4溶液應用強酸酸化,本實驗選擇________作酸化劑。若選擇HNO3酸化,則結果可能________(填“偏大”“偏小”或“不變”)。
(2)草酸與KMnO4反應的離子方程式為______________________________________
(3)滴定時,根據現象___________________________________
即可確定反應達到終點。
(4)滴定的實驗數據如下所示:
實驗編號 | 待測血液的體積/mL | 滴入KMnO4溶液的體積/mL |
1 | 20.00 | 11.95 |
2 | 20.00 | 13.00 |
3 | 20.00 | 12.05 |
經過計算,血液樣品中Ca2+離子的濃度為________mg/mL。
(5)滴定的方法有酸堿中和滴定、沉淀滴定、絡合滴定等。沉淀滴定所用的指示劑本身就是一種沉淀劑。以AgNO3標準溶液測定Cl-為例:
終點前:Ag++Cl-=AgCl (白色)
終點時:2Ag++CrO42—=Ag2CrO4(磚紅色)
這是因為AgCl溶解度比Ag2CrO4更________的緣故。
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題8電解質溶液練習卷A(解析版) 題型:選擇題
常溫下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有關粒子的物質的量變化如圖8-2(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根據圖示判斷,下列說法正確的是( )
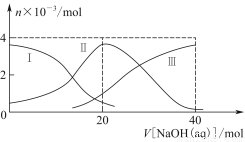
A.當V[NaOH(aq)]=20 mL時,溶液中離子濃度大小關系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水大
C.H2A第一步電離的方程式為H2A=HA-+H+
D.向NaHA溶液加入水稀釋的過程中,pH可能增大也可能減小
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題5化學反應中的能量變化練習卷(解析版) 題型:填空題
CH4、H2、C都是優質的能源物質,它們燃燒的熱化學方程式為:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1,
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1。
(1)在深海中存在一種甲烷細菌,它們依靠酶使甲烷與O2作用產生的能量存活,甲烷細菌使1 mol甲烷生成CO2氣體與液態水,放出的能量________(填“>”“<”或“=”)890.3 kJ。
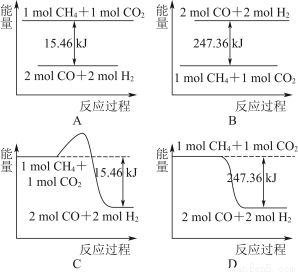
(2)甲烷與CO2可用于合成合成氣(主要成分是一氧化碳和氫氣):CH4+CO2=2CO+2H2,1 g CH4完全反應可釋放15.46 kJ的熱量,則:
①下圖能表示該反應過程中能量變化的是________(填字母)。
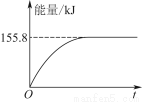
②若將物質的量均為1 mol的CH4與CO2充入某恒容密閉容器中,體系放出的熱量隨著時間的變化如圖所示,則CH4的轉化率為________。
(3)C(s)與H2(g)不反應,所以C(s)+2H2(g)=CH4(g)的反應熱無法直接測量,但通過上述反應可求出,C(s)+2H2(g)=CH4(g)的反應熱ΔH=________。
(4)目前對于上述三種物質的研究是燃料研究的重點,下列關于上述三種物質的研究方向中可行的是________(填字母)。
A.尋找優質催化劑,使CO2與H2O反應生成CH4與O2,并放出熱量
B.尋找優質催化劑,在常溫常壓下使CO2分解生成碳與O2
C.尋找優質催化劑,利用太陽能使大氣中的CO2與海底開采的CH4合成合成氣(CO、H2)
D.將固態碳合成為C60,以C60作為燃料
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com