
| 方 案 | 現象或產物 |
| ①將鐵片置于CuSO4溶液中 | 鐵片上有亮紅色物質析出 |
| ②將鐵絲和銅絲分別在氯氣燃燒 | 產物分別為FeCl3和CuCl2 |
| ③將鐵片和銅片分別置于稀硫酸溶液中 | 鐵片上有氣泡產生,銅片上無氣泡產生 |
| ④將鐵片和銅片置于盛有稀硫酸的燒杯中,并用導線連接 | 鐵片溶解,銅片上有氣泡產生 |
分析 (1)該原電池中,Zn易失電子作負極,Ag作正極,正極上氫離子得電子發生還原反應;
(2)該原電池中,負極上鋅溶解、正極上生成氫氣,所以負極質量減少、正極質量不變,則反應前后電極質量減少的量是鋅的質量,根據轉移電子相等計算生成氫氣體積;根據鋅和轉移電子之間的關系式計算轉移電子物質的量;
(3)金屬的金屬活動性越強,其單質的還原性越強,金屬單質與酸或水反應越劇烈,較活潑金屬能從較不活潑金屬鹽溶液中置換出來,一般來說原電池中較活潑金屬作負極、較不活潑金屬作正極.
解答 解:(1)該原電池中,Zn易失電子作負極,Ag作正極,正極上氫離子得電子發生還原反應,電極反應式為2H++2e-=H2↑,故答案為:負;2H++2e-=H2↑;
(2)該原電池中,負極上鋅溶解、正極上生成氫氣,所以負極質量減少、正極質量不變,則反應前后電極質量減少的量是鋅的質量,則參加反應的鋅的質量=(60-47)g=13g,其物質的量=13g÷65g/mol=0.2mol,根據轉移電子相等得生成氫氣體積=$\frac{0.2mol×2}{2}×22.4L/mol$=4.48L;根據鋅和轉移電子之間的關系式得轉移電子物質的量=0.2mol×2=0.4mol,
故答案為:4.48;0.4;
(3)金屬的金屬活動性越強,其單質的還原性越強,金屬單質與酸或水反應越劇烈,較活潑金屬能從較不活潑金屬鹽溶液中置換出來,一般來說原電池中較活潑金屬作負極、較不活潑金屬作正極,
①將鐵片置于CuSO4溶液中,鐵片上有亮紅色物質析出,說明鐵能置換出Cu,則金屬活動性Fe>Cu,故正確;
②金屬的活動性強弱與失電子多少無關,所以不能據此判斷金屬性強弱,故錯誤;
③將鐵片和銅片分別置于稀硫酸溶液中,鐵片上有氣泡產生,銅片上無氣泡產生,說明鐵能置換出氫氣、Cu不能,則金屬活動性Fe>Cu,故正確;
④將鐵片和銅片置于盛有稀硫酸的燒杯中,并用導線連接,鐵片溶解,銅片上有氣泡產生,則Fe作負極、Cu作正極,所以金屬活動性Fe>Cu,故正確;
故答案為:①③④.
點評 本題考查原電池原理及金屬活動性強弱判斷,側重考查基本原理,明確正負極的判斷方法是解本題關鍵,知道金屬活動性強弱與失電子難易程度有關,與失電子多少無關,易錯選項是(3)②.


 黃岡小狀元解決問題天天練系列答案
黃岡小狀元解決問題天天練系列答案科目:高中化學 來源: 題型:選擇題
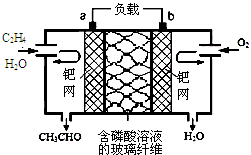 乙烯催化氧化生成乙醛可設計成如圖所示的燃料電池,能在制備乙醛的同時獲得電能,其總反應為:2CH2═CH2+O2→2CH3CHO.下列有關說法正確的是( )2.
乙烯催化氧化生成乙醛可設計成如圖所示的燃料電池,能在制備乙醛的同時獲得電能,其總反應為:2CH2═CH2+O2→2CH3CHO.下列有關說法正確的是( )2.| A. | 該電池可以實現化學能和電能的相互轉化 | |
| B. | 電子移動方向:電極a→磷酸溶液→電極b | |
| C. | 正極反應式為:O2+4e-+2H2O═4OH- | |
| D. | 每有1mol 乙烯反應,則遷移2 mol H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
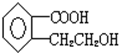
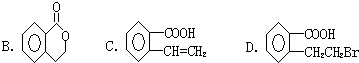
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化劑和還原劑的物質的量之比為1:8 | |
| B. | 該過程說明Fe(NO3)2溶液不宜加酸酸化 | |
| C. | 每1 mol NO3-發生氧化反應,轉移8 mol 電子 | |
| D. | 若把該反應設計為原電池,則負極反應為Fe2+-e-═Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

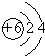 ;元素②的最高價氧化物結構式為:O=C=0;
;元素②的最高價氧化物結構式為:O=C=0;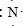 →
→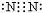 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.21的己烷所含的分子數為0.5 NA | |
| B. | 28g乙烯所含共用電子對數目為4 NA | |
| C. | 1mol苯乙烯中含有的C=C數為4NA | |
| D. | 2.8 g乙烯和丙烯的混合氣體中所含碳原子數為0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 壓強p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在基態多電子原子中,p軌道電子能量一定高于s軌道電子能量 | |
| B. | 根據原子核外電子排布的特點,Cu屬于s區元素 | |
| C. | 因氧元素電負性比氮元素大,故氧原子第一電離能比氮原子第一電離能大 | |
| D. | 核外電子排布由1s22s22p63s1-→1s22s22p6 的變化需要吸收能量 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com